人体摄入锌不足会引起多种疾病,缺锌者可以在医生指导下通过服用葡萄糖酸锌口服液来补锌。已知葡萄糖酸锌的化学式为C12H22O14Zn。试计算:
(1)葡萄糖酸锌中,碳、氢、氧、锌元素的原子个数比为_______ 。
(2)葡萄糖酸锌的相对分子质量为_______ ,其中,碳、氢、氧元素的质量比为_______ 。
(3)现有一支20mL的葡萄糖酸锌口服液,其中含葡萄糖酸锌45.5mg,那么这支口服液中锌的质量为多少_______ ?(写出计算过程,结果精确到0.1)
(1)葡萄糖酸锌中,碳、氢、氧、锌元素的原子个数比为
(2)葡萄糖酸锌的相对分子质量为
(3)现有一支20mL的葡萄糖酸锌口服液,其中含葡萄糖酸锌45.5mg,那么这支口服液中锌的质量为多少
更新时间:2023-11-15 20:11:36
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】已知莽草酸的化学式为C7H10O5,请计算
(1)莽草酸是由__________ 种元素组成的。
(2)一个莽草酸分子中共含有__________ 个原子。
(3)174克莽草酸中含有__________ 克碳元素。
(1)莽草酸是由
(2)一个莽草酸分子中共含有
(3)174克莽草酸中含有
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】在抗击新型冠状病毒肺炎疫情中,常用的医用酒精是体积分数为75%的乙醇溶液,可用于杀菌消毒,乙醇的化学式为C2H5OH。请完成下列计算。
(1)乙醇分子中碳氢氧原子个数比为_______ ;
(2)乙醇中碳元素和氢元素的质量比为_______ ;
(3)92g乙醇中碳元素的质量为_______ g。
(1)乙醇分子中碳氢氧原子个数比为
(2)乙醇中碳元素和氢元素的质量比为
(3)92g乙醇中碳元素的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】2020年6月23日,北斗三号卫星导航系统最后一颗卫星由长征三号运载火箭成功发射。至此,整个系统55颗卫星织成一张“天网”。长征三号运载火箭的常规燃料有偏二甲肼(C2H8N2)、液氢,助燃剂有四氧化二氮(N2O4)、液氧。
(1)偏二甲肼的相对分子质量为 。
(2)偏二甲肼中氮元素与氢元素的质量比为 。
(3)写出求算四氧化二氮中氧元素质量分数的计算式: 。
(4)ag四氧化二氮与32g氧气中氧元素质量相等,则a= 。
(1)偏二甲肼的相对分子质量为 。
(2)偏二甲肼中氮元素与氢元素的质量比为 。
(3)写出求算四氧化二氮中氧元素质量分数的计算式: 。
(4)ag四氧化二氮与32g氧气中氧元素质量相等,则a= 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】钙是人体内含量最高的金属元素,缺钙者可以在医生的指导下口服葡萄糖酸钙溶液来补钙,如表为某品牌“葡萄糖酸钙口服溶液”的部分说明。
葡萄糖酸钙的相对分子质量为430,请计算:
请计算:
(1)x为____________ 。
(2)葡萄糖酸钙中钙的质量分数为_________ 。(保留一位小数)
(3)如果小明每天需摄入钙的量为1000mg,他通过食物的钙摄入量为721mg,你建议他每天应该服用该品牌口服液_________ 支来补充钙摄入量的不足。(写出计算过程)
| 葡萄糖酸钙口服溶液 【成分】本品每毫升含葡萄糖酸钙【(CxH11O7)2Ca】100mg(相当于钙9.3mg) 【包装】每支装10mL,每盒12支。 |
请计算:
(1)x为
(2)葡萄糖酸钙中钙的质量分数为
(3)如果小明每天需摄入钙的量为1000mg,他通过食物的钙摄入量为721mg,你建议他每天应该服用该品牌口服液
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】SCR(选择性催化还原)技术可有效降低柴油发动机在空气过量条件下的NO2排放。其工作原理如图所示:
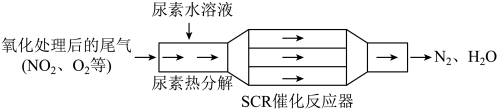
(注:尿素[CO(NH2)2]水溶液受热生成NH3和CO2,CO(NH2)2+H2O CO2↑+2NH3↑)
CO2↑+2NH3↑)
(1)CO(NH2)2相对分子质量是_______。
(2)反应器中与NO2的发生反应的物质为_______(填化学式)。
(3)尿素溶液中尿素含量会影响NO2的转化,测定溶液中尿素含量的方法如下:取100g尿素溶液,将所含氮完全转化为NH3,所得NH3用49g硫酸溶液完全吸收,得到55.8g硫酸铵溶液,则尿素溶液中溶质的质量分数是多少?已知:2NH3+H2SO4=(NH4)2SO4。

(注:尿素[CO(NH2)2]水溶液受热生成NH3和CO2,CO(NH2)2+H2O
 CO2↑+2NH3↑)
CO2↑+2NH3↑)(1)CO(NH2)2相对分子质量是_______。
(2)反应器中与NO2的发生反应的物质为_______(填化学式)。
(3)尿素溶液中尿素含量会影响NO2的转化,测定溶液中尿素含量的方法如下:取100g尿素溶液,将所含氮完全转化为NH3,所得NH3用49g硫酸溶液完全吸收,得到55.8g硫酸铵溶液,则尿素溶液中溶质的质量分数是多少?已知:2NH3+H2SO4=(NH4)2SO4。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】如图是一袋化肥标签的一部分,

请回答:
(1)CO(NH2)2的相对分子质量为:____________ 。
(2)CO(NH2)2中各元素的质量比为C∶O∶N∶H =__________ 。
(3)CO(NH2)2中N元素的质量分数为:___________ (保留一位小数)。
(4)一位农民计划施加2 kg该化肥,则给农作物施加的N元素质量为:____________ kg。
(5)该袋化肥中尿素的质量分数为:____________ (保留一位小数)。

请回答:
(1)CO(NH2)2的相对分子质量为:
(2)CO(NH2)2中各元素的质量比为C∶O∶N∶H =
(3)CO(NH2)2中N元素的质量分数为:
(4)一位农民计划施加2 kg该化肥,则给农作物施加的N元素质量为:
(5)该袋化肥中尿素的质量分数为:
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】二氧化碳是一种宝贵的碳氧资源。以CO2和NH3合成尿素CO(NH2)2是固定和利用CO2的成功范例,该反该反应的化学方程式为CO2+2NH3=CO(NH2)2+H2O。
请计算:
(1)尿素中C、O、N、H四种元素的质量比__ 。
(2)若按上述方法生产120 t尿素,可固定的CO2的质量为多少__ 。
请计算:
(1)尿素中C、O、N、H四种元素的质量比
(2)若按上述方法生产120 t尿素,可固定的CO2的质量为多少
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】乳酸亚铁片可用于治疗缺铁性贫血。下图为乳酸亚铁片说明书上的部分文字。请仔细阅读后回答以下问题:
(1)1个乳酸亚铁分子中有___________ 个原子。
(2)117g乳酸亚铁中铁元素的质量为多少?(写出计算过程)
(3)某人每天分两次服药,一次最多服用___________ 片,服药时不能喝茶的原因是___________ 。
| [主要成分]乳酸亚铁,化学式为C6H10FeO6 [用量]成人治疗量为0.3g/日~0.6g/日 [注意事项]1.宜饭后口服 2.服时忌茶,以免被鞣质沉淀 [规格]0.1g/片 |
(1)1个乳酸亚铁分子中有
(2)117g乳酸亚铁中铁元素的质量为多少?(写出计算过程)
(3)某人每天分两次服药,一次最多服用
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】碳酸氢铵[化学式为NH4HCO3]是一种常见的化学肥料。
1.(1)使用说明:“本品宜存贮于干燥阴冷处,防止受潮,施用后盖土或立即灌溉,避免爆晒或与碱性物质混合使用,以免肥效损失。”根据上面叙述,写出碳酸氢铵的两条性质:①______________ ; ②_______________ 。
2.(2)碳酸氢铵是价格较低的化肥,与其氮元素的质量分数有关,请求出碳酸氢铵中氮元素的质量分数。________ (精确到1%,写出计算过程,下同)。
3.(3)施用100千克的碳酸氢铵可为田地增加多少千克氮元素?________ (精确到1kg)
1.(1)使用说明:“本品宜存贮于干燥阴冷处,防止受潮,施用后盖土或立即灌溉,避免爆晒或与碱性物质混合使用,以免肥效损失。”根据上面叙述,写出碳酸氢铵的两条性质:①
2.(2)碳酸氢铵是价格较低的化肥,与其氮元素的质量分数有关,请求出碳酸氢铵中氮元素的质量分数。
3.(3)施用100千克的碳酸氢铵可为田地增加多少千克氮元素?
您最近一年使用:0次



