某学习小组在实验室中用加热高锰酸钾(KMnO4)方法制取氧气,反应过程中固体质量变化如图所示,请回答下列问题。(已知:含钾元素的化合物都能溶于水)
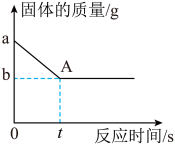
(1)写出图中A点固体的成分________ (填物质名称或化学式均可)。A点固体属于________ 物(填物质类别)。
(2)将分解后剩余固体中的不溶物分离出来的操作方法是加水溶解后________ 。该操作中需用到的玻璃仪器有烧杯、________ 、________ 。
(3)高锰酸钾中钾、锰、氧的元素质量比是________ 。
(4)含6.4克氧元素的高锰酸钾质量为多少克?(写计算过程,结果保留到0.1克)

(1)写出图中A点固体的成分
(2)将分解后剩余固体中的不溶物分离出来的操作方法是加水溶解后
(3)高锰酸钾中钾、锰、氧的元素质量比是
(4)含6.4克氧元素的高锰酸钾质量为多少克?(写计算过程,结果保留到0.1克)
更新时间:2023-11-26 09:58:33
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】在现代生活中,人们越来越注重微量元素的摄取。碘元素对人体有着至关重要的作用。
上图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答下列问题:
(1)“食用碘盐”属于_____ (填“纯净物”或“混合物”)。
(2)碘酸钾(KIO3)中钾元素、碘元素的质量比是_____ 。
(3)碘酸钾(KIO3)中碘元素的质量分数是_____ 。(计算结果精确到0.1%)
| 碘盐 配料:氯化钠、碘酸钾(KIO3) 含碘量:(20~30)mg/kg 保质期:18个月 食用方法:勿长时间炖炒 贮藏指南:避光、避热、密封防潮 |
上图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答下列问题:
(1)“食用碘盐”属于
(2)碘酸钾(KIO3)中钾元素、碘元素的质量比是
(3)碘酸钾(KIO3)中碘元素的质量分数是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某实验小组为测定实验室中氯酸钾样品中氨酸钾的质量分数,取10g该样品与1g二氧化锰均匀混合,将该混合物充分加热至完全反应,冷却后称量剩余固体的质量为7.16g。
(1)从物质分类的角度看,剩余固体属于___________ (填“纯净物”或“混合物”);
(2)完全反应后产生氧气的质量为___________ g;
(3)计算该样品中氯酸钾的质量分数。
(4)若实验中氯酸钾未完全反应就停止加热,则会导致测定结果___________ (填“不变”“偏大”或“偏小”。)
(1)从物质分类的角度看,剩余固体属于
(2)完全反应后产生氧气的质量为
(3)计算该样品中氯酸钾的质量分数。
(4)若实验中氯酸钾未完全反应就停止加热,则会导致测定结果
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】钙在人体生长发育过程中,有着极为重要的作用.青少年适量补钙有助于身高发育,可减轻生长过快引起的骨骼疼痛等症状.如图1为某钙片的商品标签,为测定钙片中钙元素的质量分数(假设钙片中其他物质不含钙元素,且不溶于水,也不与任何物质发生反应),某化学兴趣小组取20片钙片,如图2进行如下实验:

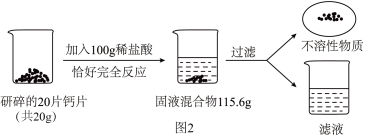
(1)过滤操作中用到玻璃仪器主要有烧杯、玻璃棒和_______________ ,其中玻璃棒的作用是_______________ ;
(2)钙片属于_______________ (选填“纯净物”“混合物”之一);标签中介绍钙片的功能是“补钙”,这里的“钙”指的是_______________ (选填“单质”“原子”“元素”之一)。
(3)图2的实验过程中,产生的二氧化碳的质量为_______________ g。
(4)计算钙片中碳酸钙的质量分数_______ (写出计算过程)。
(5)如果按说明书中的用量服用,服用者每天通过该补钙剂实际摄入钙元素的质量为_______ g。


(1)过滤操作中用到玻璃仪器主要有烧杯、玻璃棒和
(2)钙片属于
(3)图2的实验过程中,产生的二氧化碳的质量为
(4)计算钙片中碳酸钙的质量分数
(5)如果按说明书中的用量服用,服用者每天通过该补钙剂实际摄入钙元素的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某化学小组为测定实验室里一瓶盐酸的溶质质量分数,取纯净碳酸钙粉末8g于烧杯中,加入50g该盐酸溶液,充分反应后,过滤、洗涤、干燥,称量得剩余固体3g。请计算:
(1)CaCO3中碳元素与氧元素的质量比(只写结果);
(2)该盐酸的溶质质量分数。
(1)CaCO3中碳元素与氧元素的质量比(只写结果);
(2)该盐酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将一定质量的氯化钡固体粉末加到12.2g硫酸钠溶液中,搅拌、振荡,恰好完全反应,将反应后溶液过滤得到固体沉淀4.66g。计算:
(化学方程式:BaCl2+Na2SO4=BaSO4↓ + 2NaCl )
(1)硫酸钠中硫元素和氧元素的质量比为:______ 。
(2)反应后生成氯化钠的质量是多少g?
(3)反应后溶液中溶质的质量分数为多少?
(化学方程式:BaCl2+Na2SO4=BaSO4↓ + 2NaCl )
(1)硫酸钠中硫元素和氧元素的质量比为:
(2)反应后生成氯化钠的质量是多少g?
(3)反应后溶液中溶质的质量分数为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】《千里江山图》描绘了古代中国的青秀山水,用到传统颜料石绿。石绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3]。化学兴趣小组利用稀盐酸测定50g石绿中碱式碳酸铜的质量。将石绿放入烧杯中,逐滴加入溶质质量分数为10%的稀盐酸至恰好完全反应,共用去稀盐酸146g。
(提示:1. Cu2(OH)2CO3+4HCl=2CuCl2+CO2↑+3H2O。2.假定石绿中其他成分既不溶于水,也不参与反应。3. Cu2(OH)2CO3的相对分子质量为222。)
求:
(1)Cu2(OH)2CO3中碳元素与氧元素的质量比是___
(2)50g石绿中碱式碳酸铜的质量是___ g。
(3)完全反应后,溶液中溶质的质量分数是?(写出计算过程,结果精确到0.1%)
(提示:1. Cu2(OH)2CO3+4HCl=2CuCl2+CO2↑+3H2O。2.假定石绿中其他成分既不溶于水,也不参与反应。3. Cu2(OH)2CO3的相对分子质量为222。)
求:
(1)Cu2(OH)2CO3中碳元素与氧元素的质量比是
(2)50g石绿中碱式碳酸铜的质量是
(3)完全反应后,溶液中溶质的质量分数是?(写出计算过程,结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】“瘦肉精”学名盐酸克伦特罗,化学式为C12H18Cl2N2O,是一种非常廉价的药品,它有很危险的副作用,轻则导致心律不整,严重一点就会导致心脏病。根据以上信息,回答下列问题。
(1)“瘦肉精”中各元素的质量比为________ 。
(2)“瘦肉精”的相对分子质量为________ 。
(3)求554g瘦肉精中含有氯元素的质量为________ g。(本问写出计算过程)
(1)“瘦肉精”中各元素的质量比为
(2)“瘦肉精”的相对分子质量为
(3)求554g瘦肉精中含有氯元素的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】谷氨酸大量存在于谷类蛋白质中,在生物体内的蛋白质代谢过程中占重要地位,其分子结构如图所示(注“一”表示原子之间相互连接),试计算:
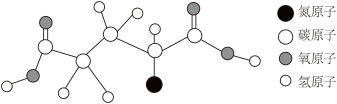
(1)在谷氨酸分子在碳、氢、氧、氮原子个数比为___________ 。
(2)29.4g谷氨酸中含氮元素的质量为___________ g。(结果精确到0.1克)

(1)在谷氨酸分子在碳、氢、氧、氮原子个数比为
(2)29.4g谷氨酸中含氮元素的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】实验室制取氧气时,某同学取一定量的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图所示,请回答下列问题:
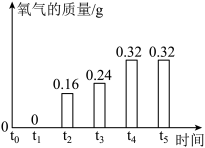
(1)理论计算:计算该同学所取高锰酸钾的质量。
(2)图形分析:t4~t5时段氧气质量不变的原因是___________ 。

(1)理论计算:计算该同学所取高锰酸钾的质量。
(2)图形分析:t4~t5时段氧气质量不变的原因是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某化学实验小组利用31.6g高锰酸钾制取氧气,固体质量变化如图所示。
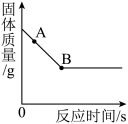
(1)A点时对应的固体成分为____________ 。(填物质化学式)
(2)求B点时生成氧气的质量。(写出计算过程)

(1)A点时对应的固体成分为
(2)求B点时生成氧气的质量。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】实验室有一瓶含杂质的高锰酸钾,兴趣小组同学取 该药品放入大试管中加热(杂质不参加反应),并在不同时刻测定试管内剩余固体物质的质量,实验数据记录如下,请回答:
该药品放入大试管中加热(杂质不参加反应),并在不同时刻测定试管内剩余固体物质的质量,实验数据记录如下,请回答:
(1)加热 时剩余固体质量为
时剩余固体质量为______ g;
(2)计算该样品中高锰酸钾的质量分数?
 该药品放入大试管中加热(杂质不参加反应),并在不同时刻测定试管内剩余固体物质的质量,实验数据记录如下,请回答:
该药品放入大试管中加热(杂质不参加反应),并在不同时刻测定试管内剩余固体物质的质量,实验数据记录如下,请回答:| 加热时间/min |  |  |  |  |  |  |  |
| 剩余固体质量/g | 10 | 10 | 9.24 | 9.16 | 9.04 | 9.04 |
 时剩余固体质量为
时剩余固体质量为(2)计算该样品中高锰酸钾的质量分数?
您最近一年使用:0次



