尿素【CO(NH2)2】是农民种植农作物的主要化肥,以下是我市某生物化工股份有限公司生产尿素的流程图,图中以经过除尘、除二氧化碳、除水的空气为原料生产尿素(部分生成物已省略),请回答有关问题。
【查阅资料】①常温下,氧气的沸点是-183℃,氮气的沸点是-196℃;②煤的主要成分是碳。
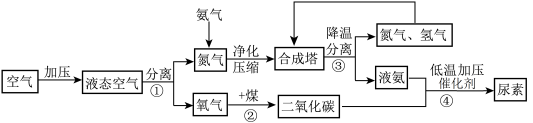
(1)工业利用液氮和液氧的_______ 不同分离得到氮气,其温度控制在-196℃到-183℃。
(2)请写出步骤②的符号表达式_______ 。
(3)合成塔中发生的化学反应属于基本反应类型中的_______ 反应。
(4)该生产流程中可以循环利用的物质是_______ 。
(5)若尿素中的氮元素可全部被农作物吸收利用,则_______ kg尿素可提供56kg氮元素。
【查阅资料】①常温下,氧气的沸点是-183℃,氮气的沸点是-196℃;②煤的主要成分是碳。

(1)工业利用液氮和液氧的
(2)请写出步骤②的符号表达式
(3)合成塔中发生的化学反应属于基本反应类型中的
(4)该生产流程中可以循环利用的物质是
(5)若尿素中的氮元素可全部被农作物吸收利用,则
更新时间:2023-12-06 09:56:26
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】写出符合下列要求物质的化学式:空气中含量最多的物质是__________ ;地壳中元素含量前两位的元素形成化合物的化学式为__________ 。
您最近一年使用:0次
【推荐2】无机非金属材料是目前研究的热点。
(1)氧化铝是一种重要的无机非金属材料,具有优异的物理、化学性质和广泛的应用前景请用化学用语填空。
①铝元素在地壳中含量(质量分数)位居第_______ (填数字)。
②2个氧分子_______ 。
③标出氧化铝中铝元素的化合价_______ 。
(2)某化工厂使用食盐和其他原料,采用侯德榜先生的联合制碱法生产纯碱。其主要流程如图所示:
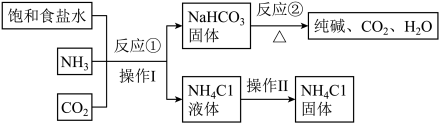
①操作I的名称是_______ 。
②该流程中可以循环利用的物质是_______ (填化学式)。
③反应①的化学方程式为_______ 。
(1)氧化铝是一种重要的无机非金属材料,具有优异的物理、化学性质和广泛的应用前景请用化学用语填空。
①铝元素在地壳中含量(质量分数)位居第
②2个氧分子
③标出氧化铝中铝元素的化合价
(2)某化工厂使用食盐和其他原料,采用侯德榜先生的联合制碱法生产纯碱。其主要流程如图所示:

①操作I的名称是
②该流程中可以循环利用的物质是
③反应①的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】1869年,门捷列夫发现了元素周期律,使化学学习和研究变得有规律可循。下图是1至18号元素和38号元素锶(元素符号为Sr)的原子结构示意图:
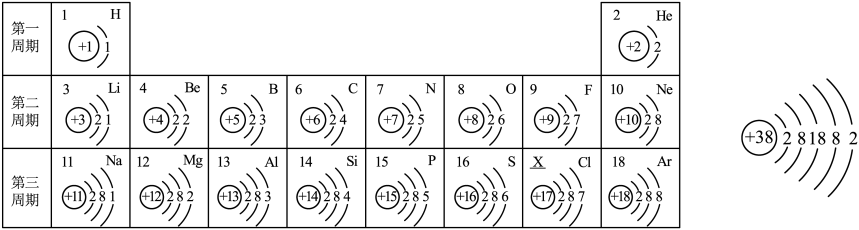
(1)上图中,X=_____________ 。
(2)锶原子在化学反应中容易_____________ (填“得到”或“失去”)电子,锶元素和氯元素形成化合物的化学式是_____________ 。
(3)通过分析图表可推测出锶元素位于元素周期表第________ 周期。
(4)Li元素与Na元素具有相似化学性质的原因是_________ 。
(5)磷原子的相对原子质量为31,中子数为_________ 。
(6)二硫化钼(MoS2)被认为是最有希望代替硅,成为未来应用在半导体芯片等高精尖领域中的理想材料之一。确定Mo为42号元素是依据其________(填字母)。

(1)上图中,X=
(2)锶原子在化学反应中容易
(3)通过分析图表可推测出锶元素位于元素周期表第
(4)Li元素与Na元素具有相似化学性质的原因是
(5)磷原子的相对原子质量为31,中子数为
(6)二硫化钼(MoS2)被认为是最有希望代替硅,成为未来应用在半导体芯片等高精尖领域中的理想材料之一。确定Mo为42号元素是依据其________(填字母)。
| A.质子数 | B.中子数 |
| C.化合价 | D.相对原子质量 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】尿素[CO(NH2)2]是一种常用化肥。下图为利用天然气(主要成分为CH4)制尿素的主要流程。
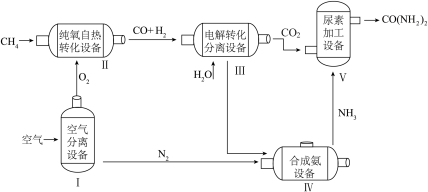
(1)设备Ⅰ内发生的是________________ (选填“物理”或“化学”)变化。
(2)设备Ⅳ中的反应必须在高温、高压并使用催化剂的条件下进行,该反应的符号表达式为________ 。
(3)结合流程分析碳元素的转化过程。请按转化的先后顺序写出含碳物质的化学式:CH4→_________ →_________ →CO(NH2)2
(4)农业生产中若施用120t尿素,可为农作物提供多少t氮元素?(写出计算过程)

(1)设备Ⅰ内发生的是
(2)设备Ⅳ中的反应必须在高温、高压并使用催化剂的条件下进行,该反应的符号表达式为
(3)结合流程分析碳元素的转化过程。请按转化的先后顺序写出含碳物质的化学式:CH4→
(4)农业生产中若施用120t尿素,可为农作物提供多少t氮元素?(写出计算过程)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】煤的气化和液化是目前实现煤综合利用的主要途径之一、以煤为原料合成甲醇(CH3OH)的流程如下:

(1)冷却器里发生的是_____ 变化(填“物理”或“化学”)。
(2)合成塔中发生的化学反应的微观示意图如下:
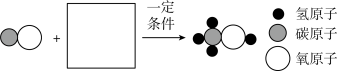
方框内另一种反应物的微粒示意图为_____ (填字母序号)。
A. B.
B. C.
C.
(3)甲醇(CH3OH)中C元素质量分数的计算式为_____ 。

(1)冷却器里发生的是
(2)合成塔中发生的化学反应的微观示意图如下:

方框内另一种反应物的微粒示意图为
A.
 B.
B. C.
C.
(3)甲醇(CH3OH)中C元素质量分数的计算式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于棉纺、造纸业的漂白剂,也用于食品消毒、水处理等,亚氯酸钠受热易分解。
(1)亚氯酸钠(NaClO2)在酸性溶液中生成HClO2而发生分解,分解的化学方程式:5HClO2═4X↑+HCl+2H2O。HClO2读作____ ,其中氯元素的化合价为___ ;X的化学式___ 。
(2)以氯酸钠(NaClO3)等为原料可以制备亚氯酸钠。氯酸钠受热会分解,其生成物与氯酸钾分解的生成物相似。除此以外,氯酸钠与氯酸钾还具有一些其它相似的化学性质。
①试写出氯酸钠受热分解的化学方程式___ 。
②试分析氯酸钠与氯酸钾具有相似化学性质的原因___ 。(填字母)
A 都含氯元素 B 都含氧元素 C 都含ClO3- D 以上都是
(1)亚氯酸钠(NaClO2)在酸性溶液中生成HClO2而发生分解,分解的化学方程式:5HClO2═4X↑+HCl+2H2O。HClO2读作
(2)以氯酸钠(NaClO3)等为原料可以制备亚氯酸钠。氯酸钠受热会分解,其生成物与氯酸钾分解的生成物相似。除此以外,氯酸钠与氯酸钾还具有一些其它相似的化学性质。
①试写出氯酸钠受热分解的化学方程式
②试分析氯酸钠与氯酸钾具有相似化学性质的原因
A 都含氯元素 B 都含氧元素 C 都含ClO3- D 以上都是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下图是在实验室完成的硫粉、铁丝、木炭在氧气中燃烧的实验。
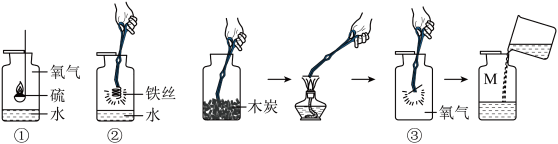
(1)写出上述实验①、②反应的文字表达式:①_______ ;②________ 。
(2)实验①中集气瓶内预先加少量水的目的是_______ 。
(3)实验②中将铁丝盘成螺旋状的目的是______ 。
(4)实验③中,木炭分别在空气、氧气中燃烧产生不同的现象,其原因是________ ;向集气瓶M中倾倒的液体名称是_______ ,其作用是_________ 。

(1)写出上述实验①、②反应的文字表达式:①
(2)实验①中集气瓶内预先加少量水的目的是
(3)实验②中将铁丝盘成螺旋状的目的是
(4)实验③中,木炭分别在空气、氧气中燃烧产生不同的现象,其原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,烧杯中盛有水,两个体积相等的集气瓶中都充满了空气。夹紧弹簧夹,并迅速将分别盛有适量燃着的红磷、木炭的燃烧匙伸入A、B瓶内,塞紧瓶塞。
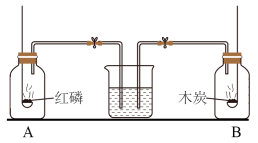
(1)待燃烧完毕,冷却至室温后,同时打开两个弹簧夹,则A瓶中发生的现象是______ ;该实验现象证明什么结论______ 。
(2)B瓶中发生反应的文字表达式是______ 。
(3)冷却后打开弹簧夹,B瓶中没有什么明显现象,请你分析B瓶中无明显现象的原因是______ 。

(1)待燃烧完毕,冷却至室温后,同时打开两个弹簧夹,则A瓶中发生的现象是
(2)B瓶中发生反应的文字表达式是
(3)冷却后打开弹簧夹,B瓶中没有什么明显现象,请你分析B瓶中无明显现象的原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】空气是宝贵的资源,绿色的莱西处处弥漫着清新的空气;请沿用科学家认识事物的方式认识“空气”。
(1)从分类角度:空气属于___________ (选填“混合物”或“纯净物”)。
(2)从微观角度:用“ ”表示氮原子,“
”表示氮原子,“ ”表示氧原子。同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,如图大约可表示空气微观模型的是___________(填标号)。
”表示氧原子。同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,如图大约可表示空气微观模型的是___________(填标号)。
(3)从应用角度:利用空气制取氮气和工业液氧的流程如下图所示。
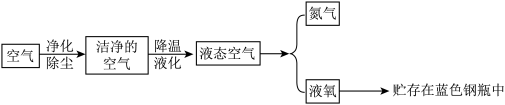
①氮气的沸点是−196℃,氧气的沸点是−183℃,在蒸发的过程中,___________ (填“氮气”或“氧气”)先被蒸发出来。
②下列选项中,不属于贮存在蓝色钢瓶中氧气的用途是___________ (填序号)。
A.气体肥料B.医疗急救C.气割气焊D.炼钢
③除分离液态空气外,现在还有一种膜分离技术制氧气,原理是在一定压力下,让空气通过薄膜,氧气能透过薄膜,从而达到分离空气的目的。据此推测氮分子比氧分子体积___________ (填“大”或“小”)。
(4)从环保角度:
下表为我市某监测点监测到的空气质量。依据表格回答问题:
说明:PM2.5是指细颗粒物,即粒径小于等于2.5微米的颗粒物;PM10是指可吸入颗粒物,即粒径小于等于10微米的颗粒物。
①污染指数越大,危害越大,该监测点的空气中危害最大的污染项目是___________ ;
②如图是我市城区街道上一辆新型环保车,通过360°旋转的“大炮筒”向四周喷水,这款环保车喷水的作用是___________ 。

(1)从分类角度:空气属于
(2)从微观角度:用“
 ”表示氮原子,“
”表示氮原子,“ ”表示氧原子。同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,如图大约可表示空气微观模型的是___________(填标号)。
”表示氧原子。同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,如图大约可表示空气微观模型的是___________(填标号)。A.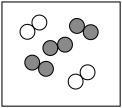 | B.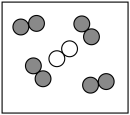 | C. |
(3)从应用角度:利用空气制取氮气和工业液氧的流程如下图所示。

①氮气的沸点是−196℃,氧气的沸点是−183℃,在蒸发的过程中,
②下列选项中,不属于贮存在蓝色钢瓶中氧气的用途是
A.气体肥料B.医疗急救C.气割气焊D.炼钢
③除分离液态空气外,现在还有一种膜分离技术制氧气,原理是在一定压力下,让空气通过薄膜,氧气能透过薄膜,从而达到分离空气的目的。据此推测氮分子比氧分子体积
(4)从环保角度:
下表为我市某监测点监测到的空气质量。依据表格回答问题:
| 污染项目 | PM2.5 | PM10 | SO2 | CO | NO2 |
| 污染指数 | 69 | 95 | 9 | 0.8 | 42 |
①污染指数越大,危害越大,该监测点的空气中危害最大的污染项目是
②如图是我市城区街道上一辆新型环保车,通过360°旋转的“大炮筒”向四周喷水,这款环保车喷水的作用是

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】氮气在高温、高能量条件下可与某些物质发生反应。下图是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题:
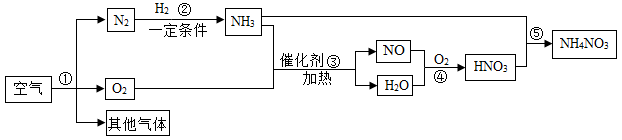
(1)步骤①中发生的是________ 变化(填“物理”或“化学”)。
(2)写出步骤③中发生反应的化学方程式__________ 。
(3)上述化学反应中属于化合反应的有________ 个。

(1)步骤①中发生的是
(2)写出步骤③中发生反应的化学方程式
(3)上述化学反应中属于化合反应的有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】空气是一种宝贵的资源,人类时时刻刻都离不开空气,人类对空气的探索之路从未停止。
(1)二百多年前,法国化学家______ 首先用定量的方法研究了空气的成分。化学课上老师使用红磷燃烧测定空气中氧气的含量,其文字表达式:______ ,该反应属于______ (填基本反应类型),如果实验结果小于五分之一,你认为可能的原因:______ (任写一条)。
(2)洁净的空气对人类非常重要。下列物质中属于空气污染物的是______ 。
a.可吸入颗粒物 b.二氧化氮 c.二氧化碳 d.氦气
(3)工业上用分离液态空气的方法来制备氧气,这主要是因为液态氮与液态氧的______ 不同。
(1)二百多年前,法国化学家
(2)洁净的空气对人类非常重要。下列物质中属于空气污染物的是
a.可吸入颗粒物 b.二氧化氮 c.二氧化碳 d.氦气
(3)工业上用分离液态空气的方法来制备氧气,这主要是因为液态氮与液态氧的
您最近一年使用:0次



