A、B、C、D、E均为初中化学常见的物质,它们之间的关系如图所示(图中“-”表示两物质之间能发生反应,“→”表示两物质之间能发生一步转化),其中A是世界上年产量最大的金属,C为气体单质,D是相对分子质量最小的氧化物,请回答下列问题:

(1)若E溶液中溶质是两种元素组成的物质,E溶液的名称是______ ,C物质的用途:______ 。
(2)A→B的基本反应类型为______ 。
(3)写出E→D的化学方程式______ 。
(4)已知 ,X中两元素的质量比为21:8,则X的化学式为
,X中两元素的质量比为21:8,则X的化学式为______ 。

(1)若E溶液中溶质是两种元素组成的物质,E溶液的名称是
(2)A→B的基本反应类型为
(3)写出E→D的化学方程式
(4)已知
 ,X中两元素的质量比为21:8,则X的化学式为
,X中两元素的质量比为21:8,则X的化学式为
更新时间:2024-01-16 08:59:44
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】请根据所学化学知识填写下列空白:
(1)我国自主研制的C919大型客机试飞成功,标志着我国飞机制造技术又有了大的飞跃。飞机外壳用的主要材料是铝合金,铝合金属于_____ 材料;空气中,铝比铁具有更好的抗腐蚀性,原因是_____ (用化学方程式表示)。
(2)载人航天飞船所用固体燃料是铝粉和高氯酸铵(NH4ClO4)的混合物,在高氯酸铵中氯元素的化合价是_____ 。
(3)味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于水)。味精中至少含有_____ 种元素,谷氨酸钠中各元素的质量比为 _____ 。
(1)我国自主研制的C919大型客机试飞成功,标志着我国飞机制造技术又有了大的飞跃。飞机外壳用的主要材料是铝合金,铝合金属于
(2)载人航天飞船所用固体燃料是铝粉和高氯酸铵(NH4ClO4)的混合物,在高氯酸铵中氯元素的化合价是
(3)味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于水)。味精中至少含有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】宏观与微观、实际质量与相对质量都是紧密相关的。根据它们的关系回。(填最简整数比,下同)
(1)①若镁、铜各为10kg,则其中所含有的原子个数比为___________ 。
②若镁、铜两种金属的原子个数都是6.02×1023个,那么镁、铜的质量比为______ 。
(2)含有相同质量氧元素时,需要CO与CO2的质量比为___________ 。
(1)①若镁、铜各为10kg,则其中所含有的原子个数比为
②若镁、铜两种金属的原子个数都是6.02×1023个,那么镁、铜的质量比为
(2)含有相同质量氧元素时,需要CO与CO2的质量比为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】2020年,罕见的新冠病毒疫情爆发,各种消毒剂如酒精、二氧化氯、过氧乙酸等被广泛使用,根据所学知识回答下列问题。
(1)使用酒精消毒时,要注意安全,避免失火,酒精(C2H5OH)在空气中完全燃烧的化学方程式为________ 。
(2)二氧化氯(CO2)具有强氧化性,可发生反应: ,则R的化学式为
,则R的化学式为________ 。
(3)过氧乙酸(CH3COOOH)中碳元素与氢元素的质量比为________ 。过氧乙酸溶液中通常还含有过氧化氢、醋酸等物质,向过氧乙酸溶液中加入二氧化锰,产生的现象是______ 。
(1)使用酒精消毒时,要注意安全,避免失火,酒精(C2H5OH)在空气中完全燃烧的化学方程式为
(2)二氧化氯(CO2)具有强氧化性,可发生反应:
 ,则R的化学式为
,则R的化学式为(3)过氧乙酸(CH3COOOH)中碳元素与氢元素的质量比为
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】写出下列变化涉及的化学方程式:
(1)酒精燃烧:__________ ;
(2)不能用铁桶配制波尔多液:__________ ;
(3)氢氧化钠溶液变质:__________ 。
(1)酒精燃烧:
(2)不能用铁桶配制波尔多液:
(3)氢氧化钠溶液变质:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】金属在日常生活、工农业生产和科学研究方面应用广泛。
(1)在空气中,铝表面生成一层致密的氧化膜,氧化膜的化学式是_____ 。
(2)某实验小组为了探究影响金属与酸反应快慢的因素,进行如表实验:
由此得出影响金属与酸反应快慢的因素有:a:_____ b:______ c: ______
(3)小明将一包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液。
①锌和硝酸银溶液反应的化学方程式是_____ 。
②若滤液为蓝色,则滤液中一定含有的金属离子是_____ 。(写离子符号)
(1)在空气中,铝表面生成一层致密的氧化膜,氧化膜的化学式是
(2)某实验小组为了探究影响金属与酸反应快慢的因素,进行如表实验:
| 实验序号 | 实验过程 | 实验现象 |
| a | 镁粉和铁粉分别与5%盐酸反应 | 镁粉产生气体快 |
| b | 铁粉和铁片分别与15%盐酸反应 | 铁粉产生气体快 |
| c | 铁片分别与5%盐酸和15%盐酸反应 | 15%盐酸产生气体快 |
(3)小明将一包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液。
①锌和硝酸银溶液反应的化学方程式是
②若滤液为蓝色,则滤液中一定含有的金属离子是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐3】已知A~F 是初中化学常见的物质,其中C、E、F为单质,A、B、D为氧化物,E是红色固体,F是目前年产量最高的金属,它们之间有如图所示的反应和转化关系。(图中“—”表示两种物质能反应,“→” 表示转化关系)

(1)写出物质F的化学式:_____ ;
(2)写出物质B的一种用途:_____ ;
(3)写出 C与 E反应的化学方程式:_____ ;
(4)F→E反应的基本类型是:_____ 。

(1)写出物质F的化学式:
(2)写出物质B的一种用途:
(3)写出 C与 E反应的化学方程式:
(4)F→E反应的基本类型是:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】氯化铜晶体 是重要的化工原料,可用作催化剂、消毒剂等。某工厂用含少量铁的氧化铜制取氯化铜晶体
是重要的化工原料,可用作催化剂、消毒剂等。某工厂用含少量铁的氧化铜制取氯化铜晶体 ,工艺流程及有关金属阳离子形成氢氧化物时溶液的pH如下。
,工艺流程及有关金属阳离子形成氢氧化物时溶液的pH如下。
(1)“酸浸”后所得溶液中主要含有的阳离子共有______ 种。
(2)“氧化”步骤中,常用的氧化剂A是过氧化氢溶液,过氧化氢及过量的盐酸将 转化为
转化为 ,该反应的化学方程式为
,该反应的化学方程式为______ 。
(3)“沉淀”步骤中,加入试剂B调节溶液的pH,为提高产品纯度并减少原料损耗,应将溶液pH范围控制在______ 。
(4)“结晶”:从滤液中得到晶体的步骤为加热浓缩→降温结晶→______ →洗涤→低温烘干。
 是重要的化工原料,可用作催化剂、消毒剂等。某工厂用含少量铁的氧化铜制取氯化铜晶体
是重要的化工原料,可用作催化剂、消毒剂等。某工厂用含少量铁的氧化铜制取氯化铜晶体 ,工艺流程及有关金属阳离子形成氢氧化物时溶液的pH如下。
,工艺流程及有关金属阳离子形成氢氧化物时溶液的pH如下。
| 氢氧化物 |  |  |
| 开始形成沉淀时的pH | 1.9 | 5.4 |
| 完全形成沉淀时的pH | 3.2 | 5.9 |
(1)“酸浸”后所得溶液中主要含有的阳离子共有
(2)“氧化”步骤中,常用的氧化剂A是过氧化氢溶液,过氧化氢及过量的盐酸将
 转化为
转化为 ,该反应的化学方程式为
,该反应的化学方程式为(3)“沉淀”步骤中,加入试剂B调节溶液的pH,为提高产品纯度并减少原料损耗,应将溶液pH范围控制在
(4)“结晶”:从滤液中得到晶体的步骤为加热浓缩→降温结晶→
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】粮食生产需要科学施肥。某化肥 样品中可能混入了
样品中可能混入了 、
、 、
、 三种物质中的一种或几种,现按如图所示进行实验探究,出现的现象如图中所述。(假设过程中发生的所有反应都恰好完全反应)
三种物质中的一种或几种,现按如图所示进行实验探究,出现的现象如图中所述。(假设过程中发生的所有反应都恰好完全反应)
(1)气体A为__________ 。滤液C中一定含有的金属阳离子是__________ 。
(2)实验过程Ⅱ中发生反应的化学方程式为______________________________ 。
(3)化肥样品中,肯定混入了上述三种物质中的______________________________ (写化学式)。
 样品中可能混入了
样品中可能混入了 、
、 、
、 三种物质中的一种或几种,现按如图所示进行实验探究,出现的现象如图中所述。(假设过程中发生的所有反应都恰好完全反应)
三种物质中的一种或几种,现按如图所示进行实验探究,出现的现象如图中所述。(假设过程中发生的所有反应都恰好完全反应)
(1)气体A为
(2)实验过程Ⅱ中发生反应的化学方程式为
(3)化肥样品中,肯定混入了上述三种物质中的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
【推荐1】某科学兴趣小组,用废渣(主要为CaCO3,还含有C、Fe2O3、MgO等少量杂质)去制作CaCl2,反应过程如图所示。______ 。
(2)Ⅰ过程中MgO发生反应的化学反应方程式______ ,此反应为______ 反应(填基本反应类型)。
(3)滤渣①的成分为______ (填化学式);
(4)X溶液为______ (填化学式);
(5)NaCl在生活中的用处:______ (写一例)。
(6)已知CaCl2与焦炭、BaSO4在高温下生成BaCl2和CO和CaS,写出该反应的方程式:______ 。

(2)Ⅰ过程中MgO发生反应的化学反应方程式
(3)滤渣①的成分为
(4)X溶液为
(5)NaCl在生活中的用处:
(6)已知CaCl2与焦炭、BaSO4在高温下生成BaCl2和CO和CaS,写出该反应的方程式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】锶元素(元素符号为Sr)及其所形成的化合物,在材料生产、油漆加工等领域中具有极其重要的用途。氢氧化锶是一种无色结晶或白色粉末,易潮解,在空气中易吸收二氧化碳生成碳酸盐。下表是部分物质的溶解性表。请利用此表回答下列问题。
(1)上述阴、阳离子形成不溶性碱的化学式为_____ ;
(2)运用此溶解性表可知, 溶液中含有的离子有
溶液中含有的离子有_____ (写离子符号);结合你对复分解反应发生条件的理解,稀盐酸能和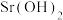 发生复分解反应,该反应发生的实质是
发生复分解反应,该反应发生的实质是_____ ;
(3)从上表中选出两种物质,写出一个有 生成的复分解反应,该反应的化学方程式为
生成的复分解反应,该反应的化学方程式为_____ (任写一个)。
| 阴离子阳离子 |  |  |  |  |
 | 溶 | 溶 | 溶 | 溶 |
 | 溶 | 溶 | 不溶 | 不溶 |
 | 不溶 | 溶 | ﹣ | 溶 |
 | 溶 | 溶 | 溶 | 不溶 |
(2)运用此溶解性表可知,
 溶液中含有的离子有
溶液中含有的离子有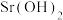 发生复分解反应,该反应发生的实质是
发生复分解反应,该反应发生的实质是(3)从上表中选出两种物质,写出一个有
 生成的复分解反应,该反应的化学方程式为
生成的复分解反应,该反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐3】海水是地球宝贵的资源,从海水中提前金属镁的主要过程如下图所示。

(1)步骤②属于________________ 反应(填基本反应类型)。
(2)操作①的名称是__________ ,该过程得到的液体依然浑浊的原因可能是______________ (写一条即可):操作③中需要用到玻璃棒,其作用是___________________ 。
(3)写出步骤④发生反应的化学方程式___________________________ 。
(4)该流程副产物氯化钙的一种用途_____________________________ 。

(1)步骤②属于
(2)操作①的名称是
(3)写出步骤④发生反应的化学方程式
(4)该流程副产物氯化钙的一种用途
您最近一年使用:0次




