海洋是巨大的资源宝库,人类应合理开发利用并予以保护。
(1)海水淡化。蒸馏法淡化海水是利用海水中各成分________ 不同进行分离的。
(2)海水晒盐。晒盐时,采用结晶的方法是_____ ;海水晒盐后得到的卤水是氯化钠的_____ (填“饱和”或“不饱和”)溶液。
(3)海水制镁。从海水中提取单质镁的工艺流程如下图所示:

①用卤水制镁的过程中发生中和反应的化学方程式是______ 。
②海水或卤水中本来就含有氯化镁,还需要过程①②的原因是______ 。
(4)海水制“碱”。下图为部分工业制碱的工艺流程,请结合图示回答。

①由氯化钠制取纯碱,从元素守恒的角度分析,还需要含有_____ 元素的物质参加反应;从酸碱反应的角度分析:先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通入二氧化碳的原因为____ 。
②在盐水(含MgCl2、CaCl2杂质)精制过程中,先后加入过量的NaOH溶液和Na2CO3溶液产生的沉淀是____ 。
③写出碳酸氢钠受热分解的反应方程式_______ 。
(1)海水淡化。蒸馏法淡化海水是利用海水中各成分
(2)海水晒盐。晒盐时,采用结晶的方法是
(3)海水制镁。从海水中提取单质镁的工艺流程如下图所示:

①用卤水制镁的过程中发生中和反应的化学方程式是
②海水或卤水中本来就含有氯化镁,还需要过程①②的原因是
(4)海水制“碱”。下图为部分工业制碱的工艺流程,请结合图示回答。

①由氯化钠制取纯碱,从元素守恒的角度分析,还需要含有
②在盐水(含MgCl2、CaCl2杂质)精制过程中,先后加入过量的NaOH溶液和Na2CO3溶液产生的沉淀是
③写出碳酸氢钠受热分解的反应方程式
更新时间:2024-02-05 14:31:16
|
相似题推荐
【推荐1】随着人类对能源的需求量日益增长,可燃冰的开采、氢气的开发和利用都越来越受到人们的关注。我国在可燃冰的试开采方面已取得重大突破,形成了国际领先的新型试采工艺。
(1)可燃冰主要含甲烷水合物,请写出甲烷(CH4)完全燃烧的化学方程式:___________ 。
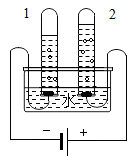
(2)电解水可产生氢气,如图中产生氢气的试管是___________ (填“1”或“2”)。

(1)可燃冰主要含甲烷水合物,请写出甲烷(CH4)完全燃烧的化学方程式:
(2)电解水可产生氢气,如图中产生氢气的试管是
您最近一年使用:0次
【推荐2】江西物产丰富,闻名天下。请用所学知识回答下列问题:
(1)景德镇瓷器文化名扬天下,氮化硅(Si3N4)陶瓷是一种新型材料,氮化硅中硅元素显+4价,则氮元素的化合价为___________ 。
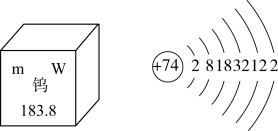
(2)赣州被誉为“世界钨都”。钨在元素周期表中的信息以及原子结构示意图如图所示。m的数值为___________ ,钨在元素周期表中位于第___________ 周期。
(3)新余有“中国新能源之都”的美称。开发新能源可以缓解能源缺乏和环境污染问题,目前正在开发和利用的新能源除太阳能外,还有___________ (写一种即可)。现提倡使用以锂空气电池作为动力的新能源电动汽车,锂空气电池放电时锂(Li)与水、空气中的氧气反应生成氢氧化锂(LiOH)。该反应的化学方程式为___________ 。
(1)景德镇瓷器文化名扬天下,氮化硅(Si3N4)陶瓷是一种新型材料,氮化硅中硅元素显+4价,则氮元素的化合价为
(2)赣州被誉为“世界钨都”。钨在元素周期表中的信息以及原子结构示意图如图所示。m的数值为

(3)新余有“中国新能源之都”的美称。开发新能源可以缓解能源缺乏和环境污染问题,目前正在开发和利用的新能源除太阳能外,还有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】海洋是巨大的资源宝库,人类应合理开发并加以保护。
(1)人类正运用各种方法开采、提取多种海洋资源,下列有关说法错误的是_______ (填序号)
A 海底蕴藏的“可燃冰”被誉为“21世纪能源”
B 利用海水涨落推动水轮机转动,从而可以发电
C 海水淡化、“晒盐”、“制碱”、“提镁”过程中,均主要涉及化学变化
D 建立海洋自然保护区,加强海洋环境监测,提高消除污染的技术水平等是保护海洋的必要措施
(2)海水晒盐得到的粗盐,常含泥沙等难溶性杂质和Ca2+、Mg2+、 等可溶性杂质离子,下列有关粗盐提纯的叙述中,错误的是
等可溶性杂质离子,下列有关粗盐提纯的叙述中,错误的是_______ (填序号)
A 除去食盐水中的可溶性杂质,可采用化学方法
B 除去食盐水中可溶性杂质的化学原理为:使杂质离子以沉淀或气体的形式从食盐中分离出来
C 除去食盐中难溶性杂质的方法,属于化学方法
D 粗盐提纯过程中,既有化学方法,又有物理方法
(3)如图是A、B两种固体物质的溶解度曲线:

①将t2℃时A物质的50g饱和溶液蒸干,理论上可以得到A物质_______ g;
②将t1℃时两种物质的饱和溶液同时升温到t2℃,所得溶液的溶质质量分数:A%_______ B%。(填“>”“=”“<”之一);
③若将B物质的不饱和溶液变为饱和溶液,下列有关说法正确的是_______ (填序号)。
A 溶质的质量一定变大
B 溶剂的质量一定变小
C 溶质的质量分数可能不变
D 溶液的温度一定升高
(1)人类正运用各种方法开采、提取多种海洋资源,下列有关说法错误的是
A 海底蕴藏的“可燃冰”被誉为“21世纪能源”
B 利用海水涨落推动水轮机转动,从而可以发电
C 海水淡化、“晒盐”、“制碱”、“提镁”过程中,均主要涉及化学变化
D 建立海洋自然保护区,加强海洋环境监测,提高消除污染的技术水平等是保护海洋的必要措施
(2)海水晒盐得到的粗盐,常含泥沙等难溶性杂质和Ca2+、Mg2+、
 等可溶性杂质离子,下列有关粗盐提纯的叙述中,错误的是
等可溶性杂质离子,下列有关粗盐提纯的叙述中,错误的是A 除去食盐水中的可溶性杂质,可采用化学方法
B 除去食盐水中可溶性杂质的化学原理为:使杂质离子以沉淀或气体的形式从食盐中分离出来
C 除去食盐中难溶性杂质的方法,属于化学方法
D 粗盐提纯过程中,既有化学方法,又有物理方法
(3)如图是A、B两种固体物质的溶解度曲线:

①将t2℃时A物质的50g饱和溶液蒸干,理论上可以得到A物质
②将t1℃时两种物质的饱和溶液同时升温到t2℃,所得溶液的溶质质量分数:A%
③若将B物质的不饱和溶液变为饱和溶液,下列有关说法正确的是
A 溶质的质量一定变大
B 溶剂的质量一定变小
C 溶质的质量分数可能不变
D 溶液的温度一定升高
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】根据如图甲、乙、丙三幅元素含量示意图,试推测元素分布领域(填图下序号):分布在人体中的是________ ;分布在海水中的是________ ;分布在地壳中的是________ .


您最近一年使用:0次
【推荐3】海洋是巨大的资源宝库,为人类提供了宝贵的自然资源。
(1)海水中含量最多的阴离子是_____ (写离子符号)。
(2)我国化学科学家侯德榜创立的“侯氏制碱法”,就是以海水“晒盐”得到的氯化钠为原料,同时制得Na2CO3
和NH4Cl产品。Na2CO3和NH4Cl的溶解度曲线如图所示。回答下列问题:
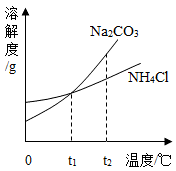
①t2℃时,NH4Cl饱和溶液的溶质质量分数_______ Na2CO3饱和溶液的溶质质量分数(填“大于”、“小于”、“等于”之一)。
②若使溶液由不饱和溶液转化为饱和溶液,可以采用的方法是_______________ 。(写一种即可)
③t1℃时一小试管内盛有的Na2CO3饱和溶液,试管底部还存有少许Na2CO3固体,将小试管放入盛有水的烧杯内,向烧杯内的水中加入一种固体物质X,发现小试管内的固体物质逐渐溶解,根据所学知识推断所加物质X可能是______ (填化学式),小试管内固体物质逐渐溶解的原因是 _______________________________ 。
(1)海水中含量最多的阴离子是
(2)我国化学科学家侯德榜创立的“侯氏制碱法”,就是以海水“晒盐”得到的氯化钠为原料,同时制得Na2CO3
和NH4Cl产品。Na2CO3和NH4Cl的溶解度曲线如图所示。回答下列问题:

①t2℃时,NH4Cl饱和溶液的溶质质量分数
②若使溶液由不饱和溶液转化为饱和溶液,可以采用的方法是
③t1℃时一小试管内盛有的Na2CO3饱和溶液,试管底部还存有少许Na2CO3固体,将小试管放入盛有水的烧杯内,向烧杯内的水中加入一种固体物质X,发现小试管内的固体物质逐渐溶解,根据所学知识推断所加物质X可能是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】海洋化学资源的利用体现了人类利用和改造物质的智慧。
(1)下列方法中能淡化海水的是______(填字母)。
(2)从海水中制备纯碱和金属镁的流程如图所示:

①流程Ⅰ海水晒盐得到粗盐的方法为_____ (填“蒸发结晶”或“降温结晶”)。
②提取氯化镁历经Ⅱ、Ⅲ两步转换的目的是______ ;写出流程Ⅳ反应的化学方程式_____ ,该反应属于_____ 反应(填反应类型)。
(1)下列方法中能淡化海水的是______(填字母)。
| A.过滤法 | B.分解法 | C.多级闪急蒸馏法 | D.膜法 |
(2)从海水中制备纯碱和金属镁的流程如图所示:

①流程Ⅰ海水晒盐得到粗盐的方法为
②提取氯化镁历经Ⅱ、Ⅲ两步转换的目的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】2014年第二十二届“世界水日”的主题是“水与能源”.海洋是巨大的资源宝库,从化学的视角看:
(1)金属资源:海水中含量最高的金属元素是_____ (填元素符号);工业上,用电解熔融状态下氯化钠的方法可得到金属钠和氯气;该反应的化学方程式为:________________ ,反应类型为_____ .
(2)淡水资源:淡化海水可以用_____ (填字母代号);
A 吸附法 B 蒸馏法 C 过滤法 D 电解法
该过程是_____ (填“化学变化”或“物理变化”)
(3)矿产资源:海底蕴藏着大量的“可燃冰”(主要成分为甲烷),甲焼燃烧的化学反应方程式为:_____ .
(4)氢能源:以水为原料,在太阳光照射和催化剂条件下分解产生氢气和氧气.该反应的化学方程式为:_____ .
(1)金属资源:海水中含量最高的金属元素是
(2)淡水资源:淡化海水可以用
A 吸附法 B 蒸馏法 C 过滤法 D 电解法
该过程是
(3)矿产资源:海底蕴藏着大量的“可燃冰”(主要成分为甲烷),甲焼燃烧的化学反应方程式为:
(4)氢能源:以水为原料,在太阳光照射和催化剂条件下分解产生氢气和氧气.该反应的化学方程式为:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】下图为海水吸收CO2并进行碳循环的原理示意图。回答下列问题:

(1)“光合”作用中太阳能转化为_________ 。
(2)写出“钙化”中发生的两个反应的化学方程式:a.__________ ; b.__________ 。
(3)此循环过程中吸收的CO2与“钙化”中释放的CO2的质量关系是_________________ (填“大于”、“小于”或“等于”)。
(4)此碳循环中将CO2转化为(CH2O)x属于_______ (填“无机物”或“有机物”),同时生成的一种无机物是_______ 。此碳循环过程的优点是_______ (写出一点即可)。
(5)工业上从海水中可提取许多广泛应用于生活、生产、科技等方面的物质和原料。
Ⅰ.从海水中获得淡水。下列方法常用于海水淡化的是_________ (填字母)。
A.蒸馏法 B.吸附法 C.沉淀法 D.过滤法
Ⅱ.从海水中提取溴(Br2)。工业上通常是将氯气通入海水晒盐后的母液中,将溶液中的溴化钠(NaBr)转化为溴单质(Br2),然后鼓入热空气,使溴单质(Br2)从溶液中挥发出来,冷凝后得到粗溴。其中主要反应的化学方程式为______ ,其基本反应类型是________ 。

(1)“光合”作用中太阳能转化为
(2)写出“钙化”中发生的两个反应的化学方程式:a.
(3)此循环过程中吸收的CO2与“钙化”中释放的CO2的质量关系是
(4)此碳循环中将CO2转化为(CH2O)x属于
(5)工业上从海水中可提取许多广泛应用于生活、生产、科技等方面的物质和原料。
Ⅰ.从海水中获得淡水。下列方法常用于海水淡化的是
A.蒸馏法 B.吸附法 C.沉淀法 D.过滤法
Ⅱ.从海水中提取溴(Br2)。工业上通常是将氯气通入海水晒盐后的母液中,将溶液中的溴化钠(NaBr)转化为溴单质(Br2),然后鼓入热空气,使溴单质(Br2)从溶液中挥发出来,冷凝后得到粗溴。其中主要反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】2021年6月8日是第13个“世界海洋日”。烟台有漫长的海岸线,蕴藏着丰富的海洋资源。某兴趣小组设计的综合利用海水的部分流程图如图。据如图回答:

(1)海水制镁:步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式为___________ 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是___________ 。
(2)海水晒盐:
①利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是___________ (填字母序号)。
A.在蒸发池中水蒸发所需能量主要为太阳能和风能
B.在结晶池中主要通过降温结晶使氯化钠析出
C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液
②粗盐中常含有泥沙等难溶性杂质。在实验室中除去粗盐中的难溶性杂质,可依次通过___________ 、过滤、蒸发结晶等操作。蒸发结晶操作中要用到玻璃棒,其作用是___________ 。通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是___________ 。
(3)海水制碱:步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向NaCl饱和溶液中先后加入的两种物质分别是___________ (写化学式)。步骤⑨中发生反应的化学方程式是___________ 。
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是___________ 。
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是___________ 。

(1)海水制镁:步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式为
(2)海水晒盐:
①利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是
A.在蒸发池中水蒸发所需能量主要为太阳能和风能
B.在结晶池中主要通过降温结晶使氯化钠析出
C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液
②粗盐中常含有泥沙等难溶性杂质。在实验室中除去粗盐中的难溶性杂质,可依次通过
(3)海水制碱:步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向NaCl饱和溶液中先后加入的两种物质分别是
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海水是一种重要的自然资源,以下是对海水资源的部分利用,回答有关问题。
(1)从海水中得到金属镁——下图是从海水中提取镁的简单流程。由无水MgCl2制取Mg的化学方程式为__________________ 。

(2)海水“制碱”——下图是海水“制碱”的部分简单流程。

①步骤Ⅲ反应的化学方程式为:_______________________ 。
②制氨盐水的过程中要先通入氨气,再通入二氧化碳。如果反过来,二氧化碳的吸收率会降低。这是因为_____________________________ 。
(1)从海水中得到金属镁——下图是从海水中提取镁的简单流程。由无水MgCl2制取Mg的化学方程式为

(2)海水“制碱”——下图是海水“制碱”的部分简单流程。

①步骤Ⅲ反应的化学方程式为:
②制氨盐水的过程中要先通入氨气,再通入二氧化碳。如果反过来,二氧化碳的吸收率会降低。这是因为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】海水含有丰富资源,向海发展、向海图强是未来的发展趋势。
(1)海水淡化

如图是“膜分离技术”淡化海水的原理图。该技术采用对海水加压,海水中的水分子可以通过半透膜,而其他微观粒子很难透过。采用膜分离技术淡化海水的原理,与化学实验中常见的______ 操作相似。半透膜上方的海水加压后,海水中溶质的质量分数会______ (填“增大”、“减小”或“不变”)。
(2)海水晒盐

20℃海水中主要盐类及其溶质的质量分数
①晒盐时不能将水全部蒸干,目的是使卤水中的NaCl大量析出,而其他盐类基本不析出,请结合两幅图分析其他盐类不析出的原因______ 。
②用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl,则“花水”应当是______ (填序号)。
A.蒸馏水 B.饱和NaCl溶液
C.饱和NaOH溶液 D.饱和BaCl2溶液
(3)海水制镁
海水还可制备金属镁,主要物质转化关系如图所示:
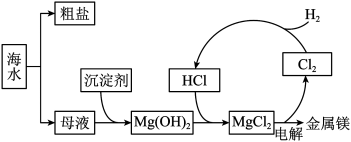
①我国有丰富的石灰石资源,实际生产中,从经济角度考虑常选用______ 作为沉淀剂。
②电解熔融MgCl2制备金属镁时需要保护气的原因是______ 。
(4)海水制“碱”

①粗盐净化成精盐水的过程中需要除去MgCl2、Na2SO4、CaCl2等杂质,若用化学沉淀法依次除去这三种物质,可采用的方法是______ (用化学方程式表示,只写一个反应即可)。
②步骤Ⅱ发生的反应是NH3+CO2+NaCl+H2O=NaHCO3↓+NH4Cl,下列叙述正确的是______ (填字母代号)。
A.该条件下NaHCO3的溶解度比NH4Cl的大
B.配制饱和氯化钠溶液时,可通过搅拌来提高食盐的溶解度
C.向饱和氯化钠溶液中先通氨气的作用是使溶液呈碱性,促进二氧化碳的吸收
D.析出晶体后剩余溶液中溶质只有NH4Cl
③根据步骤III可推测碳酸氢钠具有______ 化学性质。
(1)海水淡化

如图是“膜分离技术”淡化海水的原理图。该技术采用对海水加压,海水中的水分子可以通过半透膜,而其他微观粒子很难透过。采用膜分离技术淡化海水的原理,与化学实验中常见的
(2)海水晒盐

20℃海水中主要盐类及其溶质的质量分数
盐类 | 质量分数 |
NaCl | 2.72% |
MgCl2 | 0.38% |
MgSO4 | 0.17% |
②用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl,则“花水”应当是
A.蒸馏水 B.饱和NaCl溶液
C.饱和NaOH溶液 D.饱和BaCl2溶液
(3)海水制镁
海水还可制备金属镁,主要物质转化关系如图所示:

①我国有丰富的石灰石资源,实际生产中,从经济角度考虑常选用
②电解熔融MgCl2制备金属镁时需要保护气的原因是
(4)海水制“碱”

①粗盐净化成精盐水的过程中需要除去MgCl2、Na2SO4、CaCl2等杂质,若用化学沉淀法依次除去这三种物质,可采用的方法是
②步骤Ⅱ发生的反应是NH3+CO2+NaCl+H2O=NaHCO3↓+NH4Cl,下列叙述正确的是
A.该条件下NaHCO3的溶解度比NH4Cl的大
B.配制饱和氯化钠溶液时,可通过搅拌来提高食盐的溶解度
C.向饱和氯化钠溶液中先通氨气的作用是使溶液呈碱性,促进二氧化碳的吸收
D.析出晶体后剩余溶液中溶质只有NH4Cl
③根据步骤III可推测碳酸氢钠具有
您最近一年使用:0次



