从废旧电脑的某些零部件中回收金属银,设计流程如图所示:
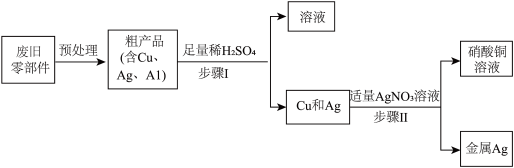
(1)废旧零部件预处理过程中需要将其粉碎,粉碎的目的是___ 。
(2)步骤Ⅰ和步骤Ⅱ都涉及的实验操作是____ 。
(3)步骤Ⅰ中加入足量稀硫酸后发生反应的现象______ ;该反应基本类型为_____ ;步骤中加入适量AgNO3溶液后发生反应的化学方程式为__________ 。

(1)废旧零部件预处理过程中需要将其粉碎,粉碎的目的是
(2)步骤Ⅰ和步骤Ⅱ都涉及的实验操作是
(3)步骤Ⅰ中加入足量稀硫酸后发生反应的现象
更新时间:2024-02-26 23:04:04
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】“宏观-微观-符号”三重表征是化学独特的表示物质及其变化的方法。请结合下图所示的氢氧化钾溶液和稀硫酸反应的微观示意图,回答下列问题:

(1)写出氢氧化钾溶液和稀硫酸反应的化学方程式:________ 。
(2)写出图中C方框内甲、乙两种粒子的符号:甲_______ 、乙_______ 。
(3)下列物质中只有一种能与KOH溶液发生上述类似反应,它是______ (填序号)。
①HCl ②CaCl2③CuCl2

(1)写出氢氧化钾溶液和稀硫酸反应的化学方程式:
(2)写出图中C方框内甲、乙两种粒子的符号:甲
(3)下列物质中只有一种能与KOH溶液发生上述类似反应,它是
①HCl ②CaCl2③CuCl2
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组为探究一氧化碳的还原性,设计了如图所示的实验装置。

(1)请解释先通CO,再加热CuO的原因。
(2)写出横放玻璃管内反应的化学方程式。
(3)该装置有缺陷,指出改正的方法。

(1)请解释先通CO,再加热CuO的原因。
(2)写出横放玻璃管内反应的化学方程式。
(3)该装置有缺陷,指出改正的方法。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】铝土矿的主要成分是氧化铝(所含杂质不参与反应,也难溶于水),工业上用铝土矿制取金属铝的过程如下图所示,请你回答以下问题:

(1)步骤1中发生如下反应:Al2O3+2NaOH═2NaAlO2+X,X的化学式是__ .
(2)操作1和操作2中均用到玻璃棒,其作用是__ ,滤液2的PH为10显__ 性(填“酸或碱”).
(3)步骤2得到的氢氧化铝可以用于治疗胃酸过多,该反应属于__ 反应(填“化合、分解、复分解”).
(4)步骤3中发生了分解反应,除了生成氧化铝,还有一种氧化物生成.请写出该反应的化学方程式__ .

(1)步骤1中发生如下反应:Al2O3+2NaOH═2NaAlO2+X,X的化学式是
(2)操作1和操作2中均用到玻璃棒,其作用是
(3)步骤2得到的氢氧化铝可以用于治疗胃酸过多,该反应属于
(4)步骤3中发生了分解反应,除了生成氧化铝,还有一种氧化物生成.请写出该反应的化学方程式
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】置换反应是化学反应的基本类型之一。
(1)金属与盐溶液之间的置换反应,一般是活动性较强的金属可把活动性较弱的金属从其盐溶液中置换出来。如铜和硝酸银溶液的化学方程式为____________________ 。
(2)非金属单质也具有类似金属与盐溶液之间的置换反应的规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,如在溶液中可发生下列反应:
Cl2+2NaBr==2NaCl + Br2,I2 + Na2S==2NaI + S↓,Br2 + 2KI==2KBr + I2
由此可判断:
①S、Cl2、I2、Br2非金属活动性由强到弱顺序是__________________ 。
②下列化学方程式书写错误的是___________ 。
A Cl2 + 2NaI===2NaCl + I2 B I2+2KBr===2KI + Br2
C Br2 + Na2S===2NaBr + S↓ D Cl2 + K2S===2KCl + S↓
(1)金属与盐溶液之间的置换反应,一般是活动性较强的金属可把活动性较弱的金属从其盐溶液中置换出来。如铜和硝酸银溶液的化学方程式为
(2)非金属单质也具有类似金属与盐溶液之间的置换反应的规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,如在溶液中可发生下列反应:
Cl2+2NaBr==2NaCl + Br2,I2 + Na2S==2NaI + S↓,Br2 + 2KI==2KBr + I2
由此可判断:
①S、Cl2、I2、Br2非金属活动性由强到弱顺序是
②下列化学方程式书写错误的是
A Cl2 + 2NaI===2NaCl + I2 B I2+2KBr===2KI + Br2
C Br2 + Na2S===2NaBr + S↓ D Cl2 + K2S===2KCl + S↓
您最近一年使用:0次
【推荐2】根据图示实验回答下列问题。________ ;该操作中用玻璃棒搅拌的目的是________ ;停止加热的最佳时机是________ 。
(2)乙是探究金属性质的实验。将金属X插入烧杯内的 溶液中,观察到溶液颜色变蓝,金属X是
溶液中,观察到溶液颜色变蓝,金属X是________ 。后取出X,向烧杯内再加入一定量锌粉,振荡后,溶液蓝色逐渐消失。实验结束后,烧杯内的溶液中一定________ (选填“存在”或“不存在”) 。
。

(2)乙是探究金属性质的实验。将金属X插入烧杯内的
 溶液中,观察到溶液颜色变蓝,金属X是
溶液中,观察到溶液颜色变蓝,金属X是 。
。
您最近一年使用:0次
【推荐3】跨学科研究小组制定了以“水和溶液”为主题的研究项目。
(1)水质净化。自制简易净水器可以选择去底倒置的可乐瓶作为容器,现提供四种材料。

其中④号材料的作用是______ 。容器中 a、b 处应放置的材料(材料间用纱布隔开)最合理的顺序为______ (选填“①②”或“②①”)。
(2)配制溶液。20℃时,取一包硫酸铜粉末(密封包装)加入 100g 水中,充分溶解后发现有固体剩余。
①此时该溶液为______ (填“饱和”或“不饱和”)溶液。
②若采用加热方法(忽略水蒸发)使剩余固体完全溶解后,溶液的溶质质量分数将______ (填“变大”“变小”或“不变”)。
③已知:20℃时,硫酸铜的溶解度为 20.5 g。若再加入 100g 水可使剩余固体完全溶解(忽略温度变化),可推测该包硫酸铜粉末质量 m 的取值范围是______ 。
④不宜在铁制容器中配制硫酸铜溶液的原因是______ (用化学方程式表示)。
(1)水质净化。自制简易净水器可以选择去底倒置的可乐瓶作为容器,现提供四种材料。

其中④号材料的作用是
(2)配制溶液。20℃时,取一包硫酸铜粉末(密封包装)加入 100g 水中,充分溶解后发现有固体剩余。
①此时该溶液为
②若采用加热方法(忽略水蒸发)使剩余固体完全溶解后,溶液的溶质质量分数将
③已知:20℃时,硫酸铜的溶解度为 20.5 g。若再加入 100g 水可使剩余固体完全溶解(忽略温度变化),可推测该包硫酸铜粉末质量 m 的取值范围是
④不宜在铁制容器中配制硫酸铜溶液的原因是
您最近一年使用:0次
【推荐1】溶液在许多方面起着十分重要的作用。请回答下列问题:
(1)硝酸钾和氯化钾的溶解度曲线如图所示。

①t1℃时,硝酸钾的饱和溶液中溶质和溶剂的质量比为___________ 。
②t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有50g水的两个烧杯中,充分搅拌后现象如图所示。

烧杯乙中的溶质是_________ (填名称)。将上图中两烧杯内的物质温度升高到t2℃(不考虑水的蒸发),充分搅拌后两烧杯内所得溶液中溶质的质量分数__________ 。
A烧杯甲中的大
B烧杯乙中的大
C一样大
D无法确定大小关系
③要从硝酸钾与氯化钾(少量)的固体混合物中获得硝酸钾,实验操作是:用适量热水溶解→得到热饱和溶液→___________ →过滤→洗涤→干燥。
(2)井水常含有较多的Ca(HCO3)2、Mg(HCO3)2等可溶物,属于硬水。
①取等量的井水和蒸馏水,向其中滴入__________ ,振荡后可根据现象,区分井水和蒸馏水。
②煮沸能降低井水的硬度,因为上述可溶物转化成了CaCO3和Mg(OH)2,即水垢。用稀盐酸洗涤水垢,有气体产生,写出产生气体的反应的化学方程式___________ 。
(3)取5.0g附着了水垢的铝质旧水壶碎片,与足量的稀盐酸充分反应,得到氢气0.4g,求该碎片中单质铝的质量分数。(写出计算过程)____________ 。
(1)硝酸钾和氯化钾的溶解度曲线如图所示。

①t1℃时,硝酸钾的饱和溶液中溶质和溶剂的质量比为
②t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有50g水的两个烧杯中,充分搅拌后现象如图所示。

烧杯乙中的溶质是
A烧杯甲中的大
B烧杯乙中的大
C一样大
D无法确定大小关系
③要从硝酸钾与氯化钾(少量)的固体混合物中获得硝酸钾,实验操作是:用适量热水溶解→得到热饱和溶液→
(2)井水常含有较多的Ca(HCO3)2、Mg(HCO3)2等可溶物,属于硬水。
①取等量的井水和蒸馏水,向其中滴入
②煮沸能降低井水的硬度,因为上述可溶物转化成了CaCO3和Mg(OH)2,即水垢。用稀盐酸洗涤水垢,有气体产生,写出产生气体的反应的化学方程式
(3)取5.0g附着了水垢的铝质旧水壶碎片,与足量的稀盐酸充分反应,得到氢气0.4g,求该碎片中单质铝的质量分数。(写出计算过程)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】国产航母“山东舰”威武入列,标志我国金属材料制造技术取得重大突破。
(1)钛合金可用于制作舰载机的起落架,构成金属钛的微粒是___________ (填“分子”“原子”或“离子”),下图是以钛酸亚铁(FeTiO3)为原料制取钛(Ti)的部分流程示意图:
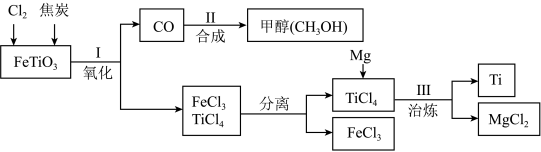
过程Ⅱ使用CO和H2化合生成甲醇(CH3OH)时,为了使CO和H2恰好完全反应,应调节原料中CO和H2的分子个数比是___________ 。
(2)金属防锈常用电镀的方法,电镀防锈的原理是___________ 。
(3)某电镀厂的废液中含有硝酸银和硝酸铜,兴趣小组的同学在实验室探究回收该废液中的金属。将一定量铁粉加入到盛有一定量废液样品的烧杯中,充分反应后过滤,得到滤渣A和滤液B.向滤渣A中加入少量稀盐酸,有气泡产生,据此分析,滤液B中含有的溶质是___________ (填化学式),写出向废液中加入铁粉的一个化学反应的化学方程式___________ 。
(1)钛合金可用于制作舰载机的起落架,构成金属钛的微粒是

过程Ⅱ使用CO和H2化合生成甲醇(CH3OH)时,为了使CO和H2恰好完全反应,应调节原料中CO和H2的分子个数比是
(2)金属防锈常用电镀的方法,电镀防锈的原理是
(3)某电镀厂的废液中含有硝酸银和硝酸铜,兴趣小组的同学在实验室探究回收该废液中的金属。将一定量铁粉加入到盛有一定量废液样品的烧杯中,充分反应后过滤,得到滤渣A和滤液B.向滤渣A中加入少量稀盐酸,有气泡产生,据此分析,滤液B中含有的溶质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】活性氧化锌是重要的工业添加剂。某工厂利用硫酸与氧化铜锌矿(主要成分是ZnO、CuO,还含有少量SiO2和Fe2O3等杂质)为原料制取活性氧化锌,流程如下:
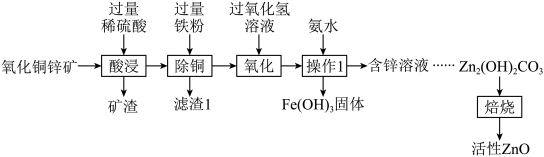
【查阅资料】过氧化氢在60°C时的分解率为50%,90~100°C时分解率达90%。
(1)为提高“酸浸”的速率,可采取的措施有___________ (写一条)。
(2)“除铜”时,加入过量铁粉反应的化学方程式为___________ (写一个)。
(3)“氧化”时,反应温度不能过高的原因是___________ 。
(4)“操作I”的名称是___________ 。
(5)氨水除用于工业生产外,还在生活、农业、医疗等领域有广泛用途,请试举一例___________ 。
(6) “焙烧”除得到产品外,还生成H2O和CO2,请写出该反应的化学方程式
“焙烧”除得到产品外,还生成H2O和CO2,请写出该反应的化学方程式___________ 。

【查阅资料】过氧化氢在60°C时的分解率为50%,90~100°C时分解率达90%。
(1)为提高“酸浸”的速率,可采取的措施有
(2)“除铜”时,加入过量铁粉反应的化学方程式为
(3)“氧化”时,反应温度不能过高的原因是
(4)“操作I”的名称是
(5)氨水除用于工业生产外,还在生活、农业、医疗等领域有广泛用途,请试举一例
(6)
 “焙烧”除得到产品外,还生成H2O和CO2,请写出该反应的化学方程式
“焙烧”除得到产品外,还生成H2O和CO2,请写出该反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】以下是某自来水厂生产原理的图示(假设每一步都达到目的)。请据此回答问题:
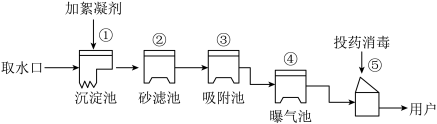
(1)其中属于化学变化的步骤是______ (填序号)。
(2)净水剂常用明矾,在此过程中明矾的作用是___________ 。
(3)经过以上处理的水,已经除去了大部分杂质,但是还有________ 等杂质。
A 悬浮的固体颗粒物 B 有颜色和有气味的物质
C 可溶性的物质 D 细菌和病毒
(4)实验室过滤操作中需要用到的玻璃仪器有玻璃棒、_______ 和________ ,其中玻璃棒的作用是___________ 。

(1)其中属于化学变化的步骤是
(2)净水剂常用明矾,在此过程中明矾的作用是
(3)经过以上处理的水,已经除去了大部分杂质,但是还有
A 悬浮的固体颗粒物 B 有颜色和有气味的物质
C 可溶性的物质 D 细菌和病毒
(4)实验室过滤操作中需要用到的玻璃仪器有玻璃棒、
您最近一年使用:0次