有一瓶久藏的Na2SO3,欲测定该药品变质程度,进行如下定量分析:将试样烘干后称取mg,用适量的蒸馏水配成溶液,加入足量的BaCl2溶液使沉淀完全。滤出的沉淀经洗涤、干燥后,质量为ng。
(1)若试样部分变质,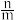 的范围为
的范围为______ 。
(2)若取试样m=10.0g,其中Na2SO3已有50%变质,则n为_______ g。
(1)若试样部分变质,
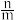 的范围为
的范围为(2)若取试样m=10.0g,其中Na2SO3已有50%变质,则n为
更新时间:2024-03-01 20:56:57
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】请在下列两小题中任选一题作答,如两小题都解答,以给出正确答案的小题评定分数。

(1)根据上图自编一道计算题并给出参考答案,含解题过程_____ 。(原来总是老师出题考我,现在我也当一回老师,并能做出参考答案。)
(2)已知标准状况下氧气的密度约为1.43g/L,16g铜粉在空气中加热至完全反应,能消耗标准状况下的氧气______ 升?(计算结果精确到0.1)

(1)根据上图自编一道计算题并给出参考答案,含解题过程
(2)已知标准状况下氧气的密度约为1.43g/L,16g铜粉在空气中加热至完全反应,能消耗标准状况下的氧气
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】为了测定某纯碱样品中碳酸钠和氯化钠的含量(其他成分可忽略),将一定量的该样品溶解在100g水中,加入足量的氯化钙溶液,反应的化学方程式为: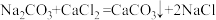 ,反应中物质间的质量关系如右图所示。当反应恰好完成时过滤,测得滤液中氯化钠的质量分数为6%。试计算该样品中:
,反应中物质间的质量关系如右图所示。当反应恰好完成时过滤,测得滤液中氯化钠的质量分数为6%。试计算该样品中:

(1)氯化钠的质量;
(2)碳酸钠的质量分数。
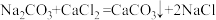 ,反应中物质间的质量关系如右图所示。当反应恰好完成时过滤,测得滤液中氯化钠的质量分数为6%。试计算该样品中:
,反应中物质间的质量关系如右图所示。当反应恰好完成时过滤,测得滤液中氯化钠的质量分数为6%。试计算该样品中: 
(1)氯化钠的质量;
(2)碳酸钠的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】我国化学家侯德榜创立的联合制碱法有提高了食盐的利用率,节约了成本等优点。现在小王同学用“侯氏联合制碱法”制得碳酸钠常含有少量氯化钠。为测定某样品中碳酸钠含量,小明称取该碳酸钠样品11g溶解于水中,加入足量氯化钙溶液,经过滤、洗涤、干燥后得沉淀质量为10g。求:该样品中碳酸钠的质量分数。(写出具体计算过程,结果精确到0.1%)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】在化学实验技能考试做完“二氧化碳的制取和性质”实验后,废液桶中有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质)。为避免污染环境并回收利用废液,化学兴趣小组做了如下实验:
取废液桶上层清液共11.88kg,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液pH与加入的碳酸钠溶液的质量关系如右图所示:

(1)通过右图可知,当碳酸钠溶液质量加到 kg时,废液恰好处理完(盐酸与氯化钙的混合溶液完全转化成氯化钠溶液)。
(2)此时所得溶液能否用于该校生物兴趣小组的小麦选种(选种液要求氯化钠的溶质质量分数在10%~20%之间)?请通过计算回答。
取废液桶上层清液共11.88kg,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液pH与加入的碳酸钠溶液的质量关系如右图所示:

(1)通过右图可知,当碳酸钠溶液质量加到 kg时,废液恰好处理完(盐酸与氯化钙的混合溶液完全转化成氯化钠溶液)。
(2)此时所得溶液能否用于该校生物兴趣小组的小麦选种(选种液要求氯化钠的溶质质量分数在10%~20%之间)?请通过计算回答。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】小明同学将13.9g含杂质氯化钠的纯碱样品与140.5g稀盐酸相混合,充分反应,测得反应生成气体的质量(m)与反应时间(t)变化的曲线如下图所示:


请计算:
(1)纯碱样品中碳酸钠的质量分数(计算结果保留一位小数);___________
(2)完全反应后所得溶液中溶质的质量分数。_________________


请计算:
(1)纯碱样品中碳酸钠的质量分数(计算结果保留一位小数);___________
(2)完全反应后所得溶液中溶质的质量分数。_________________
您最近一年使用:0次



