鸡蛋壳的主要成分是碳酸钙。为测定鸡蛋壳中CaCO3的含量,某化学社团分别进行了下图所示的实验。(假设鸡蛋壳中其他成分不溶于水,且不与稀盐酸反应)

(1)用托盘天平称取10g鸡蛋壳,称量过程中发现指针向右偏转,这时要进行的操作是______ 。
(2)当观察到烧杯中______ 时,说明反应已经结束。
(3)依据图中数据分析,鸡蛋壳中CaCO3的质量分数为______ 。
(4)计算反应过程中产生的二氧化碳的质量。(写出计算过程)
(5)若操作I中发现滤液仍然浑浊,则会导致测定的鸡蛋壳中碳酸钙的质量分数______ (填“偏大”、“偏小”或“无影响”)。

(1)用托盘天平称取10g鸡蛋壳,称量过程中发现指针向右偏转,这时要进行的操作是
(2)当观察到烧杯中
(3)依据图中数据分析,鸡蛋壳中CaCO3的质量分数为
(4)计算反应过程中产生的二氧化碳的质量。(写出计算过程)
(5)若操作I中发现滤液仍然浑浊,则会导致测定的鸡蛋壳中碳酸钙的质量分数
更新时间:2024-03-20 22:09:59
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】向16g黄铜(由锌、铜形成的合金)样品中加入稀硫酸充分反应,所加稀硫酸与生成气体的质量关系如下图所示。求:
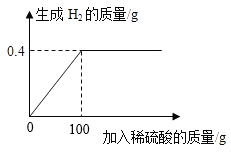
(1)硫酸中氢、硫、氧元素的质量比_____ ;
(2)样品中锌的质量。
(3)所用稀硫酸溶质的质量分数。

(1)硫酸中氢、硫、氧元素的质量比
(2)样品中锌的质量。
(3)所用稀硫酸溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某化学兴趣小组,为了测定铜锌合金样品中锌的含量,称取样品20克于烧杯中,向其中加入50克稀硫酸至恰好完全反应,反应后烧杯中物质的总质量为69.8克,求:
(1)样品中锌的质量分数 ?
(2)恰好完全反应后所得溶液中溶质的质量分数 ?
(1)样品中锌的质量分数 ?
(2)恰好完全反应后所得溶液中溶质的质量分数 ?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】为测定某纯碱样品(含少量氯化钠杂质)中碳酸钠的含量,取12g样品放入烧杯中,加入100g稀盐酸,恰好完全反应.经测定,所得溶液常温下为不饱和溶液,其质量为107.6g(产生的气体全部逸出)。试计算:
(1)12g样品中碳酸钠的质量分数.
(2)所加稀盐酸的质量分数
(1)12g样品中碳酸钠的质量分数.
(2)所加稀盐酸的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某纯碱样品中含有少量的氯化钠,某化学兴趣小组欲测定其中碳酸钠的质量分数。他们称取25.0g样品放入锥形瓶中,加入稀硫酸直到不再产生气体为止,反应中生成气体的质量与加入稀硫酸的质量关系如图所示。请计算:

(1)反应生成的二氧化碳的质量为______ g;
(2)该纯碱样品中碳酸钠的质量分数(写出计算过程,计算结果精确到0.1%)。

(1)反应生成的二氧化碳的质量为
(2)该纯碱样品中碳酸钠的质量分数(写出计算过程,计算结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】现有100g氯化铜溶液,向其中加入一定溶质质量分数的氢氧化钠溶液,实验过程中,生成沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。
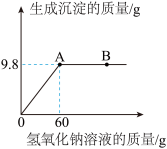
(生成沉淀原理: )
)
(1)生成沉淀的质量为_______ g。
(2)求加入NaOH溶液的溶质质量分数______ 。(写出计算过程,计算结果精确到0.1%)。

(生成沉淀原理:
 )
)(1)生成沉淀的质量为
(2)求加入NaOH溶液的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)甲同学用托盘天平称量10.2g食盐时(1g以下用游码),称后发现砝码放在左盘,食盐放在了右盘,所称食盐的实际质量是_______________ g
(2)乙学生用量筒量取液体,量筒摆放平稳,面对刻度,他先俯视读数为48mL,倾倒出部分液体后,又仰视读数为40mL,则该同学实际倒出的液体的体积是 ___________8mL (用“>” “<” “=” 填空)
(3)一个铝原子中共有40个粒子,其中14个粒子不带电,则铝原子的核电荷数是_____________,相对原子质量是_______________。
(4)假设可作确定相对原子质量标准的碳原子的质量为b克,一个X原子的质量为m克,则X的相对原子质量为______________。
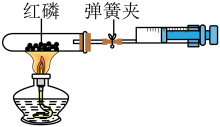
(5)某化学兴趣小组的同学,设计了用如图所示装置来“测定空气中氧气的含量”,试管的容积为50mL,注射器的活塞实验前停在25mL处,试管内红磷足量。用酒精灯加热,充分反应直至燃烧结束,试管冷却至室温,可观察到注射器的活塞最终停留的刻度是接近______________mL。
(2)乙学生用量筒量取液体,量筒摆放平稳,面对刻度,他先俯视读数为48mL,倾倒出部分液体后,又仰视读数为40mL,则该同学实际倒出的液体的体积是 ___________8mL (用“>” “<” “=” 填空)
(3)一个铝原子中共有40个粒子,其中14个粒子不带电,则铝原子的核电荷数是_____________,相对原子质量是_______________。
(4)假设可作确定相对原子质量标准的碳原子的质量为b克,一个X原子的质量为m克,则X的相对原子质量为______________。
(5)某化学兴趣小组的同学,设计了用如图所示装置来“测定空气中氧气的含量”,试管的容积为50mL,注射器的活塞实验前停在25mL处,试管内红磷足量。用酒精灯加热,充分反应直至燃烧结束,试管冷却至室温,可观察到注射器的活塞最终停留的刻度是接近______________mL。

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组同学在实验室称取7g某铝样品(杂质不溶于水也不与酸反应)放入烧杯中,逐滴加入200g一定溶质质量分数的稀硫酸,烧杯中固体的质量与加入稀硫酸的质量关系如图所示。请回答下列问题:
(铝是活泼金属,能与硫酸发生化学反应生成硫酸铝[化学式:Al2(SO4)3)]和氢气)

(1)称量样品质量时,发现托盘天平指针向左偏转,应采取的操作是______ 。
(2)计算该稀硫酸的溶质质量分数(写出计算过程,计算结果保留一位小数)。
(铝是活泼金属,能与硫酸发生化学反应生成硫酸铝[化学式:Al2(SO4)3)]和氢气)

(1)称量样品质量时,发现托盘天平指针向左偏转,应采取的操作是
(2)计算该稀硫酸的溶质质量分数(写出计算过程,计算结果保留一位小数)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】碳酸钠是一种重要的无机化工原料,主要用于平板玻璃、玻璃制品和陶瓷釉的生产。某公司新购入一批碳酸钠,化学兴趣小组同学对该批碳酸钠进行检测:称取10.7g样品于锥形瓶中,加适量水溶解,然后滴加过量的稀硫酸(装置如图所示,杂质不与稀硫酸反应),实验测得数据如表所示。请回答下列问题:
_______ 。
(2)样品在_______ s开始就完全反应完。
(3)工业碳酸钠的部分质量指标如下表,请仅从碳酸钠含量角度判断这批购入的碳酸钠的质量等级(写出计算过程)。
(4)关于本次实验的下列说法中正确的是_______(双选)。
| 时间/s | 0 |  |  |  |  |
| 装置及装置内药品的总质量/g | 215.0 | 212.8 | 210.8 | 210.6 | 210.6 |

(2)样品在
(3)工业碳酸钠的部分质量指标如下表,请仅从碳酸钠含量角度判断这批购入的碳酸钠的质量等级(写出计算过程)。
| 项目 | 指标 | |||
| Ⅰ类 | Ⅱ类 | |||
| 优等品 | 一等品 | 合格品 | ||
| 碳酸钠的含量≥ | 99.4 | 99.2 | 98.8 | 98.0 |
(4)关于本次实验的下列说法中正确的是_______(双选)。
| A.溶解碳酸钠样品时,搅拌可以加快溶解速率 |
| B.实验中可用浓盐酸代替稀硫酸 |
| C.如果没有盛氯化钙的干燥管,所测碳酸钠的含量会偏大 |
| D.实验中所用的稀硫酸必需一次性快速加入锥形瓶中 |
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某校同学探究附近赤铁矿中Fe2O3的纯度。他们采集了20g样品,加入稀盐酸,恰好完全反应,共用去稀盐酸309g,过滤得到滤渣4g。(假设杂质既不溶于水,也不溶于酸;不考虑实验中的损耗)。计算:
(1)Fe2O3在赤铁矿样品中质量分数为多少?
(2)反应后所得溶液中溶质的质量分数是多少?
(1)Fe2O3在赤铁矿样品中质量分数为多少?
(2)反应后所得溶液中溶质的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】下图为某药厂生产的“新盖中盖牌”高钙片标签上的部分文字,请仔细阅读后回答下列问题。
(1)计算碳酸钙中钙元素的质量分数。
(2)计算高钙片中碳酸钙的质量分数?(写出计算过程)
| [主要原料]碳酸钙(CaCO3)、维生素D [功效成份]补钙 每片中含钙: (以Ca计)500 mg 维生素D 100 IU [食用方法] 每日1次,每次1片 [规 格] 2.5g/片 |
(1)计算碳酸钙中钙元素的质量分数。
(2)计算高钙片中碳酸钙的质量分数?(写出计算过程)
您最近一年使用:0次




