硅及其重要化合物在现代高新技术领域应用广泛。
(1)高纯度焦炭与石英砂(SiO2)反应可制得硅:SiO2+________ C Si+
Si+________ CO↑。请完成方程式的配平。
(2)根据(1)中的方程式:现有120kg的SiO2,理论上可生产硅的质量为多少?
(1)高纯度焦炭与石英砂(SiO2)反应可制得硅:SiO2+
 Si+
Si+(2)根据(1)中的方程式:现有120kg的SiO2,理论上可生产硅的质量为多少?
更新时间:2024-04-04 11:44:16
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】甲醇( )是一种有毒、有酒味的可燃性液体。甲醇在氧气中不完全燃烧可发生如下反应:
)是一种有毒、有酒味的可燃性液体。甲醇在氧气中不完全燃烧可发生如下反应: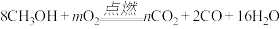 。若反应生成3.6g水,请计算:
。若反应生成3.6g水,请计算:
(1)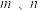 的值________。
的值________。
(2)参加反应的氧气质量是多少克__________?
 )是一种有毒、有酒味的可燃性液体。甲醇在氧气中不完全燃烧可发生如下反应:
)是一种有毒、有酒味的可燃性液体。甲醇在氧气中不完全燃烧可发生如下反应: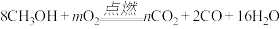 。若反应生成3.6g水,请计算:
。若反应生成3.6g水,请计算:(1)
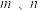 的值________。
的值________。(2)参加反应的氧气质量是多少克__________?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在含镍电镀废液的回收镍工艺中,需要除去铁元素(以Fe2+形式存在)。方法是:先将Fe2+氧化为Fe3+再沉淀除去。氧化时反应为 ,在不同温度、pH时,沉铁过程中Fe2+转化所得产物可能不同,如图所示。
,在不同温度、pH时,沉铁过程中Fe2+转化所得产物可能不同,如图所示。

(1)化学方程式中a=______ 。
(2)现有某一定量的废液,其中含 的质量为15.2g,其被过氧化氢溶液完全氧化,可得到
的质量为15.2g,其被过氧化氢溶液完全氧化,可得到 溶质的质量为多少(写出计算过程)?
溶质的质量为多少(写出计算过程)?
(3)沉铁过程中,在160°C、pH=7时,Fe3+转化为______ (填化学式)。若调节温度为30°C,pH=6,则可得到最终的含铁固体质量为______ g(假设没有损耗)。
 ,在不同温度、pH时,沉铁过程中Fe2+转化所得产物可能不同,如图所示。
,在不同温度、pH时,沉铁过程中Fe2+转化所得产物可能不同,如图所示。
(1)化学方程式中a=
(2)现有某一定量的废液,其中含
 的质量为15.2g,其被过氧化氢溶液完全氧化,可得到
的质量为15.2g,其被过氧化氢溶液完全氧化,可得到 溶质的质量为多少(写出计算过程)?
溶质的质量为多少(写出计算过程)?(3)沉铁过程中,在160°C、pH=7时,Fe3+转化为
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐1】碳酸钙是生活中常见的补钙剂,还可用于实验室制取CO2。回答下列问题:
(1)钙元素属于人体必需的______ (填“常量”或“微量”)元素。
(2)青少年缺钙易患______(填字母序号)。
(3)20g碳酸钙与足量稀盐酸反应,生成CO2的质量是多少?(写出计算步骤)
(1)钙元素属于人体必需的
(2)青少年缺钙易患______(填字母序号)。
| A.坏血病 | B.佝偻病 | C.贫血病 |
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐2】某硫酸厂废水中含有少量的硫酸,技术员检测废水中硫酸的质量分数为1%,现有98t废水,为达标排放,需要加入熟石灰中和至中性。请计算所需熟石灰的质量_____ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】已知碳酸氢钙[Ca(HCO3)2]为白色固体,易溶于水,在加热时会分解成碳酸钙,反应原理为Ca(HCO3)2  CaCO3+H2O+CO2↑,碳酸钙在高温下会继续分解产生氧化钙。如图是32.4g碳酸氢钙固体加热过程中固体质量随温度的变化关系。请回答:
CaCO3+H2O+CO2↑,碳酸钙在高温下会继续分解产生氧化钙。如图是32.4g碳酸氢钙固体加热过程中固体质量随温度的变化关系。请回答:______ 。(填“酸”“碱”或“盐”)
(2)加热至______ ℃时,碳酸氢钙分解完全。
(3)利用图像数据计算生成氧化钙的质量。(写出计算过程)
(4)32.4g碳酸氢钙固体在整个加热过程中释放二氧化碳的总质量为______ g。
 CaCO3+H2O+CO2↑,碳酸钙在高温下会继续分解产生氧化钙。如图是32.4g碳酸氢钙固体加热过程中固体质量随温度的变化关系。请回答:
CaCO3+H2O+CO2↑,碳酸钙在高温下会继续分解产生氧化钙。如图是32.4g碳酸氢钙固体加热过程中固体质量随温度的变化关系。请回答:
(2)加热至
(3)利用图像数据计算生成氧化钙的质量。(写出计算过程)
(4)32.4g碳酸氢钙固体在整个加热过程中释放二氧化碳的总质量为
您最近一年使用:0次

 6CO2 +2CO+16H2O.若反应生成7.2g水,请计算:
6CO2 +2CO+16H2O.若反应生成7.2g水,请计算:

