亚运会不仅采用氢气作为火炬燃料,还使用了大量氢燃料电池车。高纯度、低成本的大量制取和储存氢气已成为氢能源利用领域的研究热点。如图就是一种比较经济的制取氢气的新工艺流程。

(1)在制得氢气和氧化铝(Al2O3)的反应中,金属镓的作用可能是______ 。氢气是理想燃料的原因是______ (写出1点即可)。
(2)氧化铝可以在太阳光的条件下,借助太阳能重新变成氧气与金属铝,该反应的化学方程式为______ 。
(3)氧化铝生成铝和氧气的基本反应类型是______ 反应。
(4)氧化铝中铝元素的化合价为______ 。
(5)镁铝合金(Mg17Al12)是一种潜在的储氢材料,镁铝合金的熔点比镁的熔点要______ (填“高”或“一样”或“低”)。

(1)在制得氢气和氧化铝(Al2O3)的反应中,金属镓的作用可能是
(2)氧化铝可以在太阳光的条件下,借助太阳能重新变成氧气与金属铝,该反应的化学方程式为
(3)氧化铝生成铝和氧气的基本反应类型是
(4)氧化铝中铝元素的化合价为
(5)镁铝合金(Mg17Al12)是一种潜在的储氢材料,镁铝合金的熔点比镁的熔点要
更新时间:2024-03-29 21:05:05
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】中国将力争“碳排放”于2030年前达到峰值,争取在2060年前实现“碳中和”
(1)“碳中和”目的是使碳排放与碳吸收达平衡,最终实现零碳排放。结合如图1,提出一种可行的碳吸收方式:___________ 。一种捕集烟气中CO的过程如图所示:


①“吸收”时反应的化学方程式为___________ 。
②“转化”后得到的液体温度明显高于室温,可能的原因是___________ 。
③在整个捕集过程中,可以循环利用的物质是___________ 。
(2)“碳”的转化与利用
【转化I】以CO2为碳源,与H2经催化可转化为高附加值的有机物,此方法具有重要的战略意义。中国化学家使用特殊催化剂实现了CO2和H2转化为A或B等有机物和水,原理如图3所示:

①B的化学式是___________ 。
③根据催化剂的特性可知,催化剂在该反应前后的质量和___________ 不变。
③理论上讲,当原料气中碳、氢元素质量比为___________ ,最终产物是A。
【转化I】2020年哥伦比亚大学化学团队开发出了镍基双金属催化剂,用来将二氧化碳和甲烷两种温室气体在一定条件下进行重整得到两种气体燃料。反应过程如图4所示。

④写出反应的学方程式___________ ,反应一段时间后该催化剂的催化效果降低的原因是___________ 。
【转化Ⅱ】2020年10月15日我国千吨级“液态阳光”合成示范项目在兰州成功运行,该项目首次将太阳能规模转化为绿色液体燃料甲醇(CH3OH)。“液态阳光”生产过程如图所示。

⑤“液态阳光”生产过程中反应Ⅱ的化学方程式为___________ 。理论上反应Ⅰ消耗的H2O中氢元素质量___________ 反应Ⅱ生成的甲醇中反应Ⅱ催化剂氢元素质量(选填“>”、“<”或“=”)。
(1)“碳中和”目的是使碳排放与碳吸收达平衡,最终实现零碳排放。结合如图1,提出一种可行的碳吸收方式:


①“吸收”时反应的化学方程式为
②“转化”后得到的液体温度明显高于室温,可能的原因是
③在整个捕集过程中,可以循环利用的物质是
(2)“碳”的转化与利用
【转化I】以CO2为碳源,与H2经催化可转化为高附加值的有机物,此方法具有重要的战略意义。中国化学家使用特殊催化剂实现了CO2和H2转化为A或B等有机物和水,原理如图3所示:

①B的化学式是
③根据催化剂的特性可知,催化剂在该反应前后的质量和
③理论上讲,当原料气中碳、氢元素质量比为
【转化I】2020年哥伦比亚大学化学团队开发出了镍基双金属催化剂,用来将二氧化碳和甲烷两种温室气体在一定条件下进行重整得到两种气体燃料。反应过程如图4所示。

④写出反应的学方程式
【转化Ⅱ】2020年10月15日我国千吨级“液态阳光”合成示范项目在兰州成功运行,该项目首次将太阳能规模转化为绿色液体燃料甲醇(CH3OH)。“液态阳光”生产过程如图所示。

⑤“液态阳光”生产过程中反应Ⅱ的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】氢气是非常理想的清洁能源,用廉价的方法制氢气是许多科学家的愿望。下图就是一种比较经济的制取氢气的新工艺流程。
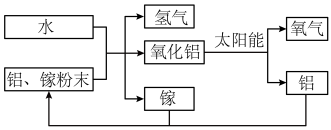
(1)在制得氢气和氧化铝(Al2O3)的反应中,金属镓的作用可能是_______ 。
(2)氢气是理想燃料的原因是_______ (写出1点即可);
(3)氧化铝可以借助太阳能重新变成氧气与金属铝,该反应的化学方程式为_______ ,所属的基本反应类型是_______ 。
(4)该生产流程中,可循环利用的物质是_______ 。

(1)在制得氢气和氧化铝(Al2O3)的反应中,金属镓的作用可能是
(2)氢气是理想燃料的原因是
(3)氧化铝可以借助太阳能重新变成氧气与金属铝,该反应的化学方程式为
(4)该生产流程中,可循环利用的物质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】甲醇(CH3OH)是一种重要的化工原料,工业上以煤、空气、水等为原料制备甲醇的主要工艺流程如下图。

(1)变换炉中发生反应: ,化合价发生变化的元素是
,化合价发生变化的元素是______ 。
(2)吸收塔中被吸收的物质是______ 。
(3)合成塔中发生化合反应,其反应的微观示意图如下,在方框内画出微粒图示。

(4)甲醇中的碳元素来自于原料中的______ 。

(1)变换炉中发生反应:
 ,化合价发生变化的元素是
,化合价发生变化的元素是(2)吸收塔中被吸收的物质是
(3)合成塔中发生化合反应,其反应的微观示意图如下,在方框内画出微粒图示。

(4)甲醇中的碳元素来自于原料中的
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】比较、归纳和总结是化学学习常用的方法,请结合所学知识填空:
(1)有下列三组物质:Ⅰ组O2 O3 Ⅱ组MnO2 CO2 P2O5 Ⅲ组KClO3 Ca(OH)2 CuSO4
①这些物质含有相同的元素,该元素是_______ 。
②Ⅰ组和Ⅱ、Ⅲ组的物质相比较,从组成上看不同之处在于_______ 。
③请补充一种属于Ⅱ组物质的化学式_______ 。
(2)找规律,填空
①化合价:HNO3、NO2、NaNO2、NO、_______ (写一氧化物的化学式)。
②已知物质间转化关系:H2O2→H2O→_______ (填化学式)→P2O5。
③物质的组成:CH4(甲烷)、C2H6(乙烷)、C3H8(丙烷)、C4H10、_______ 、_______ (戊烷)。
(1)有下列三组物质:Ⅰ组O2 O3 Ⅱ组MnO2 CO2 P2O5 Ⅲ组KClO3 Ca(OH)2 CuSO4
①这些物质含有相同的元素,该元素是
②Ⅰ组和Ⅱ、Ⅲ组的物质相比较,从组成上看不同之处在于
③请补充一种属于Ⅱ组物质的化学式
(2)找规律,填空
①化合价:HNO3、NO2、NaNO2、NO、
②已知物质间转化关系:H2O2→H2O→
③物质的组成:CH4(甲烷)、C2H6(乙烷)、C3H8(丙烷)、C4H10、
您最近一年使用:0次
【推荐3】电石渣[主要成分为Ca(OH)2,还含有MgO等杂质]是一种工业废渣,以它为原料可生产纳米碳酸钙,制备方案如下:

已知:
①NH4Cl溶液显酸性:氨水不稳定,易分解;
②“浸取”时的主要反应为
③“碳化”时的主要反应为
(1)电石渣久置在空气中会产生一定量的碱式碳酸钙 ,化学式中的n为
,化学式中的n为______ 。
(2)浸取时,向浸取液中滴加氨水调节pH,将镁元素全部沉淀,则操作1为______ (填操作名称)。

(3)工业上将操作1所得溶液碱化后。进行喷雾碳化,碳化塔的构造如图2所示,CO2从______ 处通入(填“A”或“B”),其目的是______ 。
(4)测得不同温度下碳化反应所需时间如下表(其他条件相同):
实际碳化反应的温度采用了______ °C,温度不宜过高的原因可能是______ 、______ 。
(5)该工艺流程的核心反应在“浸取”和“碳化”这两步,结合制备方案判断可循环利用的物质为______ 。

已知:
①NH4Cl溶液显酸性:氨水不稳定,易分解;
②“浸取”时的主要反应为

③“碳化”时的主要反应为

(1)电石渣久置在空气中会产生一定量的碱式碳酸钙
 ,化学式中的n为
,化学式中的n为(2)浸取时,向浸取液中滴加氨水调节pH,将镁元素全部沉淀,则操作1为

(3)工业上将操作1所得溶液碱化后。进行喷雾碳化,碳化塔的构造如图2所示,CO2从
(4)测得不同温度下碳化反应所需时间如下表(其他条件相同):
温度 | 反应液浑浊所需时间 (单位:秒) | 反应完全所需时间 (单位:分钟) |
20℃ | 480 | >180 |
40℃ | 120 | 180 |
60℃ | 1 | 50 |
80℃ | 1 | 68 |
(5)该工艺流程的核心反应在“浸取”和“碳化”这两步,结合制备方案判断可循环利用的物质为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】化学与生活联系密切,请回答下列问题。
(1)鉴别某水样是软水还是硬水,常加入的物质是______ 。
(2)通常情况下,合金的熔点比组成它们的纯金属熔点要______ ,硬度要______ 。
(3)双氧水、高锰酸钾都可以用来消毒,也可以用来制取氧气。实验室用双氧水制取氧气的化学方程式为______ ;用高锰酸钾制取氧气的化学方程式为______ 。
(4)喝了汽水以后,常常会打嗝,是因为气体的溶解度与______ 有关。
(5)“曾青得铁则化为铜”指的是铁和硫酸铜溶液能发生反应,该反应的基本反应类型为______ 。
(6)用汽油和加了洗涤剂的水都能去除衣服上的油污,但原理不同区别是______ 。
(1)鉴别某水样是软水还是硬水,常加入的物质是
(2)通常情况下,合金的熔点比组成它们的纯金属熔点要
(3)双氧水、高锰酸钾都可以用来消毒,也可以用来制取氧气。实验室用双氧水制取氧气的化学方程式为
(4)喝了汽水以后,常常会打嗝,是因为气体的溶解度与
(5)“曾青得铁则化为铜”指的是铁和硫酸铜溶液能发生反应,该反应的基本反应类型为
(6)用汽油和加了洗涤剂的水都能去除衣服上的油污,但原理不同区别是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】我国古代就掌握了炼铜技术,青铜是铜冶铸史上最早得到的合金。
I.用孔雀石【主要成分Cu2(OH)2CO3】炼铜。高温煅烧孔雀石,可得黑色固体和两种非金属氧化物。部分含铜元素的物质类别及化合价转化关系如图所示。

(1)图中Cu2(OH)2CO3位于A点,黑色固体位于_______ (选填B、C或D)点。
(2)加入木炭,一定条件下可实现C→D的转化,同时产生可使澄清石灰水变浑浊的气体。该过程体现了木炭具有_______ 性质反应的化学方程式为_______ 。
(3)图中A→B的反应属于_______ 反应(填基本反应类型)。
II.《大治赋》记载由硫化铜矿(主要成分Cu2S)制取CuSO4溶液,再用铁片浸取铜的方法。硫化铜矿中Cu2S转化的流程如下:

(4)Cu2S中Cu与S的质量比为_______ 。“浸铁”中利用了Fe的金属活动性比Cu_______ 的性质(选填“强”或“弱”)。
(5)依据上述流程分析,若需将Cu2S中铜元素全转化为铜单质,除了H2O、O2和Fe以外,还需补充的物质是_______ 。
(6)在冶炼中加入锡等金属可得到青铜,下列说法正确的是_______。
I.用孔雀石【主要成分Cu2(OH)2CO3】炼铜。高温煅烧孔雀石,可得黑色固体和两种非金属氧化物。部分含铜元素的物质类别及化合价转化关系如图所示。

(1)图中Cu2(OH)2CO3位于A点,黑色固体位于
(2)加入木炭,一定条件下可实现C→D的转化,同时产生可使澄清石灰水变浑浊的气体。该过程体现了木炭具有
(3)图中A→B的反应属于
II.《大治赋》记载由硫化铜矿(主要成分Cu2S)制取CuSO4溶液,再用铁片浸取铜的方法。硫化铜矿中Cu2S转化的流程如下:

(4)Cu2S中Cu与S的质量比为
(5)依据上述流程分析,若需将Cu2S中铜元素全转化为铜单质,除了H2O、O2和Fe以外,还需补充的物质是
(6)在冶炼中加入锡等金属可得到青铜,下列说法正确的是_______。
| A.青铜是金属材料 |
| B.纯铜比青铜的硬度大 |
| C.青铜比纯铜的熔点低 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】仰望天空,我们有牵挂,更有底气!因为空间站里有我们兢兢业业的中国航天员!占“神十三”的净重量85%以上的是——高精度铝合金材料。

(1)铝合金材料具有许多优良的性能,如_______ (填字母);
a. 耐腐蚀 、硬度小 b.密度小、强度高
(2)工业上冶炼铝是利用惰性电极电解氧化铝得到的。此反应的化学方程式为____________ ;
(3)“神十三”返回舱使用的氢气瓶来自于成都。液氢已应用于航天等领域,作为化学电源,氢氧燃料电池已经被应用。氢氧燃料电池汽车行驶时的能量转化为:__________ ;相信氢能源广泛应用后,我们的天空将更蓝、大气将更清新!这与氢能的优点——本身无毒且_________ 不污染空气有直接关系。

(1)铝合金材料具有许多优良的性能,如
a. 耐腐蚀 、硬度小 b.密度小、强度高
(2)工业上冶炼铝是利用惰性电极电解氧化铝得到的。此反应的化学方程式为
(3)“神十三”返回舱使用的氢气瓶来自于成都。液氢已应用于航天等领域,作为化学电源,氢氧燃料电池已经被应用。氢氧燃料电池汽车行驶时的能量转化为:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】2016年“冰箭”冲天,中国挺进大火箭时代。
(1)氢气的利用:火箭采用液氢、液氧作为推进剂,其内部温度极低,因此称为“冰箭”,氢气是____ (填序号)。
a.常规能源 b.绿色能源 c.不可再生能源
(2)氢气的制取:利用太阳能分解水制H2与电解水制H2相比,其优点是_______ ;
(3)氢燃料电池是将化学能直接转化为_______ ,且能量转化效率高达约80%;与化石燃料相比,氢能源的优点是:①原料来源广,②_______ ,③燃烧热值高。
(4)实验室制取氢气选择_____ 和_____ (填药品名称),发生装置选择_____ (填“固固加热型”或“固液常温型”),收集方法选择_____ 法或_______ 法,反应的方程式为_____ 。
(1)氢气的利用:火箭采用液氢、液氧作为推进剂,其内部温度极低,因此称为“冰箭”,氢气是
a.常规能源 b.绿色能源 c.不可再生能源
(2)氢气的制取:利用太阳能分解水制H2与电解水制H2相比,其优点是
(3)氢燃料电池是将化学能直接转化为
(4)实验室制取氢气选择
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】2015年4月22日是第46个世界地球日,其主题为“珍惜地球资源,转变发展方式——提高资源利用效益”。世界各国人民的节能意识日益增强,科学家也在开发新能源、研制新产品、提高化学能的转化效率等方面做着积极的努力。
(1)有待继续开发、利用的能源有(请回答三种):____________________________ 。
(2)用化学方程式表示一个由化学能转化为内能的例子________________ (写化合反应)。
(3)氢气具有热值高且________ 的特点,因此被认为是最清洁的能源。

(1)有待继续开发、利用的能源有(请回答三种):
(2)用化学方程式表示一个由化学能转化为内能的例子
(3)氢气具有热值高且

您最近一年使用:0次




