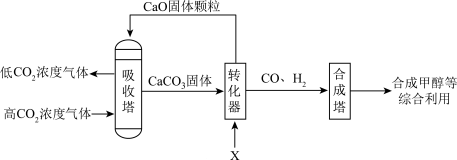
我国力争在2060年前实现“碳中和”。为实现这一目标,一种捕集烟气中二氧化碳并转化利用的流程如图:______ 。
(2)“转化器”中发生的反应是 ,X化学式是
,X化学式是______ 。
(3)“合成塔”中发生的基本反应类型是______ ,参加反应的CO和 的质量最简比是
的质量最简比是______ 。
(4)甲醇可以作燃料,甲醇在氧气中充分燃烧生成二氧化碳和水,反应的化学方程式是______ 。
(2)“转化器”中发生的反应是
 ,X化学式是
,X化学式是(3)“合成塔”中发生的基本反应类型是
 的质量最简比是
的质量最简比是(4)甲醇可以作燃料,甲醇在氧气中充分燃烧生成二氧化碳和水,反应的化学方程式是
2024·江西上饶·模拟预测 查看更多[4]
(已下线)专题09 推断题、工业流程题、溶解度曲线题-2024年中考化学二轮热点题型归纳与变式演练(辽宁专用)(已下线)易错类型12 工艺流程“四个”易错提醒-备战2024年中考化学考试易错题(全国通用)2024年江西省九江市修水县散原中学分校中考模拟预测化学试题2024年江西省上饶市鄱阳县私立洪迈学校学业水平模拟练习化学试卷(二)
更新时间:2024-05-03 20:48:43
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
【推荐1】天然气与煤炭、石油等能源相比具有使用安全、热值高、洁净等优势。天然气的主要成分是甲烷,此外还含有少量的乙烷、丙烷、二氧化碳、一氧化碳等。
(1)天然气属于______ (填“混合物”或“纯净物”)。
(2)甲烷燃烧时发生的化学反应的微观示意图如下图所示。其中, 表示碳原子,
表示碳原子, 表示氧原子,
表示氧原子, 表示氢原子。
表示氢原子。

①A中分子为甲烷分子,1个甲烷分子中含有____ 个原子。
②甲烷中碳、氢元素质量比为________ 。
③根据图示信息,写出甲烷燃烧反应的化学方程式________ 。
(3)甲烷不仅可以作为燃料,还可以用于制造多种物质。例如,在高温条件下,甲烷可以生成碳和氢气,该反应的化学方程式式为:____________ ,基本反应类型为__________ 。
(1)天然气属于
(2)甲烷燃烧时发生的化学反应的微观示意图如下图所示。其中,
 表示碳原子,
表示碳原子, 表示氧原子,
表示氧原子, 表示氢原子。
表示氢原子。
①A中分子为甲烷分子,1个甲烷分子中含有
②甲烷中碳、氢元素质量比为
③根据图示信息,写出甲烷燃烧反应的化学方程式
(3)甲烷不仅可以作为燃料,还可以用于制造多种物质。例如,在高温条件下,甲烷可以生成碳和氢气,该反应的化学方程式式为:
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
真题
【推荐2】锰及其化合物在生产中有重要作用。
(1)已知:MnSO4+K2MnO4=2MnO2↓+K2SO4, 3MnSO4+2KMnO4+2H2=5MnO2↓+K 2SO4+2H2SO4,则:①K2MnO4的名称是_____ 。上述化合物中,Mn元素化合价最高的是_____ 。
②实验室加热高锰酸钾制取氧气后,将固体剩余物中的锰元素全部以MnO2形式回收的方法是:将剩余物加入适量_____ 溶液中,搅拌,充分反应后,过滤、洗涤、烘干即可。
(2)在高温下,Al与MnO2发生置换反应可制备Mn.反应的化学方程式是_____ 。
(3)锰锌铁氧体是一种隐形飞机表面涂料,其化学组成为 MnxZn1﹣x Fe2O4(铁为+3价)。锰锌铁氧体中锰元素的化合价为_____ ,当锰锌铁氧体中Zn与Fe原子个数比为2:5时,它对某频段的雷达波吸收能力最强,其化学式为_____
(1)已知:MnSO4+K2MnO4=2MnO2↓+K2SO4, 3MnSO4+2KMnO4+2H2=5MnO2↓+K 2SO4+2H2SO4,则:①K2MnO4的名称是
②实验室加热高锰酸钾制取氧气后,将固体剩余物中的锰元素全部以MnO2形式回收的方法是:将剩余物加入适量
(2)在高温下,Al与MnO2发生置换反应可制备Mn.反应的化学方程式是
(3)锰锌铁氧体是一种隐形飞机表面涂料,其化学组成为 MnxZn1﹣x Fe2O4(铁为+3价)。锰锌铁氧体中锰元素的化合价为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】MnCO3用作涂料和清漆的颜料。MnCO3不溶于水,100℃时开始分解。以软锰矿(主要成分为MnO2)为原料制备高纯MnCO3的流程如下:
已知:①反应I的化学方程式为 。
。
②MnCO3、Mn(OH)2均难溶于水。
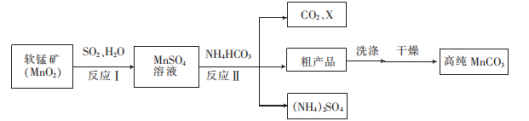
(1)MnCO3是__________ (选填“酸”、“碱"”或“盐”),其中Mn的化合价是__________ 。
(2)反应Ⅱ的生成物X是一种常见的液体,则X是_________ (写化学式)。
(3)干燥MnCO3时应选择___________ (选填“低温”或“高温”)。
(4)写出副产物(NH4)2SO4的一种用途:___________ 。
已知:①反应I的化学方程式为
 。
。②MnCO3、Mn(OH)2均难溶于水。

(1)MnCO3是
(2)反应Ⅱ的生成物X是一种常见的液体,则X是
(3)干燥MnCO3时应选择
(4)写出副产物(NH4)2SO4的一种用途:
您最近一年使用:0次
【推荐2】化学就在我们身边,人类的生活离不开化学。请回答下列问题:
(1)“稻花香里说丰年,听取蛙声一片”,请从微观角度分析闻到花香的原因:______ ;金秋九月,我们收获金灿灿的稻谷,稻谷包含的营养素主要为糖类,糖类是由______ (填元素符号)三种元素组成;稻草秸秆可以放在密闭的沼气池中发酵产生沼气,请写出沼气的主要成分充分燃烧的化学方程式:______ ;
(2)江汉平原有诸多的风力发电设备,风力发电站通过电线将电输送到千家万户,铜是用作电线的常见材料,是利用了铜的延展性和______ 性。
(3)氯化钠是日常生活中重要的调味品,也是重要的化工原料,工业上利用电解饱和的食盐水生产氯气,反应的化学方程式为: ,请写出X的化学式:
,请写出X的化学式:______ ;
(4)安全是全社会关注的焦点,如果炒菜时油锅中的油不慎着火,可以用锅盖盖灭,请分析该灭火的原理是:______ ;
(5)甲、乙两种固体物质的溶解度曲线如图所示。根据图示,回答下列问题:

①将甲物质的不饱和溶液转变成饱和溶液可采取的方法有______ (写出一种即可)。
②将t1℃下甲、乙的饱和溶液同时升温到t2℃,两溶液溶质质量分数的大小关系是甲______ 乙(填“>”、“=”或“<”)。
(1)“稻花香里说丰年,听取蛙声一片”,请从微观角度分析闻到花香的原因:
(2)江汉平原有诸多的风力发电设备,风力发电站通过电线将电输送到千家万户,铜是用作电线的常见材料,是利用了铜的延展性和
(3)氯化钠是日常生活中重要的调味品,也是重要的化工原料,工业上利用电解饱和的食盐水生产氯气,反应的化学方程式为:
 ,请写出X的化学式:
,请写出X的化学式:(4)安全是全社会关注的焦点,如果炒菜时油锅中的油不慎着火,可以用锅盖盖灭,请分析该灭火的原理是:
(5)甲、乙两种固体物质的溶解度曲线如图所示。根据图示,回答下列问题:

①将甲物质的不饱和溶液转变成饱和溶液可采取的方法有
②将t1℃下甲、乙的饱和溶液同时升温到t2℃,两溶液溶质质量分数的大小关系是甲
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐3】2018年1月19日,长十一运载火箭成功将6颗卫星送人预定轨道。回答问题
(1)制造火箭需使用钛合金、铝合金、钨合金、不锈钢等合金,合金与其成分金属相比的优点_______________________ 。
(2)火箭常用泡沫塑料作夹层填充物,用合成橡胶作密封材料,泡沫塑料和合成橡胶都属于____________ 材料。
(3)火箭推进剂有多种,液氧和液氢是其中两种,从微观角度分析,加压、降温使氧气和氢气液化时,分子的运动速率减小,__________________ 。
(4)长十一运载火箭使用的燃料是固体燃料,铝粉和高氯酸铵(NH4C1O4)可用作固体火箭燃料,高氯酸铵中氯元素的化合价为______ ,点燃时铝粉氧化放出的热量使高氯酸铵分解: ,式中X的化学式为
,式中X的化学式为___________ 。
(1)制造火箭需使用钛合金、铝合金、钨合金、不锈钢等合金,合金与其成分金属相比的优点
(2)火箭常用泡沫塑料作夹层填充物,用合成橡胶作密封材料,泡沫塑料和合成橡胶都属于
(3)火箭推进剂有多种,液氧和液氢是其中两种,从微观角度分析,加压、降温使氧气和氢气液化时,分子的运动速率减小,
(4)长十一运载火箭使用的燃料是固体燃料,铝粉和高氯酸铵(NH4C1O4)可用作固体火箭燃料,高氯酸铵中氯元素的化合价为
 ,式中X的化学式为
,式中X的化学式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某兴趣小组的同学从实验室收集到一桶含有 FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如图操作方案,结合方案回答下列问题:

(1)固体 A 中含有______ (填化学式)。
(2)操作 a 的名称是______ 。
(3)加入过量 Fe 的目的是______ 。
(4)若 11.2g Fe 与足量稀硫酸完全反应,产生氢气的质量为______ g。

(1)固体 A 中含有
(2)操作 a 的名称是
(3)加入过量 Fe 的目的是
(4)若 11.2g Fe 与足量稀硫酸完全反应,产生氢气的质量为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
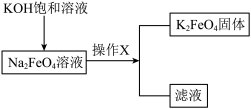
【推荐2】高铁酸钾(K2FeO4)是一种新型高效水处理剂。如图是制备K2FeO4的流程(已知:K2FeO4在中性和酸性条件下易分解):______ 。
(2)K2FeO4应保存在______ (选填“酸”、“中”或“碱”)性环境,防止其分解。
(3)Na2FeO4由______ 种元素组成,其中铁、氧元素的质量比为______ 。
(4)操作X是______ 。
(5)Na2FeO4与KOH发生的是复分解反应(Na2FeO4+2KOH═K2FeO4↓+2NaOH)。要制取19.8gK2FeO4需要KOH的质量为______ 。
(2)K2FeO4应保存在
(3)Na2FeO4由
(4)操作X是
(5)Na2FeO4与KOH发生的是复分解反应(Na2FeO4+2KOH═K2FeO4↓+2NaOH)。要制取19.8gK2FeO4需要KOH的质量为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A~F是初中化学常见的物质,它们之间的相互关系如图所示(部分物质和反应条件已略去)。A、B、C、D、E为不同类别的物质,其中C的浓溶液具有挥发性,A属于金属氧化物,其金属元素的质量分数为70%;E是大理石的主要成分;F是一种白色固体。B的化学式为__________ ;F转化为D的化学方程式为__________ ;写出一种D在生产生活中的用途__________ 。


您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
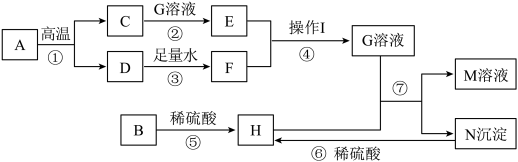
【推荐2】已知A、B、C、D、E、F为常见物质,其中A、B含有相同的元素,B、E为氧化物,C、D、F都为单质。它们相互转化的关系如右图所示
(图中反应条件略去)。
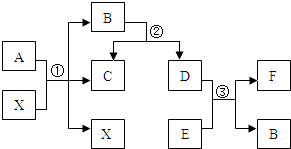
(1)X在反应①中起___________ 作用。
(2)写出有关物质的化学式: A_________ 、C ______________ 。
(3)若F不溶于稀硫酸,写出反应③的化学方程式_____________ ,
该反应的基本类型是_________ 。与D具有相同化学性质,并能与E发生反应,且反应基本类型与③相同的物质有 __________ 。
(图中反应条件略去)。

(1)X在反应①中起
(2)写出有关物质的化学式: A
(3)若F不溶于稀硫酸,写出反应③的化学方程式
该反应的基本类型是
您最近一年使用:0次

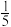 的结论。该实验过程涉及两个化学反应,写出其中任意一个反应的化学方程式
的结论。该实验过程涉及两个化学反应,写出其中任意一个反应的化学方程式