请回答下列问题。
(1)实验室现有一瓶用石灰石和稀盐酸制取二氧化碳后的剩余废液,某小组同学想探究该废液中是否有残留的稀盐酸存在。
①甲同学向剩余废液中加入紫色石蕊试液,若观察到_______ 的现象,则证明该废液中一定存在稀盐酸。
②乙同学从下列四种试剂中选取了一种试剂,也成功验证了废液中是否有残留的稀盐酸。则他所选的试剂可能是_______ (填选项序号之一)。
A.硝酸银溶液 B.氢氧化钠溶液 C.碳酸钠溶液 D.酚酞试液
③若要除去废液中的稀盐酸,在不使用酸碱指示剂的情况下,可选用下列试剂中的_______ (填选项序号之一)。
A.石灰水 B.生石灰 C.石灰石粉末 D.氢氧化钠溶液
(2)学习小组的同学欲探究某固体混合物的成分,已知某硝酸钾样品中可能含有氯化钠、碳酸氢钠、硫酸钠、碳酸钠、氯化钙五种物质中的两种或多种。按下图所示进行探究实验,出现的现象如图中所述。(设过程中所有发生的反应都恰好完全反应)
①在常温下,气体A的水溶液pH_______ 7(选填“大于”“等于”“小于”之一)。
②写出步骤I中发生反应的化学方程式:_______ 。
③溶液C中,一定大量存在的酸根阴离子是_______ (填离子符号)。
④根据实验现象,推断该混合物中一定不含有的物质是_______ (填化学式);理由是_______ 。
⑤经测定,实验过程中产生的气体A和气体D的质量相等,则碳酸钠_______ (选填“一定存在”“一定不存在”“无法确定”之一)。
(1)实验室现有一瓶用石灰石和稀盐酸制取二氧化碳后的剩余废液,某小组同学想探究该废液中是否有残留的稀盐酸存在。
①甲同学向剩余废液中加入紫色石蕊试液,若观察到
②乙同学从下列四种试剂中选取了一种试剂,也成功验证了废液中是否有残留的稀盐酸。则他所选的试剂可能是
A.硝酸银溶液 B.氢氧化钠溶液 C.碳酸钠溶液 D.酚酞试液
③若要除去废液中的稀盐酸,在不使用酸碱指示剂的情况下,可选用下列试剂中的
A.石灰水 B.生石灰 C.石灰石粉末 D.氢氧化钠溶液
(2)学习小组的同学欲探究某固体混合物的成分,已知某硝酸钾样品中可能含有氯化钠、碳酸氢钠、硫酸钠、碳酸钠、氯化钙五种物质中的两种或多种。按下图所示进行探究实验,出现的现象如图中所述。(设过程中所有发生的反应都恰好完全反应)

①在常温下,气体A的水溶液pH
②写出步骤I中发生反应的化学方程式:
③溶液C中,一定大量存在的酸根阴离子是
④根据实验现象,推断该混合物中一定不含有的物质是
⑤经测定,实验过程中产生的气体A和气体D的质量相等,则碳酸钠
更新时间:2024-04-15 09:12:03
|
相似题推荐
综合应用题
|
适中
(0.65)
【推荐1】实验室有盐酸、白醋和柠檬酸三种溶液,回答下列问题:
(1)向氧化铁中放入足量盐酸,振荡,充分反应后,观察到的现象是_________________ ,反应的化学方程式是________________________________________ 。
(2)白醋、柠檬酸溶液也能与氧化铁发生类似反应,说明白醋、柠檬酸溶液和盐酸中都含有的离子是__________ 。
(3)理论上溶解3.2g氧化铁,需要36.5%盐酸__________ g。
(1)向氧化铁中放入足量盐酸,振荡,充分反应后,观察到的现象是
(2)白醋、柠檬酸溶液也能与氧化铁发生类似反应,说明白醋、柠檬酸溶液和盐酸中都含有的离子是
(3)理论上溶解3.2g氧化铁,需要36.5%盐酸
您最近一年使用:0次
综合应用题
|
适中
(0.65)
真题
【推荐2】化学使世界变得更加绚丽多彩。
【品读化学史】
(1)火的利用是人类最早的一项化学实践活动。《庄子·外物篇》记载:“木与木相摩则然(通‘燃’)”。从燃烧的条件来看,摩擦的作用是_______ 。
【领略化学美】
(2)陶瓷是火与土的结晶,是化学与艺术的融合,是中华文明的象征之一。
①陶瓷之美在于色泽。宋代青瓷有“千峰翠色”美誉。陶土中的氧化铁与窑炉内的一氧化碳反应,部分转化为氧化亚铁使瓷器呈青色,同时生成一种能使澄清石灰水变浑浊的气体,写出该反应的化学方程式:_______ 。
②颜料赋予陶瓷精彩,一种用焙烧黄铁矿产生的红渣(成分为 和
和 ,
, 不溶于水和常见的酸)为原料制备颜料铵铁蓝的工艺流程如下。
不溶于水和常见的酸)为原料制备颜料铵铁蓝的工艺流程如下。

a.将红渣粉碎的目的是_______ 。“酸浸”时,溶液由无色变为_______ 色。
b.结合已知流程判断,工序①中可能包含的操作有_______ (填序号)。
A.溶解 B.蒸发 C.结晶 D.过滤
③古代陶器常用作饮具,陶器表面被炭烟熏黑,可用 的过氧化氢溶液擦洗清除。现欲配制
的过氧化氢溶液擦洗清除。现欲配制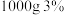 的过氧化氢溶液,需要
的过氧化氢溶液,需要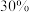 的过氧化氢溶液
的过氧化氢溶液_______ g。
【探寻化学味】
(3)食品膨松剂能使面包、饼干等食品口感松软或酥脆。某化学兴趣小组对一种膨松剂的组成(成分为 和
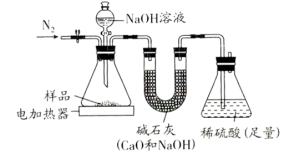
和 的混合物)进行分析,设计方案如下:如图所示,向
的混合物)进行分析,设计方案如下:如图所示,向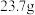 样品中滴加过量的氢氧化钠溶液,反应完全后,边加热边缓慢通入氮气。经测定,稀硫酸吸收的氨气质量为
样品中滴加过量的氢氧化钠溶液,反应完全后,边加热边缓慢通入氮气。经测定,稀硫酸吸收的氨气质量为 (损失忽略不计)。
(损失忽略不计)。
已知: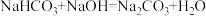 ;
;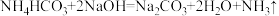 。
。
①通入氮气的目的是_______ ,加热的作用是_______ 。
②样品中碳酸氢钠与碳酸氢铵的质量比为_______ 。(写出解题过程)
【品读化学史】
(1)火的利用是人类最早的一项化学实践活动。《庄子·外物篇》记载:“木与木相摩则然(通‘燃’)”。从燃烧的条件来看,摩擦的作用是
【领略化学美】
(2)陶瓷是火与土的结晶,是化学与艺术的融合,是中华文明的象征之一。
①陶瓷之美在于色泽。宋代青瓷有“千峰翠色”美誉。陶土中的氧化铁与窑炉内的一氧化碳反应,部分转化为氧化亚铁使瓷器呈青色,同时生成一种能使澄清石灰水变浑浊的气体,写出该反应的化学方程式:
②颜料赋予陶瓷精彩,一种用焙烧黄铁矿产生的红渣(成分为
 和
和 ,
, 不溶于水和常见的酸)为原料制备颜料铵铁蓝的工艺流程如下。
不溶于水和常见的酸)为原料制备颜料铵铁蓝的工艺流程如下。
a.将红渣粉碎的目的是
b.结合已知流程判断,工序①中可能包含的操作有
A.溶解 B.蒸发 C.结晶 D.过滤
③古代陶器常用作饮具,陶器表面被炭烟熏黑,可用
 的过氧化氢溶液擦洗清除。现欲配制
的过氧化氢溶液擦洗清除。现欲配制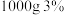 的过氧化氢溶液,需要
的过氧化氢溶液,需要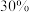 的过氧化氢溶液
的过氧化氢溶液【探寻化学味】
(3)食品膨松剂能使面包、饼干等食品口感松软或酥脆。某化学兴趣小组对一种膨松剂的组成(成分为
 和
和 的混合物)进行分析,设计方案如下:如图所示,向
的混合物)进行分析,设计方案如下:如图所示,向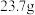 样品中滴加过量的氢氧化钠溶液,反应完全后,边加热边缓慢通入氮气。经测定,稀硫酸吸收的氨气质量为
样品中滴加过量的氢氧化钠溶液,反应完全后,边加热边缓慢通入氮气。经测定,稀硫酸吸收的氨气质量为 (损失忽略不计)。
(损失忽略不计)。
已知:
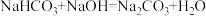 ;
;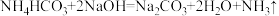 。
。①通入氮气的目的是
②样品中碳酸氢钠与碳酸氢铵的质量比为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下:

【资料】:
①垃圾焚烧产生的烟气中含有SO2、HCl等有害气体:
②+2价的铁元素容易被空气中的氧气氧化:
③SO2与CO2的化学性质相似。
(1)“烟气吸收”步骤中,石灰浆的作用是______ 。
(2)“生锈的铁制品溶解步骤中,共发生三个反应:
①铁锈与稀硫酸反应:_________ 。
②铁与稀硫酸反应: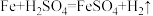
③铁与硫酸铁溶液反应:
(3)将所得硫酸亚铁溶液通过在氮气环境中加热蒸发浓缩,冷却结晶等操作,可得到硫酸亚铁晶体,认真阅读资料推测氮气的作用是________ 。
(4)列举一例生活中常见的防止铁生锈的方法:__________ 。
(5)计算:若垃圾焚烧产生32kgSO2,理论上吸收这些SO2需要消耗的氢氧化钙的质量是多少?
解:设消耗的氢氧化钙的质量为x
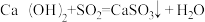 。
。
(请将计算过程补充完整)

【资料】:
①垃圾焚烧产生的烟气中含有SO2、HCl等有害气体:
②+2价的铁元素容易被空气中的氧气氧化:
③SO2与CO2的化学性质相似。
(1)“烟气吸收”步骤中,石灰浆的作用是
(2)“生锈的铁制品溶解步骤中,共发生三个反应:
①铁锈与稀硫酸反应:
②铁与稀硫酸反应:
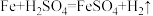
③铁与硫酸铁溶液反应:

(3)将所得硫酸亚铁溶液通过在氮气环境中加热蒸发浓缩,冷却结晶等操作,可得到硫酸亚铁晶体,认真阅读资料推测氮气的作用是
(4)列举一例生活中常见的防止铁生锈的方法:
(5)计算:若垃圾焚烧产生32kgSO2,理论上吸收这些SO2需要消耗的氢氧化钙的质量是多少?
解:设消耗的氢氧化钙的质量为x
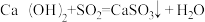 。
。(请将计算过程补充完整)
您最近一年使用:0次
【推荐1】根据化学知识回答:
Ⅰ、溶液颜色的变化蕴含许多知识。
(1)下列物质加入水中能形成有色溶液的是______。
(2)进行水电解实验时,将含酚酞的稀Na2SO4溶液(呈中性且不参与反应)加入如图所示的装置中,打开电源。
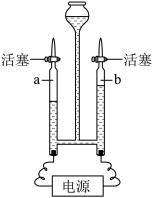
①a管中收集到的气体是______ ,a、b两管中收集到的气体质量比为______ 。
②通电后b管电极处溶液呈红色,电解结束后将容器内所有液体倒入烧杯中混合均匀,溶液又呈无色。下列说法正确的是______ 。
A.Na2SO4溶液使酚酞变红
B.电解过程中,b电极处中有酸性物质生成
C.待溶液混合均匀后呈无色,说明电解时a电极附近溶液呈酸性
Ⅱ、食盐的用途广泛,在工业上是制备纯碱的原料之一。1926年我国科学家侯德榜创立侯氏制碱法,大大提高了食盐的利用率,促进了世界制碱技术的发展。如图为氯化铵、氯化钠的溶解度曲线。试回答下列问题:

(3)t2℃时,NH4CI饱和溶液的溶质质量分数______ NaCl的饱和溶液的溶质质量分数(填“大于”“等于”或“小于”)。
(4)将t2℃时,将30gNH4Cl固体加入到50g水中,充分溶解后,所得NH4Cl溶液的溶质质量分数______ (列式,无需计算结果)。
(5)若NH4Cl中含有少量的NaCl,提纯NH4Cl可以用______ 法。
Ⅰ、溶液颜色的变化蕴含许多知识。
(1)下列物质加入水中能形成有色溶液的是______。
| A.碳酸钙 | B.高锰酸钾 | C.植物油 | D.食盐 |

①a管中收集到的气体是
②通电后b管电极处溶液呈红色,电解结束后将容器内所有液体倒入烧杯中混合均匀,溶液又呈无色。下列说法正确的是
A.Na2SO4溶液使酚酞变红
B.电解过程中,b电极处中有酸性物质生成
C.待溶液混合均匀后呈无色,说明电解时a电极附近溶液呈酸性
Ⅱ、食盐的用途广泛,在工业上是制备纯碱的原料之一。1926年我国科学家侯德榜创立侯氏制碱法,大大提高了食盐的利用率,促进了世界制碱技术的发展。如图为氯化铵、氯化钠的溶解度曲线。试回答下列问题:

(3)t2℃时,NH4CI饱和溶液的溶质质量分数
(4)将t2℃时,将30gNH4Cl固体加入到50g水中,充分溶解后,所得NH4Cl溶液的溶质质量分数
(5)若NH4Cl中含有少量的NaCl,提纯NH4Cl可以用
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】(1)如图所示是初中化学常见的实验装置图,请回答:

①实验室用B装置制取氧气,反应的化学方程式为______ 。
②若用F装置收集氧气,气体应从______ (填“a”或“b”)端进入。
③实验室制取并收集一瓶二氧化碳气体,应选用的装置为______ (填字母序号),在装入药品前应先______ ,该反应的化学方程式为______ 。
④实验室用该方法制取的二氧化碳常混杂一种气体杂质。若检验该杂质用到的试剂是______ 。
(2)皮蛋又称松花蛋,因其风味独特,深受人们喜爱。某兴趣小组在市场上获得了少许腌制皮蛋的原料。拿到实验室进行实验。将该固体混合物放于烧杯中,缓慢加入足量的蒸馏水,充分溶解后过滤,得到白色沉淀A和无色澄清滤液B。
【提出问题】①白色沉淀A是什么?
②无色滤液B中的溶质有哪些?
【查阅资料】腌制皮蛋的原料配方是少量NaCl、CaO和过量Na2CO3的固体混合物。
【理论推理】①白色沉淀A是CaCO3
②滤液B中含有Na2CO3、NaOH、NaCl三种溶质。
【实验验证】为证明滤液B中存在的三种溶质,同学们进行了如下实验。
【拓展提升】
①向步骤I中加入过量Ba(NO3)2溶液的目的是______ 。
②小妮同学认为若将步骤I中的Ba(NO3)2,溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质。你认为是否合理______ (填“合理”或“不合理”)。

①实验室用B装置制取氧气,反应的化学方程式为
②若用F装置收集氧气,气体应从
③实验室制取并收集一瓶二氧化碳气体,应选用的装置为
④实验室用该方法制取的二氧化碳常混杂一种气体杂质。若检验该杂质用到的试剂是
(2)皮蛋又称松花蛋,因其风味独特,深受人们喜爱。某兴趣小组在市场上获得了少许腌制皮蛋的原料。拿到实验室进行实验。将该固体混合物放于烧杯中,缓慢加入足量的蒸馏水,充分溶解后过滤,得到白色沉淀A和无色澄清滤液B。
【提出问题】①白色沉淀A是什么?
②无色滤液B中的溶质有哪些?
【查阅资料】腌制皮蛋的原料配方是少量NaCl、CaO和过量Na2CO3的固体混合物。
【理论推理】①白色沉淀A是CaCO3
②滤液B中含有Na2CO3、NaOH、NaCl三种溶质。
【实验验证】为证明滤液B中存在的三种溶质,同学们进行了如下实验。
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| Ⅰ | 取少量滤液B于试管中,加入过量的Ba(NO3)2溶液,过滤 | 滤液B中含有Na2CO3、NaOH、NaCl | |
| Ⅱ | 取少量步骤I中所得滤液于试管中,加入酚酞溶液 | ||
| Ⅲ | 另取少量步骤I中所得滤液于试管中,先加入足 量的稀硝酸,再加入 | 产生白色沉淀 |
①向步骤I中加入过量Ba(NO3)2溶液的目的是
②小妮同学认为若将步骤I中的Ba(NO3)2,溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质。你认为是否合理
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组利`用下列装置进行O2、CO2的实验室制法和有关性质的探究。
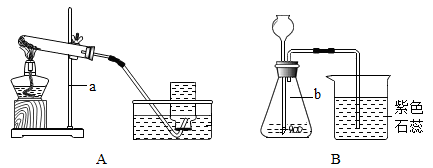
(1)写出图中所标仪器的名称b________
(2)用氯酸钾和二氧化锰固体混合物来制取O2,应选用上图中的________ 装置(填字母),其发生反应的化学方程式为_______________________ 。
(3)①写出B装置中产生CO2的化学方程式_______________________ 。
②某同学用浓盐酸和大理石在B装置中反应,并检验CO2的有关性质。此时观察到烧杯中紫色石蕊溶液变红,你对这一变化的合理解释有________ (填字母)。
A.产生的CO2直接使石蕊溶液变红
B.产生的CO2与水反应生成H2CO3使石蕊溶液变红
C.挥发出的氯化氢溶于水使石蕊溶液变红
(4)若B中烧杯内盛有含氢氧化钙0.37 g的石灰水,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是多少?(请写出计算过程)_____________________ 。

(1)写出图中所标仪器的名称b
(2)用氯酸钾和二氧化锰固体混合物来制取O2,应选用上图中的
(3)①写出B装置中产生CO2的化学方程式
②某同学用浓盐酸和大理石在B装置中反应,并检验CO2的有关性质。此时观察到烧杯中紫色石蕊溶液变红,你对这一变化的合理解释有
A.产生的CO2直接使石蕊溶液变红
B.产生的CO2与水反应生成H2CO3使石蕊溶液变红
C.挥发出的氯化氢溶于水使石蕊溶液变红
(4)若B中烧杯内盛有含氢氧化钙0.37 g的石灰水,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是多少?(请写出计算过程)
您最近一年使用:0次
【推荐1】天然碱(xNa2CO3‧yNaHCO3‧zH2O)是一种重要的工业原料,在纺织、医疗、食品等领域有着广泛的应用。研究小组对天然碱的组成进行探究和测定。
查阅资料:300℃时,NaHCO3完全分解生成碳酸钠、二氧化碳和水。
研究小组进行如下图所示的实验。
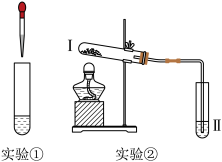
实验①:在2支分别盛有少量Na2CO3和NaHCO3溶液的试管中,分别滴加盐酸,2支试管中均有气泡产生,如实验①所示。
实验②:向Ⅱ中加入试剂a,向Ⅰ中加入少量Na2CO3或NaHCO3两种固体,分别加热一段时间。Na2CO3受热时Ⅱ中无明显现象,NaHCO3受热时Ⅱ中出现浑浊。
实验③:称取一定质量的天然碱样品于试管中,300℃时充分加热至完全分解,产生0.22gCO2和0.45g水。
实验④:另取与实验③相同质量的天然碱样品于锥形瓶中,加入足量的稀盐酸,完全反应后,产生1.32g CO2。
(1)实验①中,NaHCO3与盐酸反应的化学方程式为_______ 。
(2)足量7.3%的盐酸与10.6g碳酸钠反应,消耗盐酸的质量是_______ g。
(3)实验②中,试剂a是_______ 。
(4)计算确定天然碱(xNa2CO3▪yNaHCO3▪zH2O)的化学式_____ (写出计算过程)。
查阅资料:300℃时,NaHCO3完全分解生成碳酸钠、二氧化碳和水。
研究小组进行如下图所示的实验。

实验①:在2支分别盛有少量Na2CO3和NaHCO3溶液的试管中,分别滴加盐酸,2支试管中均有气泡产生,如实验①所示。
实验②:向Ⅱ中加入试剂a,向Ⅰ中加入少量Na2CO3或NaHCO3两种固体,分别加热一段时间。Na2CO3受热时Ⅱ中无明显现象,NaHCO3受热时Ⅱ中出现浑浊。
实验③:称取一定质量的天然碱样品于试管中,300℃时充分加热至完全分解,产生0.22gCO2和0.45g水。
实验④:另取与实验③相同质量的天然碱样品于锥形瓶中,加入足量的稀盐酸,完全反应后,产生1.32g CO2。
(1)实验①中,NaHCO3与盐酸反应的化学方程式为
(2)足量7.3%的盐酸与10.6g碳酸钠反应,消耗盐酸的质量是
(3)实验②中,试剂a是
(4)计算确定天然碱(xNa2CO3▪yNaHCO3▪zH2O)的化学式
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】钠及其化合物是中学化学学习和研究的重要内容。
(1)钠属于______ (填“金属”或“非金属”)元素,在化学反应中容易______ (填“得到”或“失去”电子。
(2)钠与水反应生成氢氧化钠和氢气,化学方程式为______ ;小苏打(NaHCO3)受热分解成碳酸钠、二氧化碳和水,化学方程式为______ 。
(3)配制一瓶如图溶液需氯化钠______ g;配制50g 6%氯化钠溶液,若用量筒量取水时俯视读数(其他操作正确),则溶液的质量分数______ 6%(填“>”、“<”或“=”)。
(4)钛和钛合金性能优良,广泛用于航空、造船和化学工业中、工业上常用钠来制取钛,在高温时,钠与四氯化钛(TiCl4)反应生成氯化钠和钛。若用该方法制取2.4kg钛,理论上需要钠的质量是多少?(写出计算过程)
(1)钠属于
(2)钠与水反应生成氢氧化钠和氢气,化学方程式为
(3)配制一瓶如图溶液需氯化钠
| 氯化钠注射液 【成分】氯化钠、水 【规格】500mL 质量分数0.9% 【密度】1.0g/cm3 |
(4)钛和钛合金性能优良,广泛用于航空、造船和化学工业中、工业上常用钠来制取钛,在高温时,钠与四氯化钛(TiCl4)反应生成氯化钠和钛。若用该方法制取2.4kg钛,理论上需要钠的质量是多少?(写出计算过程)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】碳酸氢钠俗称小苏打。在生活、医药方面有广泛应用。
(1)取溶质质量分数为4%的碳酸氢钠溶液50克,稀释成2%的溶液,需要加水______ 克。
(2)将一定质量的碳酸氢钠溶液和稀盐酸混合,充分反应,有气体逸出。
①写出该反应的化学方程式__________ 。
②探究反应后溶液除含有氯化钠,还有无剩余的反应物,某同:学取反应后的溶液倒不同方案进行如下实验。
【实验用品】pH试纸、稀盐酸、硝酸银溶液、氢氧化钠溶液、氧化铁粉未。
【进行实验】(提示:氯化银为不溶于水的白色物质)
a.方案A中的实验现象______ ;方案C中的实验现象:pH______ 7。
b.某同学认为仅凭方案B的现象,不能得出反应后溶液中有稀盐酸剩余的结论,他的理由是____ 。
(3)用碳酸氢钠测定盐酸的溶质质量分数。在一定条件下,将碳酸氧钠固体干燥至恒重,准确称取0.336g干燥的碳酸氢钠于锥形瓶中,加入50mL蒸馏水全部溶解,滴入待测的盐酸,当两者恰好完全反应时,消耗盐酸的体积20.00mL(该盐酸的密度近似等于lg·mL-1)。
①计算该盐酸的溶质质量分数为______ (结果用百分数表示,保留两位小数)。
②若上述测定过程中碳酸氢钠固体未经充分干燥,则测出盐酸的溶质质量分数将______ (填“偏大”“偏小”域“无影响”)。
(1)取溶质质量分数为4%的碳酸氢钠溶液50克,稀释成2%的溶液,需要加水
(2)将一定质量的碳酸氢钠溶液和稀盐酸混合,充分反应,有气体逸出。
①写出该反应的化学方程式
②探究反应后溶液除含有氯化钠,还有无剩余的反应物,某同:学取反应后的溶液倒不同方案进行如下实验。
【实验用品】pH试纸、稀盐酸、硝酸银溶液、氢氧化钠溶液、氧化铁粉未。
【进行实验】(提示:氯化银为不溶于水的白色物质)
| 实验方案 | A | B | C |
| 实验操作 | 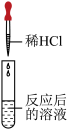 | 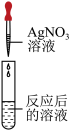 | 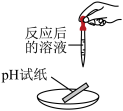 |
| 实验现象 | ______ | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH______7 |
| 实验结论 | 碳酸氢钠无剩余 | 稀盐酸有剩余 | 稀盐酸有剩余 |
b.某同学认为仅凭方案B的现象,不能得出反应后溶液中有稀盐酸剩余的结论,他的理由是
(3)用碳酸氢钠测定盐酸的溶质质量分数。在一定条件下,将碳酸氧钠固体干燥至恒重,准确称取0.336g干燥的碳酸氢钠于锥形瓶中,加入50mL蒸馏水全部溶解,滴入待测的盐酸,当两者恰好完全反应时,消耗盐酸的体积20.00mL(该盐酸的密度近似等于lg·mL-1)。
①计算该盐酸的溶质质量分数为
②若上述测定过程中碳酸氢钠固体未经充分干燥,则测出盐酸的溶质质量分数将
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】(1)如图所示是初中化学常见的实验装置图,请回答:

①实验室用B装置制取氧气,反应的化学方程式为______ 。
②若用F装置收集氧气,气体应从______ (填“a”或“b”)端进入。
③实验室制取并收集一瓶二氧化碳气体,应选用的装置为______ (填字母序号),在装入药品前应先______ ,该反应的化学方程式为______ 。
④实验室用该方法制取的二氧化碳常混杂一种气体杂质。若检验该杂质用到的试剂是______ 。
(2)皮蛋又称松花蛋,因其风味独特,深受人们喜爱。某兴趣小组在市场上获得了少许腌制皮蛋的原料。拿到实验室进行实验。将该固体混合物放于烧杯中,缓慢加入足量的蒸馏水,充分溶解后过滤,得到白色沉淀A和无色澄清滤液B。
【提出问题】①白色沉淀A是什么?
②无色滤液B中的溶质有哪些?
【查阅资料】腌制皮蛋的原料配方是少量NaCl、CaO和过量Na2CO3的固体混合物。
【理论推理】①白色沉淀A是CaCO3
②滤液B中含有Na2CO3、NaOH、NaCl三种溶质。
【实验验证】为证明滤液B中存在的三种溶质,同学们进行了如下实验。
【拓展提升】
①向步骤I中加入过量Ba(NO3)2溶液的目的是______ 。
②小妮同学认为若将步骤I中的Ba(NO3)2,溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质。你认为是否合理______ (填“合理”或“不合理”)。

①实验室用B装置制取氧气,反应的化学方程式为
②若用F装置收集氧气,气体应从
③实验室制取并收集一瓶二氧化碳气体,应选用的装置为
④实验室用该方法制取的二氧化碳常混杂一种气体杂质。若检验该杂质用到的试剂是
(2)皮蛋又称松花蛋,因其风味独特,深受人们喜爱。某兴趣小组在市场上获得了少许腌制皮蛋的原料。拿到实验室进行实验。将该固体混合物放于烧杯中,缓慢加入足量的蒸馏水,充分溶解后过滤,得到白色沉淀A和无色澄清滤液B。
【提出问题】①白色沉淀A是什么?
②无色滤液B中的溶质有哪些?
【查阅资料】腌制皮蛋的原料配方是少量NaCl、CaO和过量Na2CO3的固体混合物。
【理论推理】①白色沉淀A是CaCO3
②滤液B中含有Na2CO3、NaOH、NaCl三种溶质。
【实验验证】为证明滤液B中存在的三种溶质,同学们进行了如下实验。
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| Ⅰ | 取少量滤液B于试管中,加入过量的Ba(NO3)2溶液,过滤 | 滤液B中含有Na2CO3、NaOH、NaCl | |
| Ⅱ | 取少量步骤I中所得滤液于试管中,加入酚酞溶液 | ||
| Ⅲ | 另取少量步骤I中所得滤液于试管中,先加入足 量的稀硝酸,再加入 | 产生白色沉淀 |
①向步骤I中加入过量Ba(NO3)2溶液的目的是
②小妮同学认为若将步骤I中的Ba(NO3)2,溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质。你认为是否合理
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】酸、碱、盐是中学化学学习的重要内容,它们在生产、生活中具有广泛的用途。
(1)下列酸或碱的溶液在空气中敞口放置一段时间后,因变质而使溶液质量增加的是______。
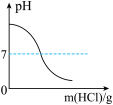
(2)向氢氧化钠中不断滴加稀盐酸溶液,反应的化学方程式为______ ,溶液pH与加入的氢氧化钠溶液质量的关系如图所示,若取反应过程中某一点时的溶液蒸干,得到纯净的NaCl固体,则该点时溶液的pH______ 7(填“<、>、=、≤或≥”)。
(3)为了除去氯化钠溶液中少量的Na2SO4、CaCl2、MgCl2杂质,某化学小组设计了如下实验步骤:
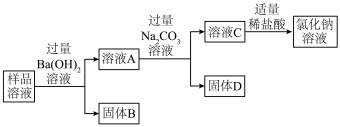
①上述过程中加入过量Ba(OH)2的目的是______ ;
Na2CO3共发生了______ 个反应;
②请设计实验证明溶液C中含有的杂质成分______ 。
(4)烧碱是一种重要的化工原料,广泛应用于肥皂,造纸等工业。
①工业上常用纯碱和石灰浆反应来制备烧碱,反应的化学方程式为______ ;
②工业上还可用电解饱和食盐水的方法制取烧碱,并得到氯气和氢气。若要制取8t烧碱,可同时得到多少吨氯气?______ 。
(1)下列酸或碱的溶液在空气中敞口放置一段时间后,因变质而使溶液质量增加的是______。
| A.H2SO4 | B.HCl | C.NaOH | D.Ca(OH)2 |
(2)向氢氧化钠中不断滴加稀盐酸溶液,反应的化学方程式为

(3)为了除去氯化钠溶液中少量的Na2SO4、CaCl2、MgCl2杂质,某化学小组设计了如下实验步骤:

①上述过程中加入过量Ba(OH)2的目的是
Na2CO3共发生了
②请设计实验证明溶液C中含有的杂质成分
(4)烧碱是一种重要的化工原料,广泛应用于肥皂,造纸等工业。
①工业上常用纯碱和石灰浆反应来制备烧碱,反应的化学方程式为
②工业上还可用电解饱和食盐水的方法制取烧碱,并得到氯气和氢气。若要制取8t烧碱,可同时得到多少吨氯气?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】科学家利用物质间转化创造新物质,服务于生产和生活。
(1)某工厂生产高锰酸钾的流程如下:
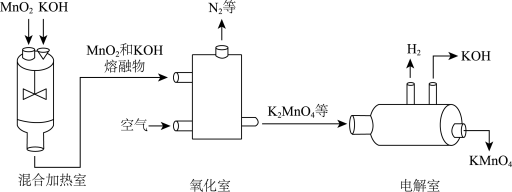
①“混合加热室”发生的主要是_______ (选填“物理变化”或“化学变化”);
②“电解室”反应中,反应前后化合价发生变化的元素有_______ (写元素符号)。
③生产流程中可循环利用的物质是_______ (写化学式)。
④写出氧化室中发生反应的化学方程式_______ 。
(2)A、B、C、D、E、F是初中化学常见的六种物质。A、B、D、E、F均由三种元素组成;A、B属于同类别的物质;固态C物质俗称干冰;A、E均合有人体中含量最多的金属元素;F可用于玻璃、造纸、纺织、洗涤剂的生产。部分反应物和产物已经略去,其中“一”表示两种物质间会反应,“→”表示一种物质会一步转化成另一种物质。
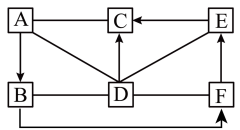
①E的化学式是_______ ,D溶液中一定含有的阳离子是_______ 。
②写出化学方程式A→B_______ 。
(1)某工厂生产高锰酸钾的流程如下:

①“混合加热室”发生的主要是
②“电解室”反应中,反应前后化合价发生变化的元素有
③生产流程中可循环利用的物质是
④写出氧化室中发生反应的化学方程式
(2)A、B、C、D、E、F是初中化学常见的六种物质。A、B、D、E、F均由三种元素组成;A、B属于同类别的物质;固态C物质俗称干冰;A、E均合有人体中含量最多的金属元素;F可用于玻璃、造纸、纺织、洗涤剂的生产。部分反应物和产物已经略去,其中“一”表示两种物质间会反应,“→”表示一种物质会一步转化成另一种物质。

①E的化学式是
②写出化学方程式A→B
您最近一年使用:0次



