金属材料在日常生活、工业上有广泛应用。
(1)铁是生活中应用最多的金属。铁易生锈,形成Fe2O3,Fe2O3属于______ (选填“酸”“碱”“盐”或“氧化物”),Fe2O3可用盐酸除去,写出反应的化学方程式______ 。
(2)铝具有良好的延展性。“延展性”属于______ (选填“物理性质”或“化学性质”)。冶炼铝时,先将冰晶石高温熔化,再将Al2O3加入,待Al2O3溶解后进行电解,该过程冰晶石可以看作______ (选填“溶质”或“溶剂”)。
(3)孔雀石(主要含Cu2(OH)2CO3)可以冶炼铜。孔雀石中元素含量最高的是______ ;将1 mol Cu2(OH)2CO3中的铜完全冶炼出来,可以得到单质铜______ mol。
(4)人类有规模使用金属单质的顺序是铜、铁、铝,请分析上述顺序的原因是______ (写出一条)。
(1)铁是生活中应用最多的金属。铁易生锈,形成Fe2O3,Fe2O3属于
(2)铝具有良好的延展性。“延展性”属于
(3)孔雀石(主要含Cu2(OH)2CO3)可以冶炼铜。孔雀石中元素含量最高的是
(4)人类有规模使用金属单质的顺序是铜、铁、铝,请分析上述顺序的原因是
2024·上海普陀·二模 查看更多[2]
更新时间:2024-05-03 16:58:23
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】《天工开物》中记载了许多我国古代劳动人民对物质的认识和应用的事例。如:硝石:凡硝刮扫取时,(墙中亦或迸出)入缸内水浸一宿,秽杂之物浮于面上,掠取去时,然后入釜,注水煎炼。硝化水干,倾于器内,经过一宿,即结成硝。
(1)硝石的主要成分是硝酸钾(KNO3),硝酸钾中氮元素的化合价是_______ ,硝酸钾中氮元素的质量分数为_______ (保留3位有效数字),硝石的主要成分还是一种_______ 肥。
(2)经过溶解的硝石,除去“秽杂之物”,实验室中可以通过_______ 的方法(填一种分离方法)。然后经过煎炼浓缩,冷却结晶的方法,可得到硝石晶体,此方法的依据是:_______ 。
(3)硝石也是制造黑火药的主要原料,其反应原理为: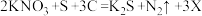 ,其中X的化学式是
,其中X的化学式是_______ 。
(1)硝石的主要成分是硝酸钾(KNO3),硝酸钾中氮元素的化合价是
(2)经过溶解的硝石,除去“秽杂之物”,实验室中可以通过
(3)硝石也是制造黑火药的主要原料,其反应原理为:
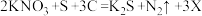 ,其中X的化学式是
,其中X的化学式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】(1)某物质R完全燃烧的化学方程式为:2R+3O2 2CO2+4H2O,R的相对分子质量等于
2CO2+4H2O,R的相对分子质量等于__ 。R中碳、氢两种元素质量比等于__ 。__ gR中氢元素质量和18g水氢元素质量相等。
(2)在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表。下列说法中不正确的是_____ 。
A 该反应为分解反应
B 甲、乙两种物质间参加反应的质量比为1:4
C 丙可能为该反应的催化剂
D 乙、丁两种物质间反应的质量比为7:5
 2CO2+4H2O,R的相对分子质量等于
2CO2+4H2O,R的相对分子质量等于(2)在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表。下列说法中不正确的是
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质质量/g | 8 | 32 | 5 | 4 |
| 反应后物质质量/g | 16 | 4 | x | 24 |
B 甲、乙两种物质间参加反应的质量比为1:4
C 丙可能为该反应的催化剂
D 乙、丁两种物质间反应的质量比为7:5
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】高铁酸钾(化学式:K2FeO4)是一种新型净水剂、消毒剂。工业制备高铁酸钾的反应流程如下图所示,回答问题。

(1)①反应中,基本反应类型是_____ ;
(2)写出②操作中发生反应的化学方程式_____ ;
(3)若要除去固体B中的杂质,可向其中加入足量的_____ ,充分反应后,过滤即可。

(1)①反应中,基本反应类型是
(2)写出②操作中发生反应的化学方程式
(3)若要除去固体B中的杂质,可向其中加入足量的
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属与我们生活息息相关。
(1)放置在空气中的铝制品表面会形成一层致密的氧化膜,该氧化膜的成分是_____ 。
(2)铸造硬币不需要 考虑金属的_____ (填字母序号)。
A 硬度B 抗腐蚀性C 导电性
(3)为了验证Fe、Cu、Ag的金属活动性顺序,设计如下实验。

实验①的化学方程式为_____ ,得到的结论是_____ 。为了达到实验目的,X溶液可以是_____ 。(填一种即可),对应的实验现象是_____ 。
(1)放置在空气中的铝制品表面会形成一层致密的氧化膜,该氧化膜的成分是
(2)铸造硬币
A 硬度B 抗腐蚀性C 导电性
(3)为了验证Fe、Cu、Ag的金属活动性顺序,设计如下实验。

实验①的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐1】用化学用语填空
(1)镁离子______ ;
(2)碘酒中的溶剂______ ;
(3)两个氨分子______ ;
(4)标出氧化铝中铝元素的化合价______ 。
(1)镁离子
(2)碘酒中的溶剂
(3)两个氨分子
(4)标出氧化铝中铝元素的化合价
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐2】自从2019年年末新冠肺炎在我国部分地区出现以来到2020年3月已经蔓延到全世界,过氧乙酸作为高效消毒剂被广泛使用。过氧乙酸在常温下是一种无色有刺激性气味的液体,易挥发,易溶于水和醋酸。它对呼吸道黏膜有刺激性,高含量的过氧乙酸溶液对皮肤有腐蚀性。一般商品过氧乙酸是40%的醋酸溶液,使用前通常先用蒸馏水等将其稀释,消毒时可用喷雾法消毒,也可将其配制成0.2%的水溶液洗手消毒。过氧乙酸不稳定,易分解生成无毒物质,若用喷雾法消毒,过氧乙酸在半小时内就可完全分解。
(1)在过氧乙酸的质量分数为40%的醋酸溶液中,溶质是________ ,溶剂是______ 。
(2)分别指出过氧乙酸的一点物理性质和一点化学性质。物理性质:______________________ ;化学性质:_____________________ 。
(3)100g过氧乙酸的质量分数为0.2%的洗手液中含过氧乙酸________ g。
(4)在新冠肺炎期间作为学生的我们应该怎么样做?___________________________ 。
(1)在过氧乙酸的质量分数为40%的醋酸溶液中,溶质是
(2)分别指出过氧乙酸的一点物理性质和一点化学性质。物理性质:
(3)100g过氧乙酸的质量分数为0.2%的洗手液中含过氧乙酸
(4)在新冠肺炎期间作为学生的我们应该怎么样做?
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】某合金的主要成分为Zn、Fe、Cu及这三种金属的少量氧化物。用该合金制成的机械零件废弃物可用于制取高纯度ZnO,其部分工艺流程如图所示。请回答:
【已知:Zn(OH)2固体不溶于水,但可溶于强碱并形成可溶性盐。】

(1)操作1的名称是____________________ 。
(2)滤渣I中一定有_____________________ 。
(3)调节pH可用NaOH,但不能过量,其原因是______________________ 。
(4)焙烧Zn(OH)2发生分解反应生成两种氧化物,该反应的化学方程式为____________________ 。
【已知:Zn(OH)2固体不溶于水,但可溶于强碱并形成可溶性盐。】

(1)操作1的名称是
(2)滤渣I中一定有
(3)调节pH可用NaOH,但不能过量,其原因是
(4)焙烧Zn(OH)2发生分解反应生成两种氧化物,该反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】硼(B)是制造火箭耐热合金的原料。镁还原法生产硼的主要工艺流程如下图。

(1)脱水炉中,硼酸( )发生分解反应生成
)发生分解反应生成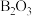 和
和 ,写出化学方程式
,写出化学方程式_______ 。
(2)还原炉中高温条件下发生的化学方程式为_______ 。
(3)酸煮罐中,加入盐酸的目的是_______ 。

(1)脱水炉中,硼酸(
 )发生分解反应生成
)发生分解反应生成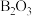 和
和 ,写出化学方程式
,写出化学方程式(2)还原炉中高温条件下发生的化学方程式为
(3)酸煮罐中,加入盐酸的目的是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐3】已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图:
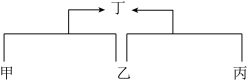
(1)常温下,若乙为胃酸的主要成分,甲为黑色粉末,则丙的化学式是______ ,甲与乙反应的化学方程式为______ ,此反应的基本反应类型为______ 。
(2)若丁为常见难溶性盐,乙可广泛用于玻璃、造纸和洗涤剂的生产,甲和丙是两种不同类别的物质,则:甲与乙反应的化学方程式为________ ,乙与丙反应的化学方程式为_______ 。

(1)常温下,若乙为胃酸的主要成分,甲为黑色粉末,则丙的化学式是
(2)若丁为常见难溶性盐,乙可广泛用于玻璃、造纸和洗涤剂的生产,甲和丙是两种不同类别的物质,则:甲与乙反应的化学方程式为
您最近一年使用:0次




