物质除杂是化学实验中经常遇到的问题。
【方法探究】为除去二氧化碳气体中混有的少量一氧化碳,小明设计了三种方案。
上述方案中有两个是合理的,写出合理方案中任意一个反应的化学方程式_______ ;
【方法提炼】上述两种合理方案体现了物质除杂的不同思路:
思路一:将杂质直接转化为所需物质;
思路二:将所需物质转化为中间物质,再将中间物质转化为所需物质。
【方法运用】
运用思路一:除去氯化镁粉末中混有的少量氯化钡,先加足量的水溶解,再向溶液中加入适量的_______ 溶液,过滤、蒸发,即得氯化镁固体。
运用思路二:除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾。
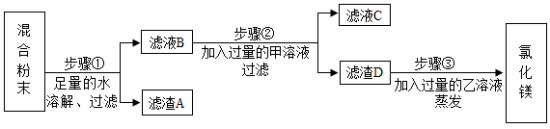
步骤①中反应的化学方程式是_________ ,滤液B中一定含有的溶质是 ________ ;
步骤②中反应的化学方程式是_________ ,滤液C中一定含有的阴离子是________ ;
步骤③中乙溶液是________ (填化学式)溶液。
【方法探究】为除去二氧化碳气体中混有的少量一氧化碳,小明设计了三种方案。
| 实验方案 | |
| 方案A |  |
| 方案B | 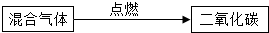 |
| 方案C | 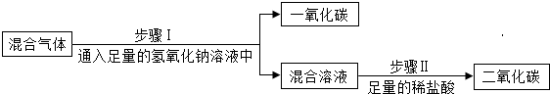 |
【方法提炼】上述两种合理方案体现了物质除杂的不同思路:
思路一:将杂质直接转化为所需物质;
思路二:将所需物质转化为中间物质,再将中间物质转化为所需物质。
【方法运用】
运用思路一:除去氯化镁粉末中混有的少量氯化钡,先加足量的水溶解,再向溶液中加入适量的
运用思路二:除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾。

步骤①中反应的化学方程式是
步骤②中反应的化学方程式是
步骤③中乙溶液是
2014·湖北宜昌·中考真题 查看更多[3]
(已下线)2014年初中毕业升学考试(湖北宜昌卷)化学(已下线)【万唯原创】2015年陕西省中考化学试题研究卷九年级练习册模块五-专题17(已下线)【万唯原创】2015年陕西省中考化学面对面卷(人教版)讲解册模块五
更新时间:2016-11-28 12:20:02
|
相似题推荐
【推荐1】阅读资料并回答问题。
钠【Na】是一种银白色金属,质软而可用小刀切割,密度为0.97g/cm3,熔点97.81°C,沸点882.9°C。钠刚切开时,新切面有银白色光泽,但在空气中马上氧化转变为暗灰色。钠能与水发生剧烈反应生成氢氧化钠和氢气,量大时发生爆炸。钠还能在二氧化碳中燃烧,生成纯碱和另一种气态氧化物。金属钠往往浸放于液体石蜡、矿物油和苯系物中密封保存,钠是人体中一种重要元素,是泪水的组成成分。
根据文章内容完成下列问题:
(1)保存钠的方法是__________ 。
(2)将钠放入水中,能观察到的现象有____________ 。
(3)将钠放在二氧化碳中燃烧的化学反应符号表达式是___________ 。
钠【Na】是一种银白色金属,质软而可用小刀切割,密度为0.97g/cm3,熔点97.81°C,沸点882.9°C。钠刚切开时,新切面有银白色光泽,但在空气中马上氧化转变为暗灰色。钠能与水发生剧烈反应生成氢氧化钠和氢气,量大时发生爆炸。钠还能在二氧化碳中燃烧,生成纯碱和另一种气态氧化物。金属钠往往浸放于液体石蜡、矿物油和苯系物中密封保存,钠是人体中一种重要元素,是泪水的组成成分。
根据文章内容完成下列问题:
(1)保存钠的方法是
(2)将钠放入水中,能观察到的现象有
(3)将钠放在二氧化碳中燃烧的化学反应符号表达式是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】某化学小组在实验室中进行酸、碱、盐化学性质的实验:
〖进行实验〗
实验一:
(1)取一根表面生锈的铁钉放于一只试管中(铁锈的主要成分是三氧化二铁),逐滴滴入稀盐酸,并轻轻振荡,观察到:铁钉表面的铁锈渐渐消失,变得光亮,溶液变为黄色。发生的化学反应方程式为_____________ 。
(2)铁钉光亮后取出,放于另一只试管中,继续滴加稀盐酸,观察到的现象是:____________ 。
实验二:
(1)另取一支试管加入约两毫升硫酸铜溶液,再加入一些氢氧化钠溶液,然后加入适量的稀硫酸,这个过程观察到的现象是:_____________ 。
(2)最后向试管中滴加适量氯化钡溶液,产生白色沉淀,写出产生白色沉淀的化学方程式(一个即可):______________ 。
〖实验总结〗
化学小组的同学根据以上二个实验对酸、碱、盐化学性质进行了总结,以下结论与以上实验无关的是:_____________ 。
A.酸能与某些金属反应
B.酸能与某些金属氧化物反应
C.某些盐之间可以发生反应
D.碱能与某些盐反应
E.酸能与碱反应
F.酸能与某些盐反应
G.盐能与某些金属反应
〖处理药品〗
实验结束后,将实验一、实验二试管中的废液全部倒入一只空烧杯中,混合后,加入适量的氢氧化钠溶液处理,经处理后溶液中一定存在的溶质是___________ 。
〖进行实验〗
实验一:
(1)取一根表面生锈的铁钉放于一只试管中(铁锈的主要成分是三氧化二铁),逐滴滴入稀盐酸,并轻轻振荡,观察到:铁钉表面的铁锈渐渐消失,变得光亮,溶液变为黄色。发生的化学反应方程式为
(2)铁钉光亮后取出,放于另一只试管中,继续滴加稀盐酸,观察到的现象是:
实验二:
(1)另取一支试管加入约两毫升硫酸铜溶液,再加入一些氢氧化钠溶液,然后加入适量的稀硫酸,这个过程观察到的现象是:
(2)最后向试管中滴加适量氯化钡溶液,产生白色沉淀,写出产生白色沉淀的化学方程式(一个即可):
〖实验总结〗
化学小组的同学根据以上二个实验对酸、碱、盐化学性质进行了总结,以下结论与以上实验无关的是:
A.酸能与某些金属反应
B.酸能与某些金属氧化物反应
C.某些盐之间可以发生反应
D.碱能与某些盐反应
E.酸能与碱反应
F.酸能与某些盐反应
G.盐能与某些金属反应
〖处理药品〗
实验结束后,将实验一、实验二试管中的废液全部倒入一只空烧杯中,混合后,加入适量的氢氧化钠溶液处理,经处理后溶液中一定存在的溶质是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】海洋中值含着丰富的资源,海洋资源开发前最十分广阔。
(1)海水中含有较多的硫酸钠。硫酸钠是制造纸浆、燃料稀释剂、医药用品等的重要原料,某硫酸钠样品中含有少量硫酸钙、氯化镁,实验室进行提纯的流程如:图1:
①用氢氧化钠和碳酸钠除杂时,反应的化学方程式分别为______ 、______ 。
②氢氧化钠和碳酸钠如果添加过量了,可在滤液中加入适量______ 溶液除去。
③“后续处理”的主要操作时蒸发,为了获得纯净的硫酸钠,应蒸发至______ (填序号)。
A.完全蒸干时停止加热
B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
④已知硫酸钠的溶解度随温度变化的曲线如图所示。40℃时,硫酸钠的溶解度为______ g。将该饱和溶液升高温度至90℃,观察到的现象是______ 。______ 。步骤Ⅲ中反应的化学方程式是______
(3)采用氨碱法生产纯碱,主要流程如图4:______
②从步骤Ⅱ过滤得到碳酸氢钠,近日,一则《重大突破! 癌细胞,竟被中国医生用小苏打“饿”死了》的新闻在网络上热传:研究人员用小苏打用来去除肿瘤内的氢离子,就可破坏乳酸根和氢离子的协同作用,从而快速有效地杀死处于葡萄糖饥饿或缺乏的肿瘤细胞,请你用一个化学反应证明该研究成果的科学性______ 。当然,科学原理如何转换到临床上来,还会是一个很艰难漫长的过程。
(1)海水中含有较多的硫酸钠。硫酸钠是制造纸浆、燃料稀释剂、医药用品等的重要原料,某硫酸钠样品中含有少量硫酸钙、氯化镁,实验室进行提纯的流程如:图1:

①用氢氧化钠和碳酸钠除杂时,反应的化学方程式分别为
②氢氧化钠和碳酸钠如果添加过量了,可在滤液中加入适量
③“后续处理”的主要操作时蒸发,为了获得纯净的硫酸钠,应蒸发至
A.完全蒸干时停止加热
B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
④已知硫酸钠的溶解度随温度变化的曲线如图所示。40℃时,硫酸钠的溶解度为


(3)采用氨碱法生产纯碱,主要流程如图4:

②从步骤Ⅱ过滤得到碳酸氢钠,近日,一则《重大突破! 癌细胞,竟被中国医生用小苏打“饿”死了》的新闻在网络上热传:研究人员用小苏打用来去除肿瘤内的氢离子,就可破坏乳酸根和氢离子的协同作用,从而快速有效地杀死处于葡萄糖饥饿或缺乏的肿瘤细胞,请你用一个化学反应证明该研究成果的科学性
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐1】A、B、C、D、E、F是初中化学常见的六种物质,已知A是黑色固体单质。

(1)A的化学式_____ ,E的化学式 _____ 。
(2)写出下列反应的化学方程式:反应②_____ ,反应④ _____ 。
(3)反应③的基本反应类型是_____ 反应。
(4)写出B物质的一种用途_____ 。

(1)A的化学式
(2)写出下列反应的化学方程式:反应②
(3)反应③的基本反应类型是
(4)写出B物质的一种用途
您最近一年使用:0次
【推荐2】化学实验活动课上,同学们进行了如图所示的实验。

(1)B试管内发生反应的化学方程式是______ 。
(2)说明实验二中氢氧化钙与稀盐酸发生反应的现象是______ 。
(3)实验三中试管内发生反应的化学方程式是______ ,该试管内发生反应的现象是______ 。
(4)实验结束后,同学们将A、B、C三支试管中的物质倒入同一个洁净的烧杯内,得到无色澄清溶液。取该溶液少量于试管中,加入锌粉,有气泡产生。这种滤液会对水体产生污染,需要加入过量的试剂处理后再排放,下列提供的试剂有一种能满足要求,该试剂为______ (填字母)。
A 生石灰 B 熟石灰 C 石灰石 D 稀硫酸
(5)某金属粉末可能由镁、锌、铁、铝、银中的一种或几种组成。取该样品2.4g,向其中加入100g一定溶质量分数的稀盐酸,恰好完全反应,生成0.2g氢气,得到无色溶液,固体无剩余。下列说法不正确的是______ (填序号)
A 根据恰好完全反应得到无色溶液的信息,该金属粉末中一定不含有铁和银
B 由产生0.2g氢气,利用氢元素守恒可以计算出反应消耗了7.3gHCl,进而求出加入的稀盐酸溶质质量分数为14.6%
C 所得溶液中溶质为氯化物,其质量可以表示为m氯元素+m金属,经过计算其质量为9.5g
D 样品中一定含有镁

(1)B试管内发生反应的化学方程式是
(2)说明实验二中氢氧化钙与稀盐酸发生反应的现象是
(3)实验三中试管内发生反应的化学方程式是
(4)实验结束后,同学们将A、B、C三支试管中的物质倒入同一个洁净的烧杯内,得到无色澄清溶液。取该溶液少量于试管中,加入锌粉,有气泡产生。这种滤液会对水体产生污染,需要加入过量的试剂处理后再排放,下列提供的试剂有一种能满足要求,该试剂为
A 生石灰 B 熟石灰 C 石灰石 D 稀硫酸
(5)某金属粉末可能由镁、锌、铁、铝、银中的一种或几种组成。取该样品2.4g,向其中加入100g一定溶质量分数的稀盐酸,恰好完全反应,生成0.2g氢气,得到无色溶液,固体无剩余。下列说法不正确的是
A 根据恰好完全反应得到无色溶液的信息,该金属粉末中一定不含有铁和银
B 由产生0.2g氢气,利用氢元素守恒可以计算出反应消耗了7.3gHCl,进而求出加入的稀盐酸溶质质量分数为14.6%
C 所得溶液中溶质为氯化物,其质量可以表示为m氯元素+m金属,经过计算其质量为9.5g
D 样品中一定含有镁
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C、D和甲、乙均为初中化学中常见的物质,物质间存在着如图所示的相互转化关系(部分生成物未标出).请回答下列问题:

(1)若A为气体氧化物,与溶液甲和溶液乙反应均生成盐和水.则A的化学式为______ ;取溶液D少量于试管中,加入碳酸钠溶液,有白色沉淀生成,则溶液D中溶质为______ (写化学式);③反应的化学方程式为______ .
(2)若向一定质量的碳酸钠溶液中加入足量的氯化钙溶液,所得沉淀质量等于原碳酸钠溶液质量的 ,则原碳酸钠溶液中溶质的质量分数为
,则原碳酸钠溶液中溶质的质量分数为______ .

(1)若A为气体氧化物,与溶液甲和溶液乙反应均生成盐和水.则A的化学式为
(2)若向一定质量的碳酸钠溶液中加入足量的氯化钙溶液,所得沉淀质量等于原碳酸钠溶液质量的
 ,则原碳酸钠溶液中溶质的质量分数为
,则原碳酸钠溶液中溶质的质量分数为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐1】FeCl3可用作催化剂和外伤止血剂。某实验兴趣小组利用FeCl3腐蚀电路铜板后的溶液(主要成分为FeCl2、CuCl2)进行了氯化铁回收实验。

实验一:(如图1)
(1)写出步骤①中发生的化学方程式_________________ ,此反应的基本类型是 _____________ 。
(2)步骤②中的操作a名称是___________ ;步骤③中加入稀盐酸的目的是 ______________ 。
实验二:该实验小组同学通过查阅资料,又进行了另一种尝试。
【阅读资料】不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离。
如表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
(3)如图2,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式__________________ ;你认为步骤b调节溶液的pH到 _______ (数值范围)比较合适。
(4)该实验需要用pH试纸测量溶液的pH,请将pH试纸的使用方法补充完整:________________ ,把试纸显示的颜色与标准比色卡比较,读出该溶液的pH。
(5)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用_____ (用字母表示)最合理。
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸

实验一:(如图1)
(1)写出步骤①中发生的化学方程式
(2)步骤②中的操作a名称是
实验二:该实验小组同学通过查阅资料,又进行了另一种尝试。
【阅读资料】不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离。
如表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 4.7 |
| 沉淀完全的pH | 3.2 | 6.7 |
(3)如图2,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式
(4)该实验需要用pH试纸测量溶液的pH,请将pH试纸的使用方法补充完整:
(5)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
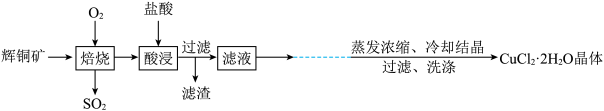
【推荐2】CuCl2是一种广泛用于生产颜料、木材防腐剂等的化工产品。工业上以辉铜矿(主要含有Cu2S和一些不溶性杂质)为原料制备CuCl2·2H2O晶体的主要工艺流程如下:
请回答下列问题:
(1)焙烧中生成黑色固体,反应的化学方程式为_____ 。
(2)酸浸后要过滤,实验室进行该操作需要的玻璃仪器有漏斗、玻璃棒和_____ 。
(3)酸浸中,为加快反应速率,以下措施无法达到目的是_____ (填字母序号)。
a、延长酸浸时间
b、将辉铜矿粉碎
c、适当增加盐酸浓度
(4)色光度是产品质量指标之一,合格的CuCl2·2H2O晶体色光度范围为-0.5~0.5,反应过程溶液pH对产率、色光度的影响如图2所示综合考虑制备时应控制pH的较合理范围是_____ 。

(5)CuCl2·2H2O晶体可用氯化铜饱和溶液洗涤而不用蒸馏水的原因是_____ 。

请回答下列问题:
(1)焙烧中生成黑色固体,反应的化学方程式为
(2)酸浸后要过滤,实验室进行该操作需要的玻璃仪器有漏斗、玻璃棒和
(3)酸浸中,为加快反应速率,以下措施无法达到目的是
a、延长酸浸时间
b、将辉铜矿粉碎
c、适当增加盐酸浓度
(4)色光度是产品质量指标之一,合格的CuCl2·2H2O晶体色光度范围为-0.5~0.5,反应过程溶液pH对产率、色光度的影响如图2所示综合考虑制备时应控制pH的较合理范围是

(5)CuCl2·2H2O晶体可用氯化铜饱和溶液洗涤而不用蒸馏水的原因是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】化肥对粮食增产有着非常重要的贡献
(1)硫酸钾和硝酸钾是常见的两种化肥,其中属于复合肥的是__________ ,请简述区分硫酸钾和硝酸钾的实验操作、现象及结论_____________________________
(2)硫酸铵是一种速效氮素化学肥料,小雪在实验室发现一瓶(NH4)2SO4溶液,设计了以下实验测定该溶液中溶质的质量分数
①取出10.0g(NH4)2SO4溶液置于一个洁净的烧杯中。
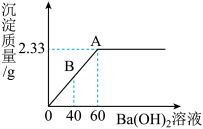
②用胶头滴管向烧杯中滴加Ba(OH)2溶液直至不再产生沉淀为止。现象:有白色沉淀产生,还看到有能使湿润的红色石蕊试纸变_________ 色的气体生成。
③过滤:玻璃棒的作用为____________ ; B点时滤液中溶质为__________ (写化学式)。
④取沉淀物于蒸发皿中加热蒸干,在充分干燥之后称重。根据得到沉淀物的质量与加入Ba(OH)2溶液质量关系计算硫酸铵溶液中溶质质量分数___________ 。(写出计算过程,计算结果精确至0.1%)
(1)硫酸钾和硝酸钾是常见的两种化肥,其中属于复合肥的是
(2)硫酸铵是一种速效氮素化学肥料,小雪在实验室发现一瓶(NH4)2SO4溶液,设计了以下实验测定该溶液中溶质的质量分数
①取出10.0g(NH4)2SO4溶液置于一个洁净的烧杯中。
②用胶头滴管向烧杯中滴加Ba(OH)2溶液直至不再产生沉淀为止。现象:有白色沉淀产生,还看到有能使湿润的红色石蕊试纸变
③过滤:玻璃棒的作用为
④取沉淀物于蒸发皿中加热蒸干,在充分干燥之后称重。根据得到沉淀物的质量与加入Ba(OH)2溶液质量关系计算硫酸铵溶液中溶质质量分数

您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
真题
解题方法
【推荐1】已知A~G是初中化学常见的物质,A、B、C、E、F属于不同类别的物质,G溶液呈 黄色,A与C反应产生白色沉淀(微溶物不列为沉淀),它们相互间发生反应或转化 的关系如图所示(“﹣”表示两种物质间能发生反应,“→”表示两种物质间的转化 关系,部分反应物、生成物和反应条件已经略去).

(1)A、F的化学式分别为_____ ,_____ ;
(2)B与E反应的化学方程式为_____ ,其反应的基本反应类型为_____ ;G→D的化学方程式为_____ ;
(3)A→D反应的实验现象为_____ .

(1)A、F的化学式分别为
(2)B与E反应的化学方程式为
(3)A→D反应的实验现象为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
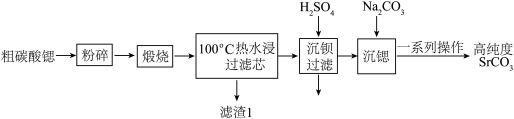
【推荐2】碳酸锶(SrCO3)广泛应用于生产锶铁氧体磁性材料,现以粗碳酸锶(含杂质BaCO3、MgCO3、CaCO3)为原料制备高纯碳酸锶的工艺流程如下:
ⅱ、某些金属氧化物与水发生化合反应的条件是生成物为可溶性碱。
iii、可能用到某些物质的溶解度见下表:(g/100g水)
回答下列问题:
(1)将粗碳酸锶“粉碎”的目的是______ 。
(2)“煅烧”粗碳酸锶时,碳酸锶发生反应的化学方程式为______ 。
(3)滤渣1的主要成分是______ (写化学式)。
(4)流程中需用温度为100℃热水浸的目的是______ 。
(5)“沉钡”过程中:
①写出含锶化合物与H2SO4反应的化学方程式______ 。
②下表为H2SO4溶液的加入量对溶液中Sr2+和Ba2+含量的影响情况:
根据表中的数据回答,实际生产中加入过量20%的H2SO4溶液较为合适,原因是______ 。
(6)“沉锶”反应后的“一系列操作”为______ 。
ⅱ、某些金属氧化物与水发生化合反应的条件是生成物为可溶性碱。
iii、可能用到某些物质的溶解度见下表:(g/100g水)
温度/℃ | 20 | 40 | 60 | 80 | 100 |
Sr(OH)2 | 0.81 | 1.77 | 3.68 | 8.30 | 27.9 |
Ca(OH)2 | 0.173 | 0.141 | 0.121 | 0.094 | 0.076 |
(1)将粗碳酸锶“粉碎”的目的是
(2)“煅烧”粗碳酸锶时,碳酸锶发生反应的化学方程式为
(3)滤渣1的主要成分是
(4)流程中需用温度为100℃热水浸的目的是
(5)“沉钡”过程中:
①写出含锶化合物与H2SO4反应的化学方程式
②下表为H2SO4溶液的加入量对溶液中Sr2+和Ba2+含量的影响情况:
H2SO4溶液加入量 | 过量10% | 过量20% | 过量30% |
Sr2+/(g/L) | 89.86 | 89.57 | 89.23 |
Ba2+/(g/L) | 0.21 | 0.13 | 0.11 |
(6)“沉锶”反应后的“一系列操作”为
您最近一年使用:0次




