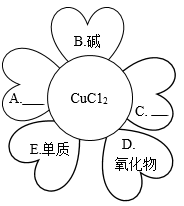
某种粗盐水中有少量杂质Na2SO4,小林用这种粗盐水制取纯净的氯化钠溶液,设计了如图步骤:________________ 。
(2)加入过量碳酸钠溶液的目的是什么?________________ 。
(3)有同学提出可用稀硝酸代替稀盐酸,请给出你的评价并解释原因________________ 。
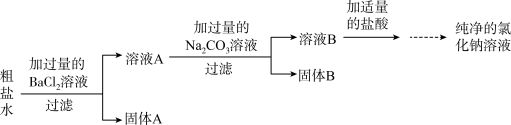
(2)加入过量碳酸钠溶液的目的是什么?
(3)有同学提出可用稀硝酸代替稀盐酸,请给出你的评价并解释原因
更新时间:2024-04-22 15:30:44
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】“宏观-微观-符号”三重表征是体现化学学科特征的思维方法。如图是几种元素的粒子结构示意图或元素的信息,请回答:
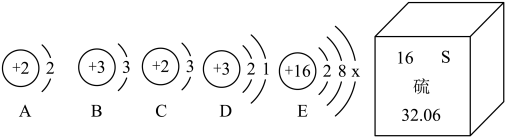
(1)图E为硫原子结构示意图,x=_______ 。
(2)氦-1、氦-2、氦-3,它们都是同一种元素的原因是_______ 。我国“嫦娥五号”探测器取回土镶含有丰富的氦-3,它是由一个中子和两个质子构成的,其原子结构示意图为图中_______ 。(选A、B、C、D中一项)
(3)工业上,可以利用甲烷获得氢气,其反应的微观示意图如图:
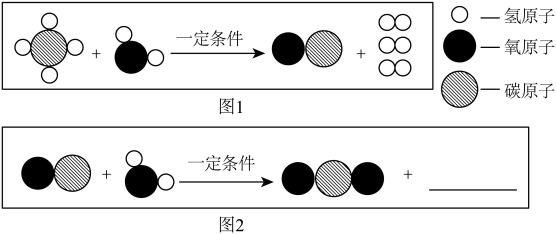
①图1所示反应的化学方程式为_______ 。
②补全图2横线处相应微粒的图示_______ 。
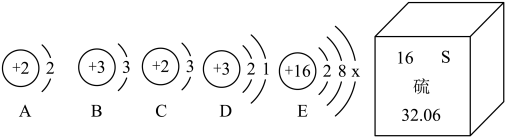
(1)图E为硫原子结构示意图,x=
(2)氦-1、氦-2、氦-3,它们都是同一种元素的原因是
(3)工业上,可以利用甲烷获得氢气,其反应的微观示意图如图:

①图1所示反应的化学方程式为
②补全图2横线处相应微粒的图示
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】写出下列反应的文字或符号表达式并回答问题。
(1)硫在空气中燃烧:______ 。
(2)铁丝在氧气里燃烧______ 。为了防止______ ,应当在瓶内装少量水。
(3)在常温下过氧化钠跟二氧化碳 反应生成碳酸钠和氧气______ 。
(1)硫在空气中燃烧:
(2)铁丝在氧气里燃烧
(3)在常温下
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】分析下表中KCl和KNO3的溶解度数据,回答相关问题。
(1)在KCl和KNO3中,溶解度受温度影响较大的是_____ ;
(2)欲将55g KNO3固体完全溶解,至少需要_____ g 60℃的水;
(3)KNO3溶液中含有少量KCl,提纯KNO3晶体,宜采用的结晶方法是____ ,若要完全提纯KNO3 晶体,采用的化学方法是向混合溶液中加入适量的某种溶液,充分反应后过滤,再对滤液蒸发即可,发生反应的化学方程式为____ 。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)欲将55g KNO3固体完全溶解,至少需要
(3)KNO3溶液中含有少量KCl,提纯KNO3晶体,宜采用的结晶方法是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】粗盐中除含有泥沙等不溶性杂质外,还含有少量的MgCl2、CaCl2等可溶性杂质;为了得到较纯净的氯化钠,除去泥沙的“精盐”又作了如下处理(假定杂质只有MgCl2、CaCl2两种)注:反应中所加试剂均过量。
(1)实验中加入Na2CO3的目的是:_____ 。
(2)若实验过程中不考虑损耗,最终得到的NaCl固体的质量将_____ (填“大于”“小于”或“等于”)原精盐中NaCl固体的质量。
(3)过滤后滤液中的杂质有哪些?_____ 。

(1)实验中加入Na2CO3的目的是:
(2)若实验过程中不考虑损耗,最终得到的NaCl固体的质量将
(3)过滤后滤液中的杂质有哪些?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】金属在生产、生活和社会发展中的应用较为广泛。
(1)考古工作者在三星堆遗址新发现6座三星堆文化“祭祀坑”,发掘并出土了巨型青铜面具。
①青铜与纯铜相比,其硬度更________ (填“大”或“小”),青铜中的铜以________ (填“单质”或“化合物”)形式存在。
②人类最早进入青铜器时代,继而进入铁器时代,而人类利用铝的历史仅100多年,这个先后顺序跟下列因素有关的是________ (填序号)
A.金属的活动性顺序
B.金属的导电、导热性
C.金属的延展性
D.地壳中金属元素的含量
(2)在天平两边的烧杯中分别盛有同质量、同溶质质量分数的稀硫酸,天平平衡,再向两烧杯中分别加入相同质量的镁和铁,充分反应后,若天平平衡,则反应物中一定有剩余的物质________ 。
(3)有一包白色固体粉末可能由 、
、 、
、 、
、 、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:
、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:
①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;
②另取少量白色粉末加入到适量的水中,出现白色浑浊,静置后,上层清液无色;
③小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生。
由以上实验可推断:
这包白色固体中肯定存在________ ,肯定不存在________ ;写出②中出现白色浑浊的化学方程式________ 。
(1)考古工作者在三星堆遗址新发现6座三星堆文化“祭祀坑”,发掘并出土了巨型青铜面具。
①青铜与纯铜相比,其硬度更
②人类最早进入青铜器时代,继而进入铁器时代,而人类利用铝的历史仅100多年,这个先后顺序跟下列因素有关的是
A.金属的活动性顺序
B.金属的导电、导热性
C.金属的延展性
D.地壳中金属元素的含量
(2)在天平两边的烧杯中分别盛有同质量、同溶质质量分数的稀硫酸,天平平衡,再向两烧杯中分别加入相同质量的镁和铁,充分反应后,若天平平衡,则反应物中一定有剩余的物质
(3)有一包白色固体粉末可能由
 、
、 、
、 、
、 、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:
、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;
②另取少量白色粉末加入到适量的水中,出现白色浑浊,静置后,上层清液无色;
③小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生。
由以上实验可推断:
这包白色固体中肯定存在
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】科学实验中要研究纯净物的组成、结构、性质等,常常需要把混合物进行除杂、分离和提纯等。
(1)除去二氧化碳气体中的水蒸气,可选用的试剂是______________ (写名称)。
(2)为了将氯化钠和氯化钙两种固体混合物分离,设计了下列实验方案:

试回答下列问题:
①操作②中加入过量Na2CO3的目的是_______________ ,发生反应的化学方程式为 __________ 。
②甲同学认为,上述所得的NaCl固体不纯,要得到较纯净的NaCl固体,需增加一步实验,他的做法是________ 。
(1)除去二氧化碳气体中的水蒸气,可选用的试剂是
(2)为了将氯化钠和氯化钙两种固体混合物分离,设计了下列实验方案:

试回答下列问题:
①操作②中加入过量Na2CO3的目的是
②甲同学认为,上述所得的NaCl固体不纯,要得到较纯净的NaCl固体,需增加一步实验,他的做法是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】对含有杂质氯化镁、氯化钙、硫酸钠的某粗盐进行提纯,某同学设计了如下的实验步骤:

(1)加入过量碳酸钠的作用是________ 。
(2)写出步骤⑤发生反应的化学反应方程式(任写其中一个)。
(3)步骤⑥中玻璃棒的作用________ 。

(1)加入过量碳酸钠的作用是
(2)写出步骤⑤发生反应的化学反应方程式(任写其中一个)。
(3)步骤⑥中玻璃棒的作用
您最近一年使用:0次
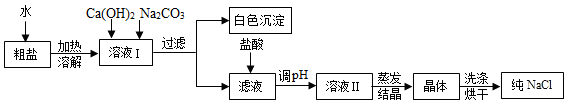
【推荐3】NaC1是日常生活的必需品,也是重要的化工原料。工业上用粗盐(含有少量Ca2+、Mg2+、 等杂质离子)提纯NaCl,其流程如下图所示。请回答下列问题。
等杂质离子)提纯NaCl,其流程如下图所示。请回答下列问题。

(1)操作1加水溶解的过程中,为了加快溶解,可以采取的措施是__________ (举一例即可)。操作2的名称是__________ 。
(2)在a处添加过量的试剂①饱和Na2CO3溶液、②NaOH溶液、③BaCl2溶液,以除去粗盐中的Ca2+、Mg2+、 离子,试剂的添加顺序为:
离子,试剂的添加顺序为:___________ (填序号)。
(3)在溶液I中加入稀盐酸,其目的是__________ 。
(4)NaC1是无机化工生产之母,通电电解饱和氯化钠溶液可以得到氢氧化钠、氢气和氯气(Cl2),该反应的化学方程式是________ 。
 等杂质离子)提纯NaCl,其流程如下图所示。请回答下列问题。
等杂质离子)提纯NaCl,其流程如下图所示。请回答下列问题。
(1)操作1加水溶解的过程中,为了加快溶解,可以采取的措施是
(2)在a处添加过量的试剂①饱和Na2CO3溶液、②NaOH溶液、③BaCl2溶液,以除去粗盐中的Ca2+、Mg2+、
 离子,试剂的添加顺序为:
离子,试剂的添加顺序为:(3)在溶液I中加入稀盐酸,其目的是
(4)NaC1是无机化工生产之母,通电电解饱和氯化钠溶液可以得到氢氧化钠、氢气和氯气(Cl2),该反应的化学方程式是
您最近一年使用:0次