考古发掘与研究表明:湖北省铜绿山古铜矿遗址是迄今已发掘的古铜矿中开采规模最大、采冶时间最长、冶炼水平最高、采冶链最完整、文化内涵最丰富的--处文化遗产。
Ⅰ.铜矿的开采与冶炼
(1)铜绿山主要矿石有孔雀石[主要成分:Cu2(OH)2CO3]和赤铜矿(主要成分:Cu2O),还存在少量自然铜(主要成分:Cu)。自然铜能在地壳中少量存在的原因是______ 。
(2)研究发现,铜绿山古铜矿采用了多种冶铜技术。例如,先破碎铜矿石至一定粒度才入炉冶炼,目的是______ 。
Ⅱ.青铜的铸造与锈蚀
(3)纯铜制作的器皿使用时可能锈蚀成铜绿[主要成分:Cu2(OH)2CO3],由其化学式推测,下图试管中的铜片最易生锈的是______ (填字母)。______ 。但是,在含氯离子的地下土壤中,青铜表面会产生氯化亚铜(CuCl),氯化亚铜再进一步与地下水、地下氧(O2)作用生成碱式氯化铜[Cu2(OH)3Cl]和氯化氢,周而复始地腐蚀青铜器形成粉状锈,写出该反应的化学方程式______ 。
Ⅲ.青铜器的修复与维护
(5)青铜器表面的粉状锈可用锌粉转化法去除。用乙醇和锌粉调成胶状物涂抹在文物表层,将表面的锈迹修复成铜,此过程利用的化学原理是______ 。修复后的青铜器表面需用蒸馏水不断地冲洗,去除氯离子,检验青铜器表面的氯离子完全除去的方法是______ 。
(6)存放修复完成的青铜器时,操作合理的是______ (填字母)。
a.青铜器表面涂缓蚀剂
b.用自来水清洗青铜器表面的灰尘
c.搬运青铜器时戴棉质手套
d.保存在恒温、干燥、充氮气的储藏柜中
Ⅰ.铜矿的开采与冶炼
(1)铜绿山主要矿石有孔雀石[主要成分:Cu2(OH)2CO3]和赤铜矿(主要成分:Cu2O),还存在少量自然铜(主要成分:Cu)。自然铜能在地壳中少量存在的原因是
(2)研究发现,铜绿山古铜矿采用了多种冶铜技术。例如,先破碎铜矿石至一定粒度才入炉冶炼,目的是
Ⅱ.青铜的铸造与锈蚀
(3)纯铜制作的器皿使用时可能锈蚀成铜绿[主要成分:Cu2(OH)2CO3],由其化学式推测,下图试管中的铜片最易生锈的是
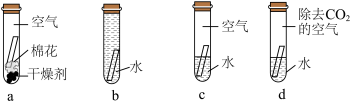
Ⅲ.青铜器的修复与维护
(5)青铜器表面的粉状锈可用锌粉转化法去除。用乙醇和锌粉调成胶状物涂抹在文物表层,将表面的锈迹修复成铜,此过程利用的化学原理是
(6)存放修复完成的青铜器时,操作合理的是
a.青铜器表面涂缓蚀剂
b.用自来水清洗青铜器表面的灰尘
c.搬运青铜器时戴棉质手套
d.保存在恒温、干燥、充氮气的储藏柜中
2024·江苏无锡·一模 查看更多[3]
江苏省无锡市梁溪区2024年中考一模考试理科综合题-初中化学(已下线)专题11 实验探究-【好题汇编】2024年中考化学一模试题分类汇编(江苏专用)(已下线)专题08 金属和金属材料-【好题汇编】2024年中考化学一模试题分类汇编(江苏专用)
更新时间:2024-05-08 13:28:25
|
相似题推荐
综合应用题
|
较难
(0.4)
解题方法
【推荐1】对于金属材料,我们应该从多角度了解。
Ⅰ.金属冶炼
(1)《天工开物》中记载了炼锡的场景:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化。
①鼓入足量空气的目的是_______ ,从而提高炉温。
②“点铅勾锡”是炼锡的关键步骤,加铅能使锡较易熔化流出,其原因是_______ 。
Ⅱ.金属的活动性
(2)为探究锌、铁、铜三种金属的活动性及它们和氢元素的位置关系,小明设计了如下实验:
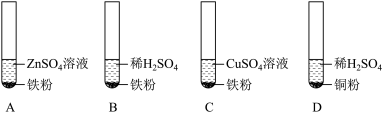
①试管B中发生反应的化学方程式为_______ ,该反应属于_______ (填基本反应类型)。
②小莉认为省略上述实验中的_______ (填字母),也能达到实验目的。
Ⅲ.金属的锈蚀与防护
(3)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。“发蓝”过程属于______ (填“物理”或“化学”)变化。
Ⅵ.金属的回收再利用
(4)某电镀厂为了减少对水的污染并节约成本,从排放的废液(主要含ZnSO4、FeSO4和CuSO4)中回收金属铜、铁以及工业原料硫酸锌,设计了如图所示的工艺流程,请据图回答下列问题:
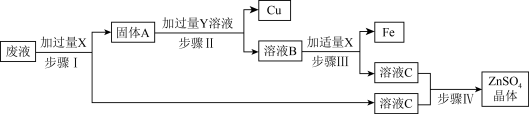
①步骤1中分离固体A和溶液C的操作名称是_______ 。
②物质X的化学式为_______ 。
③溶液B中含有的溶质有_______ 。
④请写出步骤Ⅲ中生成Fe的化学反应方程式:_______ 。
Ⅰ.金属冶炼
(1)《天工开物》中记载了炼锡的场景:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化。
①鼓入足量空气的目的是
②“点铅勾锡”是炼锡的关键步骤,加铅能使锡较易熔化流出,其原因是
Ⅱ.金属的活动性
(2)为探究锌、铁、铜三种金属的活动性及它们和氢元素的位置关系,小明设计了如下实验:

①试管B中发生反应的化学方程式为
②小莉认为省略上述实验中的
Ⅲ.金属的锈蚀与防护
(3)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。“发蓝”过程属于
Ⅵ.金属的回收再利用
(4)某电镀厂为了减少对水的污染并节约成本,从排放的废液(主要含ZnSO4、FeSO4和CuSO4)中回收金属铜、铁以及工业原料硫酸锌,设计了如图所示的工艺流程,请据图回答下列问题:

①步骤1中分离固体A和溶液C的操作名称是
②物质X的化学式为
③溶液B中含有的溶质有
④请写出步骤Ⅲ中生成Fe的化学反应方程式:
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】工业铁红主要成分是Fe2O3,还含有少量的FeO、Fe3O4
【查阅资料】(1)草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O4•3H2O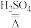 CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
(2)碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
(3)铁的常见氧化物中铁的质量分数:
【问题讨论】为了测定铁红中铁的质量分数,小组间进行如下实验。(装置气密性良好)
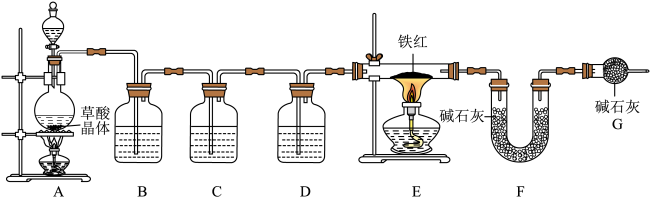
(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是________ (填字母序号)
a.浓硫酸b.澄清的石灰水c氢氧化钠溶液
(2)C装置的作用是__________________________ 。
(3)写出E装置中所发生反应的一个化学方程式:_____________________ 。
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①若E中充分反应后得到铁粉的质量为mg,则____ <m<______ 。
②若实验前后称得F装置增重7.7g,则此铁红中铁的质量分数是_________ 。
【实验反思】(1)如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会________ (选填“偏小”“不变”“偏大”)。
(2)该实验装置的一个明显缺陷是___________________ 。
【查阅资料】(1)草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O4•3H2O
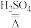 CO2↑+CO↑+H2O
CO2↑+CO↑+H2O(2)碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
(3)铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
【问题讨论】为了测定铁红中铁的质量分数,小组间进行如下实验。(装置气密性良好)

(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是
a.浓硫酸b.澄清的石灰水c氢氧化钠溶液
(2)C装置的作用是
(3)写出E装置中所发生反应的一个化学方程式:
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①若E中充分反应后得到铁粉的质量为mg,则
②若实验前后称得F装置增重7.7g,则此铁红中铁的质量分数是
【实验反思】(1)如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会
(2)该实验装置的一个明显缺陷是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】新冠肺炎在全球肆虐,医用防护口罩和消毒剂在预防新冠肺炎传播过程中发挥了不可替代的作用。生产医用口罩最核心的材料是“熔喷布”,它的主要成分是聚丙烯塑料,口罩上的鼻梁压条是金属铝。一定浓度的乙醇(C2H5OH)、过氧化氢、过氧乙酸(CH3COOOH)和84消毒液(有效成分为NaClO)均能有效杀灭新型冠状病毒。
(1)熔喷布的主要成分属于______ (填“金属”“合成”或“复合”)材料。
(2)四种消毒液的主要成分中属于盐类的是______ (填字母)。
a.C2H5OH b.H2O2 c.CH3COOOH d.NaClO
(3)金属铝生活中使用广泛。铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动顺序,某同学设计了如图3个实验:实验甲中会出现的现象是______ ;另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你的看法是______ (填序号)。
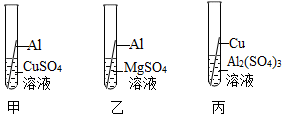
A.乙、丙都可以省去 B.乙、丙都不能省去
C.丙可以省去,乙不能省 D.乙可以省去,丙不能省
(4)工业上以粗盐为原料制备次氯酸钠(NaClO)的生产流程如图:
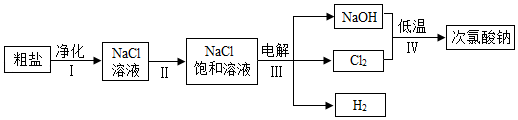
注:Cl2在通常情况下为黄绿色气体,有毒。
①使用84消毒液进行消毒时,要注意避免与洁厕灵(主要成分为浓HCl)混用,以免产生Cl2引起中毒:2HCl+NaClO═X+Cl2↑+H2O。X的化学式为______ 。
②将NaCl溶液由不饱和转变为饱和常采用蒸发浓缩的方法。一般不采用降温方法的主要原因是______ 。
③写出电解NaCl饱和溶液时反应的化学方程式:______ 。
④要把50g质量分数为12%的次氯酸钠溶液稀释为质量分数为2%的次氯酸钠溶液,需要水的体积为______ mL,下列仪器该实验过程中不需要的是______ (填名称)。
(1)熔喷布的主要成分属于
(2)四种消毒液的主要成分中属于盐类的是
a.C2H5OH b.H2O2 c.CH3COOOH d.NaClO
(3)金属铝生活中使用广泛。铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动顺序,某同学设计了如图3个实验:实验甲中会出现的现象是

A.乙、丙都可以省去 B.乙、丙都不能省去
C.丙可以省去,乙不能省 D.乙可以省去,丙不能省
(4)工业上以粗盐为原料制备次氯酸钠(NaClO)的生产流程如图:

注:Cl2在通常情况下为黄绿色气体,有毒。
①使用84消毒液进行消毒时,要注意避免与洁厕灵(主要成分为浓HCl)混用,以免产生Cl2引起中毒:2HCl+NaClO═X+Cl2↑+H2O。X的化学式为
②将NaCl溶液由不饱和转变为饱和常采用蒸发浓缩的方法。一般不采用降温方法的主要原因是
③写出电解NaCl饱和溶液时反应的化学方程式:
④要把50g质量分数为12%的次氯酸钠溶液稀释为质量分数为2%的次氯酸钠溶液,需要水的体积为

您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】金属材料在生产生活中有广泛的用途。
(1)用镍钛合金制成的飞船天线在低温下折叠,进入太空后可重新展开恢复成原状。关于镍钛合金的表述错误的是_____
A.具有良好的导电性 B.化学性质非常活泼
C.具有形状记忆功能 D.具有良好的延展性
(2)我国客机C919 外壳中含有钛合金和铝锂合金。飞机大量使用合金而不用纯金属的原因_____ 。(答出一点即可)
(3)将一包银粉和锌粉的混合物放入一定量的硫酸铜溶液中,充分反应后过滤。
①写出发生反应的化学方程式_____ 。
②若向滤渣中加入稀盐酸有气泡生成,则该反应的化学方程式为_____ 。
③若滤液为蓝色,则滤液中一定含有的金属离子是_____ (写离子符号)。
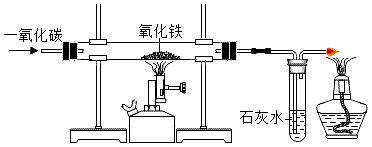
(4)如图为实验室模拟工业上炼铁的原理。当观察到_____ 现象时,即证明该反应已经结束可停止加热。该装置末端中添加酒精灯的目的是_____ 。
(5)生铁是由含铁的矿石冶炼得到的。要炼得含铁98%的生铁500t,需要氧化铁的质量是_____ ?
(1)用镍钛合金制成的飞船天线在低温下折叠,进入太空后可重新展开恢复成原状。关于镍钛合金的表述错误的是
A.具有良好的导电性 B.化学性质非常活泼
C.具有形状记忆功能 D.具有良好的延展性
(2)我国客机C919 外壳中含有钛合金和铝锂合金。飞机大量使用合金而不用纯金属的原因
(3)将一包银粉和锌粉的混合物放入一定量的硫酸铜溶液中,充分反应后过滤。
①写出发生反应的化学方程式
②若向滤渣中加入稀盐酸有气泡生成,则该反应的化学方程式为
③若滤液为蓝色,则滤液中一定含有的金属离子是
(4)如图为实验室模拟工业上炼铁的原理。当观察到
(5)生铁是由含铁的矿石冶炼得到的。要炼得含铁98%的生铁500t,需要氧化铁的质量是

您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】金属在生产生活中有广泛应用。
(1)共享单车作为代步工具,既轻便灵活,又环保。如图是一款自行车的图片,所标材料中,车架要含有的金属元素是______ ,为防止车架生锈,可以采取的防锈措施是______ ,铝合金与纯铝相比,其硬度更______ (填“大”或“小”)。

(2)赤铁矿(主要成分Fe2O3)是炼铁的一种矿石,Fe2O3属于______ (填“单质”或“氧化物”)。我国是使用“水法冶铜”最早的国家,请写出铁和硫酸铜溶液反应的化学方程式______ 。
(3)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是______ (填序号)。
①Fe、CuSO4溶液、Ag
②FeSO4溶液、Cu、Ag
③FeSO4溶液、Cu、AgNO3溶液
④FeSO4溶液、CuSO4溶液、Ag
(4)学校的实验室中,某黑色固体粉末可能是Fe、FeO、CuO、C中的一种或几种,为了探究其成分,化学兴趣小组的同学按照如图所示流程进行了实验。
(已知:FeO+H2SO4═FeSO4+H2O,CuO+H2SO4═CuSO4+H2O)
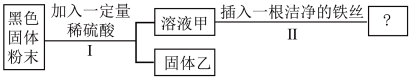
关于该实验有以下说法:
①若溶液甲呈浅绿色,则原黑色固体粉末中可能有Fe
②若步骤Ⅱ中无明显现象,则固体乙中最多有五种物质
③若步骤Ⅱ中有红色固体析出,则固体乙中一定没有CuO
④若固体乙呈红色,则原固体中一定含有Fe和CuO
以上说法中正确的是______ 。
(1)共享单车作为代步工具,既轻便灵活,又环保。如图是一款自行车的图片,所标材料中,车架要含有的金属元素是

(2)赤铁矿(主要成分Fe2O3)是炼铁的一种矿石,Fe2O3属于
(3)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是
①Fe、CuSO4溶液、Ag
②FeSO4溶液、Cu、Ag
③FeSO4溶液、Cu、AgNO3溶液
④FeSO4溶液、CuSO4溶液、Ag
(4)学校的实验室中,某黑色固体粉末可能是Fe、FeO、CuO、C中的一种或几种,为了探究其成分,化学兴趣小组的同学按照如图所示流程进行了实验。
(已知:FeO+H2SO4═FeSO4+H2O,CuO+H2SO4═CuSO4+H2O)

关于该实验有以下说法:
①若溶液甲呈浅绿色,则原黑色固体粉末中可能有Fe
②若步骤Ⅱ中无明显现象,则固体乙中最多有五种物质
③若步骤Ⅱ中有红色固体析出,则固体乙中一定没有CuO
④若固体乙呈红色,则原固体中一定含有Fe和CuO
以上说法中正确的是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐3】金属材料在人类发展的历史长河中起着非常重要的作用。
(1)我国探月工程嫦娥五号探测器用到了铝合金材料。一般情况下,铝合金的强度和硬度比纯铝的______ (填“高”或“低”)。
(2)铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动性顺序、某同学设计了如图1所示三个实验:
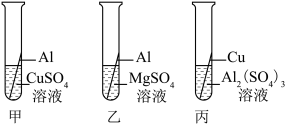
①实验甲中铝丝会出现的现象是______ ,该反应的化学方程式为______ 。
②另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你的看法是______ (填字母代号)。
A.乙、丙都可以省去B.乙、丙都不能省去
C.丙可以省去,乙不能省D.乙可以省去,丙不能省
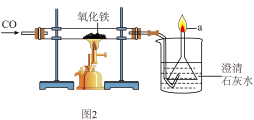
(3)钢铁是使用最多的金属材料。某化学小组利用如图2所示装置模拟工业炼铁的实验。
①写出玻璃长管中发生反应的化学方程式______ 。
②检验CO还原Fe2O3反应的气体生成物的实验现象是什么?______ 。
③a处尾气被点燃,写出反应的化学方程式______ 。
(4)高铁的快速发展方便了人们的出行。工业上可利用铝粉和Fe2O3在高温下发生置换反应制得铁来焊接钢轨。用13.5kg铝粉可制取铁的质量是多少?______ (反应方程式: )
)
(1)我国探月工程嫦娥五号探测器用到了铝合金材料。一般情况下,铝合金的强度和硬度比纯铝的
(2)铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动性顺序、某同学设计了如图1所示三个实验:


①实验甲中铝丝会出现的现象是
②另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你的看法是
A.乙、丙都可以省去B.乙、丙都不能省去
C.丙可以省去,乙不能省D.乙可以省去,丙不能省
(3)钢铁是使用最多的金属材料。某化学小组利用如图2所示装置模拟工业炼铁的实验。
①写出玻璃长管中发生反应的化学方程式
②检验CO还原Fe2O3反应的气体生成物的实验现象是什么?
③a处尾气被点燃,写出反应的化学方程式
(4)高铁的快速发展方便了人们的出行。工业上可利用铝粉和Fe2O3在高温下发生置换反应制得铁来焊接钢轨。用13.5kg铝粉可制取铁的质量是多少?
 )
)
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】(1)金属的用途与性质密切相关。
①如图所示的赤铁矿的主要成分是__________ (填化学式)。

②家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据表格中的信息分析,其原因是______________________ 。
③生铁和钢是常见的两种铁合金,它们的性能不同是由于_______________ 不同。常用生铁铸铁锅,请你说出一个厨房中防止铁锅生锈的方法:__________________________ 。
④在空气中,铝具有很好的抗腐蚀性,其原因用化学方程式表示为_______________ 。
(2)A、B、C是金属活动性顺序表中的三种金属。取形状大小相同的A、B、C三种金属,分别向其加入同体积同溶质质量分数的稀盐酸,实验现象记录如下表。
从上表信息得出A、B、C三种金属的活动性由强到弱的顺序是_______ (填序号)。
(3)将一定量铝、铜粉末混合物加入硝酸银溶液中,充分反应后过滤,滤液为蓝色。关于该滤渣和滤液有下列四种说法:
①向滤渣中加入稀盐酸,一定有气泡产生。
②向滤液中加入稀盐酸,一定有沉淀产生。
③滤渣中一定含有Ag,可能含有Cu。
④滤液中一定含有Cu(NO3)2,一定不含AgNO3,可能含有Al(NO3)3。
⑤滤液中一定含有Cu(NO3)2和Al(NO3)3,可能含AgNO3。以上说法正确的是_________ (填序号)。
| 铜 | 铝 | |
| 密度/(g·cm-3) | 8.92 | 2.70 |
| 地壳中含量(质量分数/%) | 0.007 | 7.73 |
| 导电性(以银的导电性为100作标准) | 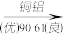 | |
①如图所示的赤铁矿的主要成分是

②家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据表格中的信息分析,其原因是
③生铁和钢是常见的两种铁合金,它们的性能不同是由于
④在空气中,铝具有很好的抗腐蚀性,其原因用化学方程式表示为
(2)A、B、C是金属活动性顺序表中的三种金属。取形状大小相同的A、B、C三种金属,分别向其加入同体积同溶质质量分数的稀盐酸,实验现象记录如下表。
| 实验 |  |  |  |
| 现象 | 速率快,产生大量气泡 | 速率缓慢,产生气泡较少 | 无现象 |
从上表信息得出A、B、C三种金属的活动性由强到弱的顺序是
(3)将一定量铝、铜粉末混合物加入硝酸银溶液中,充分反应后过滤,滤液为蓝色。关于该滤渣和滤液有下列四种说法:
①向滤渣中加入稀盐酸,一定有气泡产生。
②向滤液中加入稀盐酸,一定有沉淀产生。
③滤渣中一定含有Ag,可能含有Cu。
④滤液中一定含有Cu(NO3)2,一定不含AgNO3,可能含有Al(NO3)3。
⑤滤液中一定含有Cu(NO3)2和Al(NO3)3,可能含AgNO3。以上说法正确的是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】金属及其制品是现代生活中不可缺少的材料和工具。

(1)随着我国经济的飞速发展,轿车已进入我们大部分家庭。
①下列汽车部件使用了有机合成材料的是______ (填字母序号)。
A铝合金轮毂 B合成橡胶轮胎
C防撞钢梁 D玻璃车窗
②汽车电路使用的是铜导线,是因为铜具有良好的______ 性和延展性。车身喷漆除了美观,还可以防止生锈,其防锈原理是______ ;轮毂用铝合金而不用纯铝的原因是______ 。
(2)炼铁原理的实验装置如图所示:
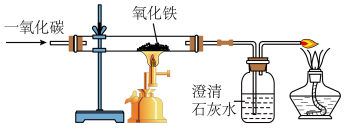
该实验操作有四个关键步骤:a加热、b停止加热、c通入CO、d停止通入CO,其正确的操作顺序是______ (填字母序号)。装置末端放一盏燃着的酒精灯,其作用是______ 。
(3)探究金属化学性质时,某同学按下列选项所示,将不同的金属放入到不同的盐溶液中,其中不能 发生反应的是______ (填字母序号,选项可能不唯一)。
AFe和CuSO4 BCu和FeSO4
CAg和CuCl2 DZn和AgNO3
(4)将一定量的Fe粉放入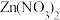 、
、 、AgNO3的混合溶液中,一段时间后过滤,往滤渣中滴加稀盐酸无任何变化,则以下说法正确的是
、AgNO3的混合溶液中,一段时间后过滤,往滤渣中滴加稀盐酸无任何变化,则以下说法正确的是______ (填字母序号,选项可能不唯一)。
A滤渣中一定有Ag,可能有Cu
B滤液中一定含有Zn2+、Fe2+、 可能含有Cu2+和Ag+
可能含有Cu2+和Ag+
C滤液中一定含有Zn2+、Fe2+、 和Cu2+,一定没有Ag+
和Cu2+,一定没有Ag+
D滤渣中一定有Ag和Cu,可能含有Fe

(1)随着我国经济的飞速发展,轿车已进入我们大部分家庭。
①下列汽车部件使用了有机合成材料的是
A铝合金轮毂 B合成橡胶轮胎
C防撞钢梁 D玻璃车窗
②汽车电路使用的是铜导线,是因为铜具有良好的
(2)炼铁原理的实验装置如图所示:

该实验操作有四个关键步骤:a加热、b停止加热、c通入CO、d停止通入CO,其正确的操作顺序是
(3)探究金属化学性质时,某同学按下列选项所示,将不同的金属放入到不同的盐溶液中,其中
AFe和CuSO4 BCu和FeSO4
CAg和CuCl2 DZn和AgNO3
(4)将一定量的Fe粉放入
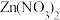 、
、 、AgNO3的混合溶液中,一段时间后过滤,往滤渣中滴加稀盐酸无任何变化,则以下说法正确的是
、AgNO3的混合溶液中,一段时间后过滤,往滤渣中滴加稀盐酸无任何变化,则以下说法正确的是A滤渣中一定有Ag,可能有Cu
B滤液中一定含有Zn2+、Fe2+、
 可能含有Cu2+和Ag+
可能含有Cu2+和Ag+C滤液中一定含有Zn2+、Fe2+、
 和Cu2+,一定没有Ag+
和Cu2+,一定没有Ag+D滤渣中一定有Ag和Cu,可能含有Fe
您最近一年使用:0次
【推荐3】(1)从海水中可以提取粗盐(含少量泥沙和CaCl2、MgSO4等可溶性杂质)。小明利用如图流程对1.8g粗盐进行除杂,得到精盐(实验环境温度为20℃)。

①操作1需要在______ (填字母序号)中进行。
A研钵 B量筒 C烧杯 D广口瓶
②操作2的步骤为溶解、过滤、______ 、结晶,过滤操作中玻璃棒的作用是______ 。
③已知20℃时NaCl的溶解度为36g,从节约能源和提高产率的角度分析,操作2中所需水的最佳体积是______ mL。(提示:水的密度为1g/mL)
④操作3的步骤为“盐洗”(即用NaCl溶液浸洗粗盐,以溶解除去其中可溶性杂质),过滤、烘干,则“盐洗”溶液应选用NaCl的______ (选填“饱和”或“不饱和”)溶液。
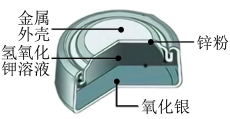
(2)纽扣电池是生活中常用的电源,下图是银锌纽扣电池的构造示意图,回答下列问题。
①纽扣电池的外壳可以加工得很薄,说明金属具有______ 性。
②氧化银加热分解可以得到两种单质,其化学反应方程式为______ 。
③该电池中涉及的铁、锌、银三种金属,它们的金属活动性由强到弱的顺序是______ ,为了验证该结论,某同学向质量、外形相同的铁片、锌片、银片中分别加入足量15%的稀盐酸,以下现象中不能成为该结论证据的是______ (填序号)。
A银表面没有气泡生成
B铁表面产生气泡的速率比锌慢
C铁表面最终生成气体的总量比锌多

①操作1需要在
A研钵 B量筒 C烧杯 D广口瓶
②操作2的步骤为溶解、过滤、
③已知20℃时NaCl的溶解度为36g,从节约能源和提高产率的角度分析,操作2中所需水的最佳体积是
④操作3的步骤为“盐洗”(即用NaCl溶液浸洗粗盐,以溶解除去其中可溶性杂质),过滤、烘干,则“盐洗”溶液应选用NaCl的
(2)纽扣电池是生活中常用的电源,下图是银锌纽扣电池的构造示意图,回答下列问题。

①纽扣电池的外壳可以加工得很薄,说明金属具有
②氧化银加热分解可以得到两种单质,其化学反应方程式为
③该电池中涉及的铁、锌、银三种金属,它们的金属活动性由强到弱的顺序是
A银表面没有气泡生成
B铁表面产生气泡的速率比锌慢
C铁表面最终生成气体的总量比锌多
您最近一年使用:0次




