某小组用W形管探究C还原 后的气体产物。
后的气体产物。
(1)按照配比,混合相应质量的C粉和 粉末,并充分混合、研磨。
粉末,并充分混合、研磨。

______ g。
(2)实验探究1: 研磨均匀后的粉末①装入A处,B处放入
研磨均匀后的粉末①装入A处,B处放入 澄清石灰水,用金属网罩住酒精灯加热。一段时间后,A处粉末变成红色,B处澄清石灰水变浑浊。请写B处出相关化学方程式
澄清石灰水,用金属网罩住酒精灯加热。一段时间后,A处粉末变成红色,B处澄清石灰水变浑浊。请写B处出相关化学方程式_______ 。
步骤2:分别用粉末②、粉末③重复上述实验,一段时间后,均出现A处粉末变成红色,B处澄清石灰水变浑浊。
根据上述实验结果可以得出的实验探究1的结论是_______ 。
(3)实验探究2:探究 与C反应能否生成
与C反应能否生成
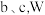 形管
形管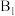 处放入
处放入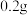 氧化铜粉末,凹槽
氧化铜粉末,凹槽 处不放置药品。点燃酒精灯,并对
处不放置药品。点燃酒精灯,并对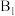 处固体加热5分钟,无明显现象。
处固体加热5分钟,无明显现象。
步骤2:另取W形管,取 粉末①装入
粉末①装入 处。从另一端放入
处。从另一端放入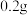 氧化铜粉末于
氧化铜粉末于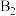 处,加热5分钟,发现
处,加热5分钟,发现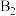 处
处 无明显变化。
无明显变化。
步骤3:分别用粉末②、粉末③重复上述实验,加热5分钟,发现 处
处 变成红色。
变成红色。
实验探究2中,步骤1的目的是______ 。
(4)进一步用仪器测量实验探究2产生的气体,得到以下图像:________ 。
②从定量角度分析,C还原 生成
生成 的含量增加的原因可能是
的含量增加的原因可能是________ 。
 后的气体产物。
后的气体产物。(1)按照配比,混合相应质量的C粉和
 粉末,并充分混合、研磨。
粉末,并充分混合、研磨。| 编号 | 粉末① | 粉末② | 粉末③ |
| C原子与O原子个数比 |  | 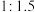 |  |
| C粉质量 |  |  |  |
 质量 质量 |  | x | 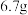 |

(2)实验探究1:

 研磨均匀后的粉末①装入A处,B处放入
研磨均匀后的粉末①装入A处,B处放入 澄清石灰水,用金属网罩住酒精灯加热。一段时间后,A处粉末变成红色,B处澄清石灰水变浑浊。请写B处出相关化学方程式
澄清石灰水,用金属网罩住酒精灯加热。一段时间后,A处粉末变成红色,B处澄清石灰水变浑浊。请写B处出相关化学方程式步骤2:分别用粉末②、粉末③重复上述实验,一段时间后,均出现A处粉末变成红色,B处澄清石灰水变浑浊。
根据上述实验结果可以得出的实验探究1的结论是
(3)实验探究2:探究
 与C反应能否生成
与C反应能否生成
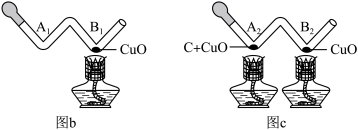
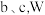 形管
形管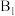 处放入
处放入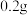 氧化铜粉末,凹槽
氧化铜粉末,凹槽 处不放置药品。点燃酒精灯,并对
处不放置药品。点燃酒精灯,并对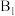 处固体加热5分钟,无明显现象。
处固体加热5分钟,无明显现象。步骤2:另取W形管,取
 粉末①装入
粉末①装入 处。从另一端放入
处。从另一端放入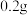 氧化铜粉末于
氧化铜粉末于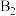 处,加热5分钟,发现
处,加热5分钟,发现 处
处 无明显变化。
无明显变化。步骤3:分别用粉末②、粉末③重复上述实验,加热5分钟,发现
 处
处 变成红色。
变成红色。实验探究2中,步骤1的目的是
(4)进一步用仪器测量实验探究2产生的气体,得到以下图像:

②从定量角度分析,C还原
 生成
生成 的含量增加的原因可能是
的含量增加的原因可能是
更新时间:2024-05-09 13:11:28
|
相似题推荐
实验题
|
较难
(0.4)
【推荐1】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g进行系列实验。
【查阅资料】①氧化铜(CuO)为黑色固体。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+ H2SO4 = CuSO4 + H2O + Cu
【进行实验】
实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
实验2:取一定量的混合物,用1—2装置进行实验。
【解释与结论】
(1)配平化学方程式:___ C+ ___ CuO高温___ Cu+ ___ CO2↑。
(2)实验1—2中,证明产生CO2的现象是_______________________ 。
(3)实验1的目的是__________ 。
(4)实验2的结论是_____________ 。
【反思与评价】
(5)实验2没有进行质量比为1:14的实验,理由是________________ 。
(6)为检验2—4的红色固体中是否含Cu2O,所需试剂是__________ 。
【查阅资料】①氧化铜(CuO)为黑色固体。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+ H2SO4 = CuSO4 + H2O + Cu
【进行实验】
实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
| 序号 | 1-1 | 1-2 |
| 装置 | 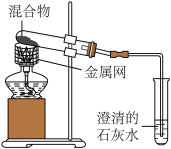 | 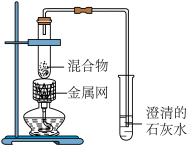 |
| 反应后物质的颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量,黑色物质 |
实验2:取一定量的混合物,用1—2装置进行实验。
| 序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
| 2-1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
| 2-2 | 1:10 | 混有很少量黑色物质 | |
| 2-3 | 1:11 | 混有极少量黑色物质 | |
| 2-4 | 1:12 | 无黑色物质 | |
| 2-5 | 1:13 | 混有较多黑色物质 | |
【解释与结论】
(1)配平化学方程式:
(2)实验1—2中,证明产生CO2的现象是
(3)实验1的目的是
(4)实验2的结论是
【反思与评价】
(5)实验2没有进行质量比为1:14的实验,理由是
(6)为检验2—4的红色固体中是否含Cu2O,所需试剂是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐2】实验与探究是化学学习的重要方法,请以碳及其化合物的知识探究以下问题。
①探究一:木炭与氧化铜在一定条件下发生反应。甲同学查阅资料后,建议用超细炭粉与氧化铜粉末混合进行实验,他的理由是_______________ 。
②探究二:现有混有少量二氧化碳的一氧化碳气体,乙同学为了检验两种气体的存在,用如下装置进行实验。
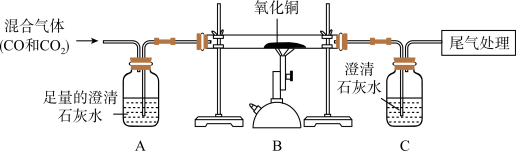
I.A装置的作用是_______________ ,产生的现象是 __________________ 。
II.B装置中发生反应的化学方程式是______________ ,其中氧化铜发生 _______ (填“氧化”或“还原”)反应。
Ⅲ.C装置中尾气处理的方法是______________ (写出一种)。
③探究三:人们曾用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和碳酸钠(俗名:纯碱)为原料制取氢氧化钠,丙同学按下图所示流程进行实验。
【提示:碳酸钠能与氢氧化钙反应,化学方程式为Na2CO3+ Ca(OH)2→ CaCO3↓ + 2NaOH】
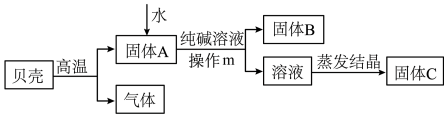
I.贝壳高温煅烧时,该反应的基本类型是________ (填“化合”或“分解”)。
II.流程中操作m是_________ ;将溶液蒸发结晶至 ___________ 时停止加热。
Ⅲ.将固体C配成溶液,其溶液中一定含有的溶质是________________ 。
①探究一:木炭与氧化铜在一定条件下发生反应。甲同学查阅资料后,建议用超细炭粉与氧化铜粉末混合进行实验,他的理由是
②探究二:现有混有少量二氧化碳的一氧化碳气体,乙同学为了检验两种气体的存在,用如下装置进行实验。

I.A装置的作用是
II.B装置中发生反应的化学方程式是
Ⅲ.C装置中尾气处理的方法是
③探究三:人们曾用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和碳酸钠(俗名:纯碱)为原料制取氢氧化钠,丙同学按下图所示流程进行实验。
【提示:碳酸钠能与氢氧化钙反应,化学方程式为Na2CO3+ Ca(OH)2→ CaCO3↓ + 2NaOH】

I.贝壳高温煅烧时,该反应的基本类型是
II.流程中操作m是
Ⅲ.将固体C配成溶液,其溶液中一定含有的溶质是
您最近一年使用:0次
实验题
|
较难
(0.4)
【推荐3】用碳、一氧化碳还原氧化铜的仪器、装置如下图。(连接装置的橡皮管省略)

请回答以下问题:
① 一氧化碳还原氧化铜的实验中,除A装置外,还需选用的仪器、装置组合是__________ (填字母),选用该仪器、装置的目的是___________ 、____________ 。
② 碳还原氧化铜的实验中(将A中的酒精灯换成酒精喷灯),反应的化学方程式是________________ 。
③ 用碳和一氧化碳还原氧化铜的两个实验中,装置A中观察到的现象是_____________ 。
④ 现有一包混有少量碳粉的氧化铜粉末,为了测定其碳粉的质量分数,称取m g样品进行高温加热,实验过程中获取两组数据:
Ⅰ.反应前后仪器a中质量减少x g;
Ⅱ.吸收生成物的仪器中质量增加y g。
假设反应充分,称量准确,你认为应选择哪组数据进行计算会更为合理准确?你的理由是_________ ,请列出计算碳粉质量分数的式子___________ 。(用m、x、y表示)。

请回答以下问题:
① 一氧化碳还原氧化铜的实验中,除A装置外,还需选用的仪器、装置组合是
② 碳还原氧化铜的实验中(将A中的酒精灯换成酒精喷灯),反应的化学方程式是
③ 用碳和一氧化碳还原氧化铜的两个实验中,装置A中观察到的现象是
④ 现有一包混有少量碳粉的氧化铜粉末,为了测定其碳粉的质量分数,称取m g样品进行高温加热,实验过程中获取两组数据:
Ⅰ.反应前后仪器a中质量减少x g;
Ⅱ.吸收生成物的仪器中质量增加y g。
假设反应充分,称量准确,你认为应选择哪组数据进行计算会更为合理准确?你的理由是
您最近一年使用:0次
实验题
|
较难
(0.4)
名校
【推荐1】某固体粉末,可能含有硫酸钠、硫酸铜、氯化钠、硝酸钡、碳酸钙中的一种或几种,某科学兴趣小组为探究其成分,设计了如下实验流程(所加试剂均足量):

(1)操作Ⅰ、Ⅱ的名称是____ ;
(2)固体粉末中一定含有____ ;一定不含____ ,可能含有____ ;
(3)灼烧时发生的化学反应方程式是____ 。

(1)操作Ⅰ、Ⅱ的名称是
(2)固体粉末中一定含有
(3)灼烧时发生的化学反应方程式是
您最近一年使用:0次
实验题
|
较难
(0.4)
【推荐2】酸、碱、盐在生产生活中具有广泛的用途。
(1)制作“叶脉书签”需用到10%的氢氧化钠溶液。现配制100g质量分数为10%的氢氧化钠溶液。
①若用氢氧化钠固体配制,需称量氢氧化钠的质量为__________ g。
②用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、烧杯、玻璃棒、胶头滴管、试剂瓶外,还需要__________ 。
③下列操作正确的是__________ (填字母序号)。
A.称量氢氧化钠固体时,左盘放砝码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
D.将配好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
④若用20%的氢氧化钠溶液加水(水的密度为1g/cm3)配制100g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为_________ g;配制时应选用_________ mL的量筒取水(填“100”或“50”或10)。
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如下实验:

回答下列问题:
①反应Ⅰ的化学方程式为__________________________ 。
②白色沉淀C是_________________ (填化学式)。
③原固体粉末中一定不含________________ 、______________ (填化学式)。
(1)制作“叶脉书签”需用到10%的氢氧化钠溶液。现配制100g质量分数为10%的氢氧化钠溶液。
①若用氢氧化钠固体配制,需称量氢氧化钠的质量为
②用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、烧杯、玻璃棒、胶头滴管、试剂瓶外,还需要
③下列操作正确的是
A.称量氢氧化钠固体时,左盘放砝码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
D.将配好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
④若用20%的氢氧化钠溶液加水(水的密度为1g/cm3)配制100g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如下实验:

回答下列问题:
①反应Ⅰ的化学方程式为
②白色沉淀C是
③原固体粉末中一定不含
您最近一年使用:0次
实验题
|
较难
(0.4)
名校
【推荐3】为探究氢氧化钡的化学性质,同学们进行了以下实验:

(1)实验1:氢氧化钡溶液中滴加酚酞后显红色,说明氢氧化钡溶液显______ 性;
(2)实验2:通入二氧化碳气体后,能观察到的实验现象是_________ ;
(3)实验3:充分反应后,静置,为确定上层清液的成分,取少量上层清液于试管中,向其中加入的一种试剂是________ ;
(4)将上述实验1、实验2、实验3反应后的混合物倒入同一个洁净的烧杯中,静置后过滤,得到白色沉淀和红色溶液,取少量红色溶液,通入足量二氧化碳,无明显现象,为确定红色溶液中溶质的成分,需补充的操作是________ 。

(1)实验1:氢氧化钡溶液中滴加酚酞后显红色,说明氢氧化钡溶液显
(2)实验2:通入二氧化碳气体后,能观察到的实验现象是
(3)实验3:充分反应后,静置,为确定上层清液的成分,取少量上层清液于试管中,向其中加入的一种试剂是
(4)将上述实验1、实验2、实验3反应后的混合物倒入同一个洁净的烧杯中,静置后过滤,得到白色沉淀和红色溶液,取少量红色溶液,通入足量二氧化碳,无明显现象,为确定红色溶液中溶质的成分,需补充的操作是
您最近一年使用:0次



