阿司匹林(C9H8O4)是一种用于解热镇痛的抗炎药。实验小组对无催化剂合成阿司匹林产率的影响因素进行了探究。
【进行实验】
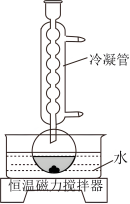
取水杨酸和乙酸酐于烧瓶中,在不同温度下,采用500r/min的转速进行磁力搅拌(如图),反应一段时间后冷却结晶,洗涤干燥,称量得到的阿司匹林的质量,并计算产率。实验记录如表:
【解释与结论】
(1)阿司匹林(C9H8O4)中氢、氧原子的个数比为_______ 。
(2)①②③的目的是_______ 。
(3)得出“乙酸酐的体积对无催化剂合成阿司匹林的产率有影响”的结论,依据的一组实验是_______ (填序号)。
(4)依据表中数据分析,无催化剂合成阿司匹林的最佳实验条件是3.5g水杨酸、3.5mL乙酸酐、_______ 。
【反思与评价】
(5)继续实验探究磁力搅拌转速对无催化剂合成阿司匹林的产率是否有影响,实验方案为:取3.5g水杨酸和3.5mL乙酸酐于烧瓶中,在85℃时,_______ 。
(6)在上述实验的基础上,关于合成阿司匹林还可以研究的问题是_______ 。
【进行实验】
取水杨酸和乙酸酐于烧瓶中,在不同温度下,采用500r/min的转速进行磁力搅拌(如图),反应一段时间后冷却结晶,洗涤干燥,称量得到的阿司匹林的质量,并计算产率。实验记录如表:
| 实验序号 | 水杨酸的质量/g | 乙酸酐的体积/mL | 温度/℃ | 反应时间/min | 产率/% |
| ① | 3.5 | 3.5 | 85 | 20 | 63.73 |
| ② | 3.5 | 3.5 | 85 | 25 | 75.25 |
| ③ | 3.5 | 3.5 | 85 | 30 | 45.64 |
| ④ | 3.5 | 2.4 | 85 | 25 | 29.81 |
| ⑤ | 3.5 | 4.7 | 85 | 25 | 58.77 |
| ⑥ | 3.5 | 3.5 | 75 | 25 | 43.44 |
| ⑦ | 3.5 | 3.5 | 95 | 25 | 19.93 |
(1)阿司匹林(C9H8O4)中氢、氧原子的个数比为
(2)①②③的目的是
(3)得出“乙酸酐的体积对无催化剂合成阿司匹林的产率有影响”的结论,依据的一组实验是
(4)依据表中数据分析,无催化剂合成阿司匹林的最佳实验条件是3.5g水杨酸、3.5mL乙酸酐、
【反思与评价】
(5)继续实验探究磁力搅拌转速对无催化剂合成阿司匹林的产率是否有影响,实验方案为:取3.5g水杨酸和3.5mL乙酸酐于烧瓶中,在85℃时,
(6)在上述实验的基础上,关于合成阿司匹林还可以研究的问题是
2024·北京房山·一模 查看更多[1]
更新时间:2024-05-09 22:02:49
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】2020年新冠肺炎肆虐期间,很多人使用84消毒液对家里和公共区域进行消毒。同学们对84消毒液的漂白和消毒杀菌效果产生了兴趣,进行了如下实验探究:
【查阅资料】
(1)84消毒液为无色或淡黄色液体,是次氯酸钠(化学式NaClO)和表面活性剂的混合物。
(2)消毒杀菌就是使细菌病毒的蛋白质变性;鸡蛋清中蛋白质变性会变白。
【进行实验】
实验1:漂白褪色实验
室温下,取不同浓度的消毒液各30mL于4只烧杯中。将形状大小相同的布条投入烧杯中,记录如下:
1小时后,发现实验1-1中的布条已经浸烂,实验1-2中布条抽出的棉线极易被拉断,实验1-3、实验1-4中布条损害很小。
实验2:消毒杀菌实验
室温下,分别取2mL鸡蛋清于四支试管中,试管编号分别为2-1、2-2、2-3、2-4,分别向四支试管中滴加10滴消毒液原液、1:25、1:100、1:200的溶液,振荡静置15分钟后观察现象。记录如下:
【解释与结论】
(1)84消毒液主要成分为次氯酸钠(化学式NaClO),次氯酸钠由_____ 种元素组成。
(2)根据实验1可知:消毒液浓度对棉质衣物漂白效果的影响是_____ 。要得到较好的漂白效果,又可以使衣物少受伤害,应选择比例为_____ 稀释84消毒液,且浸泡时间在20分钟以内最好。
(3)实验2的目的是:_____ 。
【反思与评价】
(4)84消毒液与洁厕灵混用,会反应产生有毒的氯气。氯气是一种气体单质,每个氯气分子中含有两个氯(Cl)原子,其化学式为_____ 。
(5)综合上述实验,你还有什么使用84消毒液的建议?_____ 。
【查阅资料】
(1)84消毒液为无色或淡黄色液体,是次氯酸钠(化学式NaClO)和表面活性剂的混合物。
(2)消毒杀菌就是使细菌病毒的蛋白质变性;鸡蛋清中蛋白质变性会变白。
【进行实验】
实验1:漂白褪色实验
室温下,取不同浓度的消毒液各30mL于4只烧杯中。将形状大小相同的布条投入烧杯中,记录如下:
| 实验编号 | 布条种类 | 84消毒液体积与水的体积比 | 实验现象 |
| 1-1 | 粉红色棉质 | 1:0 | 布条立即褪色,而且完全褪成白色 |
| 1-2 | 粉红色棉质 | 1:25 | 刚接触溶液,布条褪色缓慢。1分钟后布条颜色褪成淡粉色。15分钟后,布条的淡粉色完全褪尽。 |
| 1-3 | 粉红色棉质 | 1:100 | 刚接触溶液,布条褪色不明显。2分钟后,布条红色基本褪成粉色。20分钟后,布条粉色完全褪尽。 |
| 1-4 | 粉红色棉质 | 1:200 | 刚接触溶液,布条不褪色。5分钟后,布条褪成淡粉色。25分钟后布条仍呈淡粉色。 |
1小时后,发现实验1-1中的布条已经浸烂,实验1-2中布条抽出的棉线极易被拉断,实验1-3、实验1-4中布条损害很小。
实验2:消毒杀菌实验
室温下,分别取2mL鸡蛋清于四支试管中,试管编号分别为2-1、2-2、2-3、2-4,分别向四支试管中滴加10滴消毒液原液、1:25、1:100、1:200的溶液,振荡静置15分钟后观察现象。记录如下:
| 实验 编号 | 第一步 | 84消毒液体积与水的体积比 | 实验现象 |
| 2-1 | 鸡蛋清2mL | 1:0 | 液体表面产生大量气泡,无其他现象 |
| 2-2 | 鸡蛋清2mL | 1:25 | 液体中产生大量白色物质 |
| 2-3 | 鸡蛋清2mL | 1:100 | 液体中产生少量白色物质 |
| 2-4 | 鸡蛋清2mL | 1:200 | 液体中产生极少量白色物质 |
【解释与结论】
(1)84消毒液主要成分为次氯酸钠(化学式NaClO),次氯酸钠由
(2)根据实验1可知:消毒液浓度对棉质衣物漂白效果的影响是
(3)实验2的目的是:
【反思与评价】
(4)84消毒液与洁厕灵混用,会反应产生有毒的氯气。氯气是一种气体单质,每个氯气分子中含有两个氯(Cl)原子,其化学式为
(5)综合上述实验,你还有什么使用84消毒液的建议?
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组同学做了一个“黑面包”实验将适量的蔗糖(C12H22O11)放入一烧杯中,再加入浓硫酸(H2SO4),观察到蔗糖变黑,体积膨胀,形成疏松多孔的“黑面包”,并闻到刺激性气味。同学们对反应产生了哪些气体展开了如下探究(假设每步反应均充分进行):
【物质分析】蔗糖是由碳、氢、氧三种元素组成,蔗糖是由蔗糖分子构成的,一个蔗糖分子中含有___ 个原子,蔗糖的相对分子质量是_______ 。
【查阅资料】①CO2与SO2都能使澄清石灰水变浑浊;
②SO2能与稀高锰酸钾溶液反应而使溶液褪色,CO2与之不反应;
③无水硫酸铜固体吸水后会由白色变成蓝色;
④H2和CO均具有可燃性。
【提出猜想】可能生成H2、N2、CO2、CO、SO2气体及水蒸气。
【实验步骤】实验小组设计了如下步骤:

①按如图安装好仪器(夹持装置已略去);
②_______ ;
③将蔗糖和浓H2SO4分别加入仪器中;
④打开活塞,使浓H2SO4缓缓地滴入烧瓶中;
⑤观察并记录实验现象。
【实验分析】
(1)某同学认真仔细审阅了题目,认为不需要进行实验就可以确定气体肯定不是N2,该同学得出此结论的依据是_______ 。
(2)B处无水硫酸铜变为_______ 色,说明气体中有水蒸气。
(3)C处稀高锰酸钾溶液褪色,说明有_______ (填化学式)生成;D处高锰酸钾溶液不褪色,E处_____ (填现象),说明有CO2生成,产生该现象反应的符号表达式为_______ 。
(4)反应一段时间后,在F的出口处放一燃着的木条,发现出口处无明显现象。
【实验结论】反应产生的气体的成分有_______ (填序号)。
A.H2、CO2、H2O B.CO、CO2、H2O C.CO2、SO2、H2O
【物质分析】蔗糖是由碳、氢、氧三种元素组成,蔗糖是由蔗糖分子构成的,一个蔗糖分子中含有
【查阅资料】①CO2与SO2都能使澄清石灰水变浑浊;
②SO2能与稀高锰酸钾溶液反应而使溶液褪色,CO2与之不反应;
③无水硫酸铜固体吸水后会由白色变成蓝色;
④H2和CO均具有可燃性。
【提出猜想】可能生成H2、N2、CO2、CO、SO2气体及水蒸气。
【实验步骤】实验小组设计了如下步骤:

①按如图安装好仪器(夹持装置已略去);
②
③将蔗糖和浓H2SO4分别加入仪器中;
④打开活塞,使浓H2SO4缓缓地滴入烧瓶中;
⑤观察并记录实验现象。
【实验分析】
(1)某同学认真仔细审阅了题目,认为不需要进行实验就可以确定气体肯定不是N2,该同学得出此结论的依据是
(2)B处无水硫酸铜变为
(3)C处稀高锰酸钾溶液褪色,说明有
(4)反应一段时间后,在F的出口处放一燃着的木条,发现出口处无明显现象。
【实验结论】反应产生的气体的成分有
A.H2、CO2、H2O B.CO、CO2、H2O C.CO2、SO2、H2O
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】材料:2013年12月2日,“嫦娥三号”探测器由长征三号运载火箭发射,首次实现月球软着陆和月面巡视勘察。12月15日晚,“嫦娥三号”着陆器和巡视器(玉兔月球车)成功分离,顺利互拍,任务取得圆满成功。长征三号运载火箭主要用于发射地球同步轨道有效载荷,它的一子级和二子级使用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作推进剂,三子级则使用效能更高的液氢(H2)和液氧(O2)。
(1)“长征三号”三子级火箭用液氢做燃料,其反应的化学方程式为_________ ,使用液氢做燃料的优点有:_________ (填一条)。
(2)下列有关偏二甲肼(C2H8N2)的叙述正确的是________
(3)“玉兔”月球车(下图)主体为长方形盒状,车底安有六个轮状的移动装置,顶部两片太阳翼可以打开,太阳翼打开可将太阳能转化成_________ 能,为“玉兔”提供能源的还有锂电池和核电池。“玉兔号”对“车轮”要求极高。月球车底盘和车轮由铝合金材料制成,这是由于铝合金具有质轻坚硬的特性。

(4)看见玉兔车金灿灿的车身后,小聪想到家里新换的水龙头。他从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请你参与。
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu >Cr; 猜想3.你的猜想是_________ 。
【查阅资料】
① 铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
② 铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
【结论与解释】
① 小聪得到的结论是猜想_________ 正确。
② 实验前用砂纸打磨金属片的目的是____________________ 。
【知识运用】
将铬片投入FeSO4溶液中,反应_________ (填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式__________________ 。
(1)“长征三号”三子级火箭用液氢做燃料,其反应的化学方程式为
(2)下列有关偏二甲肼(C2H8N2)的叙述正确的是
| A.由2个碳原子,4个氢原子,一个氮分子组成 |
| B.由碳、氢、氮三种元素组成 |
| C.由2个碳原子,8个氢原子,2个氮原子构成 |
| D.偏二甲肼分子中碳、氢、氮的原子个数比为1:4:1 |

(4)看见玉兔车金灿灿的车身后,小聪想到家里新换的水龙头。他从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请你参与。
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu >Cr; 猜想3.你的猜想是
【查阅资料】
① 铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
② 铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 | 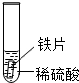 |  |  |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 |
【结论与解释】
① 小聪得到的结论是猜想
② 实验前用砂纸打磨金属片的目的是
【知识运用】
将铬片投入FeSO4溶液中,反应
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】人教版新课标化学九年级上册教材中“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其效果如何?
【实验结论】
(1)A中产生的气体是______ 。
(2)实验Ⅱ、Ⅲ证明:氧化铁的______ 和______ 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(3)写出氧化铁催化过氧化氢分解的符号表达式:______ 。
【实验评价】
(4)设计实验Ⅳ的目的是______ 。
(5)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此可以得到的结论是______ 。
【拓展延伸】
(6)你还能想到什么因素能影响过氧化氢分解的速率?请举一例说明。
因素______ ;实验方法:______ ;实验现象________ ;实验结论________ .
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其效果如何?
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象。 | A试管中产生气泡,带火星的木条复燃,B试管中无明显现象 |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象 | 试管中均产生气泡,带火星的木条均复燃 |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag | |
| Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
(1)A中产生的气体是
(2)实验Ⅱ、Ⅲ证明:氧化铁的
(3)写出氧化铁催化过氧化氢分解的符号表达式:
【实验评价】
(4)设计实验Ⅳ的目的是
(5)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此可以得到的结论是
【拓展延伸】
(6)你还能想到什么因素能影响过氧化氢分解的速率?请举一例说明。
因素
您最近一年使用:0次
【推荐2】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
Ⅰ.甲同学探究了影响双氧水分解速度的一些因素的相关数据。实验数据记录如下:
(1)本实验中,测量O2体积的装置是________ (填编号)。

(2)实验结论:通过实验①和②对比可知,_______ ,双氧水分解得越快。通过对比实验____ 和____ 可知,双氧水分解速度与温度的关系是________ 。
Ⅱ.为探究催化剂的种类对氯酸钾分解的影响,乙同学进行如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表进行实验:并测定分解温度(分解温度越低,催化效果越好)。
【分析数据、得出结论】
(1)由实验________ 与实验④对比,证明猜想合理。
(2)实验所用的三种物质,催化效果最好的是____________ 。
(3)写出二氧化锰催化氯酸钾分解的文字表达式:__________ 。
【反思】若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的_______ 和_____ 不变。
Ⅰ.甲同学探究了影响双氧水分解速度的一些因素的相关数据。实验数据记录如下:
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/mL | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 40 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |

(2)实验结论:通过实验①和②对比可知,
Ⅱ.为探究催化剂的种类对氯酸钾分解的影响,乙同学进行如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表进行实验:并测定分解温度(分解温度越低,催化效果越好)。
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | 氯酸钾 | 580 |
| ② | 氯酸钾、二氧化锰(质量比1:1) | 350 |
| ③ | 氯酸钾、氧化铜(质量比l:1) | 370 |
| ④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
(1)由实验
(2)实验所用的三种物质,催化效果最好的是
(3)写出二氧化锰催化氯酸钾分解的文字表达式:
【反思】若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】维生素C(简称Vc,又名抗坏血酸),易溶于水,易被氧化。人体缺乏Vc可能引发多种疾病。水果和蔬菜中含有丰富的Vc。某研究性学习小组对它探究如下:
(1)探究一:检验三种饮品中Vc含量的顺序。
【查阅资料】Vc能和高锰酸钾反应,使紫色的高锰酸钾溶液褪色。
【设计方案】分别向盛有lmL等浓度高锰酸钾稀溶液的三只试管中逐滴滴加果味饮料、苹果汁和梨汁,边滴边振荡,直至高锰酸钾溶液褪色。
【实验数据】
【实验结论】三种饮品中Vc含量由高到低的顺序是______________ (各液体浓度的差别忽略不计),依据是_________________ 。
(2)探究二:蔬菜放置时间的长短对其Vc含量是否有影响。
【设计方案】请你用新鲜的黄瓜、放置一周的黄瓜、高锰酸钾稀溶液和必要的仪器设计实验方案:
_________________________
【实验结论】按上述方案实验,根据______________________ 这一实验结果,分析得出蔬菜放置时间的长短对其Vc的含量有影响。
【实验反思】化学实验需要控制变量。在做探究二时,下列情况会影响到测定结果的是__________ 。
A、试管的大小不同
B、没有用同一规格胶头滴管滴加
C、所用高锰酸钾溶液的浓度不同
(1)探究一:检验三种饮品中Vc含量的顺序。
【查阅资料】Vc能和高锰酸钾反应,使紫色的高锰酸钾溶液褪色。
【设计方案】分别向盛有lmL等浓度高锰酸钾稀溶液的三只试管中逐滴滴加果味饮料、苹果汁和梨汁,边滴边振荡,直至高锰酸钾溶液褪色。
【实验数据】
| 果味饮料 | 苹果汁 | 梨汁 | |
| 滴加的滴数 | 40 | 10 | 20 |
(2)探究二:蔬菜放置时间的长短对其Vc含量是否有影响。
【设计方案】请你用新鲜的黄瓜、放置一周的黄瓜、高锰酸钾稀溶液和必要的仪器设计实验方案:
【实验结论】按上述方案实验,根据
【实验反思】化学实验需要控制变量。在做探究二时,下列情况会影响到测定结果的是
A、试管的大小不同
B、没有用同一规格胶头滴管滴加
C、所用高锰酸钾溶液的浓度不同
您最近一年使用:0次



