某小组开展了“探究催化剂的奥秘”项目式学习。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法正确的是______(填字母)。
【任务二】探究催化剂:查阅资料发现氧化铜也可以作为过氧化氢分解的催化剂,于是进行相应探究。
称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行下图所示实验。
(3)步骤⑦的目的______ 。
【任务三】探究不同催化剂的催化效果
(4)对比分析图2中的______ 点(填字母),可知化学反应速率与催化剂的种类有关。
(5)请从催化剂的角度解释在实验过程中,上述两个反应虽化学反应速率不同,但完全反应后两个装置内压强相同的原因______ 。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法正确的是______(填字母)。
| A.不加入催化剂化学反应就不能发生 |
| B.在化学反应前后催化剂的化学性质不发生改变 |
| C.用作催化剂的物质不可能是其他反应的反应物或生成物 |
【任务二】探究催化剂:查阅资料发现氧化铜也可以作为过氧化氢分解的催化剂,于是进行相应探究。
称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行下图所示实验。
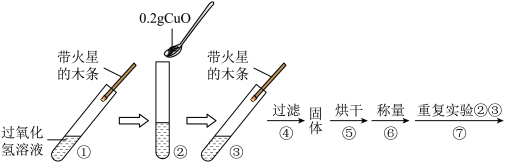
| 步骤①现象 | 步骤③现象 | 步骤⑥结果 | 实验结论 |
| 无明显现象 | 试管中有气泡产生, | 称得氧化铜的质量为 | 氧化铜是过氧化氢分解反应的催化剂 |
(3)步骤⑦的目的
【任务三】探究不同催化剂的催化效果
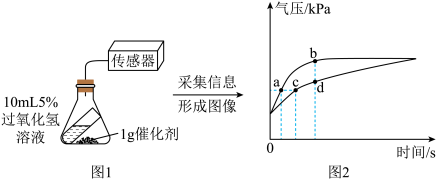
(4)对比分析图2中的
(5)请从催化剂的角度解释在实验过程中,上述两个反应虽化学反应速率不同,但完全反应后两个装置内压强相同的原因
更新时间:2024-05-11 23:22:58
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】学习了二氧化锰对过氧化氢有催化作用的知识后。某同学想:氧化铜能否起到类似二氧化锰的催化剂作用昵?于是进行了如下探究。
【提出猜想】
I.氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
II.氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
III.氧化铜是反应的催化剂,反应前后质量和化学性质不变。
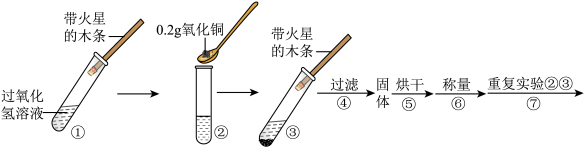
【进行实验】用天平称量 0.2g化氧铜,取5mL5%过的氧化氢溶液于试管中,进行如下实验:
(1)填写下表:
(2)步骤①的目的.是与步骤_______ 对比,检验加入氧化铜前后双氧水分解速度有无变化。
(3)过氧化氢能被氧化铜催化分解放出氧气的化学反应的文字表达式为___________ 。
【提出猜想】
I.氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
II.氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
III.氧化铜是反应的催化剂,反应前后质量和化学性质不变。

【进行实验】用天平称量 0.2g化氧铜,取5mL5%过的氧化氢溶液于试管中,进行如下实验:
(1)填写下表:
| 步骤③ 现象 | 步骤⑥ 结果 | 步骤⑦ 现象 | 结论 |
带火星的木条复燃 | 所得固体 | 溶液中有气泡放出, 带火星的木条复燃 | 猜想I、Ⅱ 不成立 猜想Ⅲ 成立 |
(2)步骤①的目的.是与步骤
(3)过氧化氢能被氧化铜催化分解放出氧气的化学反应的文字表达式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】84消毒液、过氧化氢溶液都是常用消毒剂,兴趣小组对两种消毒剂进行了如下探究活动。
【查阅资料】84消毒液的有效成分是次氯酸钠(化学式为NaClO)。
【实验1】取少量84消毒液于试管中,滴加过氧化氢溶液,发现有大量气泡产生:然后把_______ (填写实验操作和现象),证明产生的气体是氧气。
【提出问题】在上述反应中,NaClO的作用是什么?
【作出猜想】猜想一:作反应物,NaClO与过氧化氢溶液发生化学反应;
猜想二:作_______ 。
【实验2】
①按如图所示组装实验装置,并检查气密性。
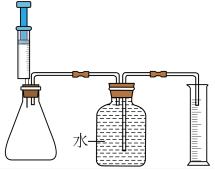
②向锥形瓶中加入30mL 84消毒液,注射器中吸入25mL过氧化氢溶液。
③将注射器中的过氧化氢溶液平均分5次推入锥形瓶中:每次推入过氧化氢溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响)见下表。
(1)表中的数据x=_______ 。
(2)分析表中数据得出“猜想一正确”,其依据是_______ 。
【分析讨论】次氯酸钠与过氧化氢溶液反应除生成氧气外,还生成氯化钠和水。写出该反应的符号表达式_______ 。
【拓展反思】生活中常用消毒剂除84消毒液、过氧化氢溶液外,还有75%酒精、过氧乙酸等。
(3)在使用各种消毒剂时,要考虑它们的性质。切记:科学使用,注意安全!生活中下列使用消毒剂的做法正确的是_______ 。
A 不同的消毒剂不可随意混合使用
B 使用84消毒液的浓度越高越好
C 使用75%酒精消毒应远离明火,防止火灾
【查阅资料】84消毒液的有效成分是次氯酸钠(化学式为NaClO)。
【实验1】取少量84消毒液于试管中,滴加过氧化氢溶液,发现有大量气泡产生:然后把
【提出问题】在上述反应中,NaClO的作用是什么?
【作出猜想】猜想一:作反应物,NaClO与过氧化氢溶液发生化学反应;
猜想二:作
【实验2】
①按如图所示组装实验装置,并检查气密性。

②向锥形瓶中加入30mL 84消毒液,注射器中吸入25mL过氧化氢溶液。
③将注射器中的过氧化氢溶液平均分5次推入锥形瓶中:每次推入过氧化氢溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响)见下表。
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 收集气体的总体积/mL | 140 | 280 | 365 | x | 375 |
(2)分析表中数据得出“猜想一正确”,其依据是
【分析讨论】次氯酸钠与过氧化氢溶液反应除生成氧气外,还生成氯化钠和水。写出该反应的符号表达式
【拓展反思】生活中常用消毒剂除84消毒液、过氧化氢溶液外,还有75%酒精、过氧乙酸等。
(3)在使用各种消毒剂时,要考虑它们的性质。切记:科学使用,注意安全!生活中下列使用消毒剂的做法正确的是
A 不同的消毒剂不可随意混合使用
B 使用84消毒液的浓度越高越好
C 使用75%酒精消毒应远离明火,防止火灾
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小马虎在做过氧化氢溶液制取氧气时,错误地添加了同样是黑色的氧化铜,发现同样也能加快过氧化氢的分解速度,同学们对催化剂产生了兴趣,通过咨询和查阅资料了解到氧化铁同样也能加快过氧化氢的分解速度。他们设计了实验装置并进行了探究实验。实验以生成100mL的气体为标准,记录的时间如下表所示:
(1)实验④的作用是:_________ 。
(2)写出实验③的反应的文字表达式:___________ 。
(3)通过实验____ 和_____ 的比较可知氧化铁也能加快过氧化氢的分解速度,但若要证明氧化铁也是该反应的催化剂,还需要验证氧化铁在反应前后的_______ 和__________ 也没有改变。
(4)由实验可知,实验所用的三种物质中,___________ 催化效果最好。
(5)比较两组实验生成气体的快慢,除上述实验所用方法外,还可以采用的方法是:_______ 。
(6)上述实验表明催化剂的种类会影响过氧化氢的分解速率,而温度也可能会影响过氧化氢的分解速率,请你设计实验方案进行验证:_______ 。
你还知道影响过氧化氢分解速率的因素还可能有___________ (只要写一种即可)。
| 实验编号 | 过氧化氢溶液浓度(%) | 过氧化氢溶液体积(mL) | 过氧化氢溶液温度(℃) | 催化剂及其质量 | 收集100mL氧气 需要时间(s) |
| ① | 5 | 30 | 20 | 二氧化锰0.1g | 30.8 |
| ② | 5 | 30 | 20 | 氧化铜0.1g | 54.6 |
| ③ | 5 | 30 | 20 | 氧化铁0.1g | 64.7 |
| ④ | 5 | 30 | 20 | 无 | 150.5 |
(1)实验④的作用是:
(2)写出实验③的反应的文字表达式:
(3)通过实验
(4)由实验可知,实验所用的三种物质中,
(5)比较两组实验生成气体的快慢,除上述实验所用方法外,还可以采用的方法是:
(6)上述实验表明催化剂的种类会影响过氧化氢的分解速率,而温度也可能会影响过氧化氢的分解速率,请你设计实验方案进行验证:
你还知道影响过氧化氢分解速率的因素还可能有
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】双氧水(hydrogen peroxide),是过氧化氢的水溶液,即过氧化氢和水形成的混合物,请从微观角度解释其为混合物的原因________ 。双氧水分医用、军用和工业用三种,日常消毒的是医用双氧水,其浓度等于或低于3%,使用双氧水消毒的时候会有小气泡产生是因为双氧水遇见手指上灰尘、脏物也会分解,分解生成水和________ 。
小虹同学对家里久置的医用双氧水生了浓厚的兴趣,想利用其制取氧气,于是查阅资料。
【查阅资料】
①在常温下过氧化氢的溶液会缓慢分解,请写出此反应的符号表达式________ 。
②加快其反应速度的办法是加入催化剂或用短波射线照射。
小虹对瓶中久置后液体成分又提出了猜想,与小桥展开讨论。
【提出问题】剩余液体的成分是什么?
【猜想与假设】小虹猜想:水、过氧化氢;小桥猜想:________ 。
【设计与实验】为了验证液体的成分,小组同学设计了实验,请你参与并完成下列表格。
【总结与反思】药品在久置的过程中可能会变质,我们要善于利用学过的知识分析问题,解决问题。
小虹同学对家里久置的医用双氧水生了浓厚的兴趣,想利用其制取氧气,于是查阅资料。
【查阅资料】
①在常温下过氧化氢的溶液会缓慢分解,请写出此反应的符号表达式
②加快其反应速度的办法是加入催化剂或用短波射线照射。
小虹对瓶中久置后液体成分又提出了猜想,与小桥展开讨论。
【提出问题】剩余液体的成分是什么?
【猜想与假设】小虹猜想:水、过氧化氢;小桥猜想:
【设计与实验】为了验证液体的成分,小组同学设计了实验,请你参与并完成下列表格。
| 实验方法 | 实验现象 | 实验结论 |
| 取瓶中的剩余液体放入试管中 | 小桥的猜想是正确的 |
您最近一年使用:0次
【推荐2】常温下过氧化氢分解生成氧气的速率较缓慢,研究性学习小组选择“过氧化氢分解生成氧气的快慢与什么因素有关”的课题进行探究,以下他们探究的主要过程。
【提出假设】催化剂的种类会影响过氧化氢分解生成氧气的快慢。
供选择的试剂:5%过氧化氢溶液,15%过氧化氢溶液,30%过氧化氢溶液,二氧化锰粉末,氧化铜粉末。
【设计方案】常温下取两份5%的过氧化氢溶液各100毫升,分别加入______ ,测量生成一瓶相同体积氧气所需的时间。
【实验探究】如图1所示,是他们进行实验的装置图,此实验中,A处应当采用的气体收集方法是______ 。检查装置气密性良好,将分液漏斗中液体加入锥形瓶中,收集立即收集一瓶气体,并记录所用时间。

【实验记录】
【实验分析】若要证明二氧化锰、氧化铜是该反应的催化剂,还需要验证他们在化学反应前后的______ 和______ 没有改变。
【得出结论】该探究过程得出的结论是______ ,实验室用过氧化氢溶液制取氧气的化学方程式为______ 。
【提出假设】催化剂的种类会影响过氧化氢分解生成氧气的快慢。
供选择的试剂:5%过氧化氢溶液,15%过氧化氢溶液,30%过氧化氢溶液,二氧化锰粉末,氧化铜粉末。
【设计方案】常温下取两份5%的过氧化氢溶液各100毫升,分别加入
【实验探究】如图1所示,是他们进行实验的装置图,此实验中,A处应当采用的气体收集方法是

【实验记录】
实验编号 | 1 | 2 |
反应物 | 5%过氧化氢溶液100mL | 5%过氧化氢溶液100mL |
加入固体 | CuO | MnO2 |
收集一瓶气体所需时间 | 165S | 46S |
【得出结论】该探究过程得出的结论是
您最近一年使用:0次
【推荐3】学校化学兴趣小组的同学知道二氧化锰能作过氧化氢分解的催化剂以后,想再探究其他一些物质如三氧化二铝是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白:
(1)〔问题〕Al2O3能不能作过氧化氢分解的催化剂呢?
(2)〔猜想〕Al2O3能作过氧化氢分解的催化剂。
(3)〔实验验证〕
(4)〔结论〕Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂。
(5)〔讨论与反思〕经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验(实验三):
〔实验目的〕 探究________ 。
〔实验步骤〕①准确称量少量Al2O3 的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、烘干、________ ;④反应前后进行对比。
〔讨论〕如果Al2O3在反应前后_______ 不变,也不能说明Al2O3可以作过氧化氢分解的催化剂。理由是还应设计实验:探究Al2O3的_______ 性质是否发生变化。
(1)〔问题〕Al2O3能不能作过氧化氢分解的催化剂呢?
(2)〔猜想〕Al2O3能作过氧化氢分解的催化剂。
(3)〔实验验证〕
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 木条不复燃 | 常温下过氧化氢溶液的分解速率很慢 | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,将带火星的木条伸入试管中 | 木条复燃 | Al2O3能加快过氧化氢的分解速率 |
(4)〔结论〕Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂。
(5)〔讨论与反思〕经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验(实验三):
〔实验目的〕 探究
〔实验步骤〕①准确称量少量Al2O3 的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、烘干、
〔讨论〕如果Al2O3在反应前后
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】自然界并不缺少“镁”,而是缺少发现“镁”的眼睛。某化学兴趣小组开启寻“镁”之旅,现邀请你一起进行项目式学习。
任务一:初步认识镁
(1)镁的物理性质:__________ (写出一点)。
(2)镁的部分化学性质:将打磨后的镁条在空气中点燃,化学方程式是____________ 。
任务二:揭开镁表面变黑的奥秘
(3)镁条在空气中放置一段时间后表面形成黑色。小芳认为黑色物质是MgO,根据所学的知识,MgO是__________ 色固体,查阅资料得知该黑色固体的主要成分是Mg2(OH)2CO3,这可能是Mg与空气中的O2、CO2和__________ (填化学式)反应生成的。
(4)设计实验方案如下图,一段时间后,A中镁条表面变黑,B、C、D中镁条表面均无明显变化。
下列有关说法正确的是__________ (填序号)

①A和B对比的目的是探究镁条表面形成Mg2(OH)2CO3,是否与O2有关
②A和C对比的目的是探究镁条表面形成Mg2(OH)2CO3,是否与CO2有关
③A、B、D中的蒸馏水可以用自来水代替
④C中的干燥剂可以是氢氧化钠固体
任务三:利用镁验证质量守恒定律
(5)项目小组同学分别利用镁在空气中燃烧来验证质量守恒定律。镁条点燃后实验现象如图所示,待完全燃烧后:

①小明称量得到石棉网上留下的固体质量比反应前镁条的质量小,其原因可能是___________ 。
②小刚称量得到石棉网上留下的固体质量比反应前镁条的质量大,其原因可能是___________ 。
③小芳称量得到石棉网上留下的固体质量与反应前镁条的质量相等,她的实验__________ (填“能”或“不能”)证明化学反应前后质量守恒。
任务一:初步认识镁
(1)镁的物理性质:
(2)镁的部分化学性质:将打磨后的镁条在空气中点燃,化学方程式是
任务二:揭开镁表面变黑的奥秘
(3)镁条在空气中放置一段时间后表面形成黑色。小芳认为黑色物质是MgO,根据所学的知识,MgO是
(4)设计实验方案如下图,一段时间后,A中镁条表面变黑,B、C、D中镁条表面均无明显变化。
下列有关说法正确的是

①A和B对比的目的是探究镁条表面形成Mg2(OH)2CO3,是否与O2有关
②A和C对比的目的是探究镁条表面形成Mg2(OH)2CO3,是否与CO2有关
③A、B、D中的蒸馏水可以用自来水代替
④C中的干燥剂可以是氢氧化钠固体
任务三:利用镁验证质量守恒定律
(5)项目小组同学分别利用镁在空气中燃烧来验证质量守恒定律。镁条点燃后实验现象如图所示,待完全燃烧后:

①小明称量得到石棉网上留下的固体质量比反应前镁条的质量小,其原因可能是
②小刚称量得到石棉网上留下的固体质量比反应前镁条的质量大,其原因可能是
③小芳称量得到石棉网上留下的固体质量与反应前镁条的质量相等,她的实验
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】兴趣小组在课外实验中意外发现:将镁条放入Na2CO3溶液中,快速产生较多气泡,有白色沉淀生成。小组同学对此进行了系列探究活动。
【探究1】:反应产生的气体是什么?
【作出猜想】作出如下猜想:①氢气;②二氧化碳;③氢气和二氧化碳。
【实验1】取适量镁条、100 mL Na2CO3溶液于反应装置A中,按如图所示方案进行实验,B中石灰水不变浑浊;C处气体燃烧,烧杯内壁有水珠。说明猜想_____ 正确。
小组同学讨论认为,上述实验中“烧杯内壁有水珠”作为“反应产生的气体是氢气”的证据不可靠。为使这一证据可靠,且仍能一次性地验证三个猜想,只需在图所示方案的基础上加以改进完善。你的改进方案是_________ 。
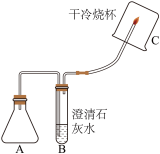
【探究Ⅱ】:快速产生气体的原因是什么?
【查阅资科】镁与水缓慢反应生成氢气:Na2CO3溶液显碱性,其溶液中除Na+、CO32﹣外,还有OH-。
【作出猜想】可能是Na2CO3溶液中的某一种离子促进了镁与水的反应。
【实验2】按图2所示方案进行实验。G、I中缓慢产生气泡,H中快速产生较多气泡,说明是CO32﹣而不是Na+、OH﹣促进了镁与水的反应。

(1)G中实验的作用是_________ 。
(2)试剂X是_________ 。
探究Ⅲ:反应产生的白色沉淀中是否含有MgCO3?
【实验3】取实验1反应生成的沉淀于试管中,加入试剂Y,根据实验现象说明白色沉淀中含有MgCO3。试剂Y及实验现象为______ ,该化学反应的基本类型_______ 。
反思交流:有些伟大的发现就是从异常现象中得到启发,通过深入研究而实现的。
【探究1】:反应产生的气体是什么?
【作出猜想】作出如下猜想:①氢气;②二氧化碳;③氢气和二氧化碳。
【实验1】取适量镁条、100 mL Na2CO3溶液于反应装置A中,按如图所示方案进行实验,B中石灰水不变浑浊;C处气体燃烧,烧杯内壁有水珠。说明猜想
小组同学讨论认为,上述实验中“烧杯内壁有水珠”作为“反应产生的气体是氢气”的证据不可靠。为使这一证据可靠,且仍能一次性地验证三个猜想,只需在图所示方案的基础上加以改进完善。你的改进方案是

【探究Ⅱ】:快速产生气体的原因是什么?
【查阅资科】镁与水缓慢反应生成氢气:Na2CO3溶液显碱性,其溶液中除Na+、CO32﹣外,还有OH-。
【作出猜想】可能是Na2CO3溶液中的某一种离子促进了镁与水的反应。
【实验2】按图2所示方案进行实验。G、I中缓慢产生气泡,H中快速产生较多气泡,说明是CO32﹣而不是Na+、OH﹣促进了镁与水的反应。

(1)G中实验的作用是
(2)试剂X是
探究Ⅲ:反应产生的白色沉淀中是否含有MgCO3?
【实验3】取实验1反应生成的沉淀于试管中,加入试剂Y,根据实验现象说明白色沉淀中含有MgCO3。试剂Y及实验现象为
反思交流:有些伟大的发现就是从异常现象中得到启发,通过深入研究而实现的。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】在二氧化锰的催化作用下,过氧化氢迅速分解生成氧气和水。哪些因素还影响着过氧化氢分解的速率?课外活动小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
请你设计:实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
探究实验一:浓度对化学反应速率的影响
| 实验步骤 | 现象 | 结论 |
取一支试管加入3 5mL5%的过氧化氢溶液,然后加入少量二氧化锰。 5mL5%的过氧化氢溶液,然后加入少量二氧化锰。 | 缓慢有少量气泡冒出 | |
另取一支试管加入3 5mL15%的过氧化氢溶液,然后加入少量二氧化锰。 5mL15%的过氧化氢溶液,然后加入少量二氧化锰。 | 迅速有大量气泡冒出 |
探究实验二:温度对化学反应速率的影响
| 实验步骤 | 现象 | 结论 |
取一支试管加入3 5mL5%的过氧化氢溶液,然后放入 5mL5%的过氧化氢溶液,然后放入 | 温度越高,过氧化氢分解的速率越大 | |
取一支试管加入3 5mL5%的过氧化氢溶液,然后放入 5mL5%的过氧化氢溶液,然后放入 |
您最近一年使用:0次
【推荐1】催化剂的相关研究是一项重要的课题,某小组以“探究催化剂的奥秘”为题展开了学习。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,其_______ 和_______ 在化学反应前后都不变。
【任务二】探究催化剂

(2)小组同学查阅资料发现氧化铜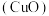 也可作为过氧化氢分解的催化剂,于是设计了上图实验进行验证,请填写下表:
也可作为过氧化氢分解的催化剂,于是设计了上图实验进行验证,请填写下表:
(3)步骤______的现象对比可以证明氧化铜能够加快过氧化氢的分解速率。
(4)写出实验室用过氧化氢溶液制取氧气反应的符号表达式_______ 。
【任务三】探究不同催化剂的催化效果
小组同学以生成 氧气为标准,设计了下列实验。
氧气为标准,设计了下列实验。
(5)表中的待测数据是收集相向体积的氧气所需要的时间,若 ,可得到的结论是
,可得到的结论是_______ 的催化效果较好。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,其
【任务二】探究催化剂

(2)小组同学查阅资料发现氧化铜
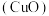 也可作为过氧化氢分解的催化剂,于是设计了上图实验进行验证,请填写下表:
也可作为过氧化氢分解的催化剂,于是设计了上图实验进行验证,请填写下表:| 步骤①现象 | 步骤③现象 | 步骤⑥结果 | 实验结论 |
| 无明显现象 | 试管中有气泡产生,带火星的木条 | 氧化铜的质量为 | 氧化铜是过氧化氢分解的催化剂 |
(3)步骤______的现象对比可以证明氧化铜能够加快过氧化氢的分解速率。
| A.②③ | B.①③ |
(4)写出实验室用过氧化氢溶液制取氧气反应的符号表达式
【任务三】探究不同催化剂的催化效果
小组同学以生成
 氧气为标准,设计了下列实验。
氧气为标准,设计了下列实验。| 序号 | 5% 溶液的体积 溶液的体积 | 催化剂 | 待测数据 |
| ① |  |  氧化铜 氧化铜 | a |
| ② |  |  二氧化锰 二氧化锰 | b |
(5)表中的待测数据是收集相向体积的氧气所需要的时间,若
 ,可得到的结论是
,可得到的结论是
您最近一年使用:0次
【推荐2】某中学化学兴趣小组的同学们进行有关分子性质的探究实验如下:
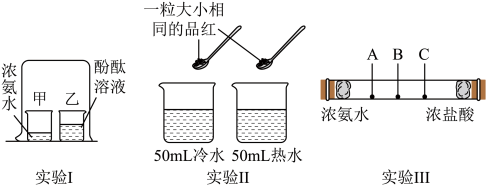
(1)实验I中,观察到烧杯_______ (填“甲”或“乙”)内液体变红色,可证明分子在不断运动。
(2)为何实验I中另一烧杯内液体不变红色,某同学提出可能与分子运动速率有关。
探究一:分子运动速率与温度的关系
实验Ⅱ中,观察品红扩散速度可得出:温度越高,分子运动越_______ (填“快”或“慢”)。
探究二:分子运动速率与分子质量的关系
【猜想假设】猜想1:分子质量越小,分子运动越快:
猜想2:分子质量越小,分子运动越慢。
【查阅资料】①浓盐酸会挥发出氯化氢(HCl)气体,浓氨水会挥发出氨气(NH3),两种气体反应会产生白烟,即生成新物质氯化铵(NH4Cl):
②氯化氢(HCl)分子质量大于氨气(NH3)分子质量。
【设计实验】
【反思交流】
①实验Ⅲ中,生成物氯化铵(NH4Cl)常温下的状态是_______ (填“固体”、“液体”或“气体”)。
②实验I中,另一烧杯内液体不变红色,是因为_______ (填“酚酞”或“氨气”)的分子质量很大。
③从研究分子性质角度,实验Ⅲ较实验I的优点是_______ (填序号)。
A.可证明分子间有间隔 B.可证明分子的质量和体积都很小
C.节约药品,操作简单 D.可证明分子运动与温度有关

(1)实验I中,观察到烧杯
(2)为何实验I中另一烧杯内液体不变红色,某同学提出可能与分子运动速率有关。
探究一:分子运动速率与温度的关系
实验Ⅱ中,观察品红扩散速度可得出:温度越高,分子运动越
探究二:分子运动速率与分子质量的关系
【猜想假设】猜想1:分子质量越小,分子运动越快:
猜想2:分子质量越小,分子运动越慢。
【查阅资料】①浓盐酸会挥发出氯化氢(HCl)气体,浓氨水会挥发出氨气(NH3),两种气体反应会产生白烟,即生成新物质氯化铵(NH4Cl):
②氯化氢(HCl)分子质量大于氨气(NH3)分子质量。
【设计实验】
| 步骤 | 现象 | 结论 |
| 组装实验Ⅲ装置,在玻璃管左右两端分别放置沾有浓氨水和浓盐酸的棉花,观察现象。 | 玻璃管 | 猜想1正确 |
①实验Ⅲ中,生成物氯化铵(NH4Cl)常温下的状态是
②实验I中,另一烧杯内液体不变红色,是因为
③从研究分子性质角度,实验Ⅲ较实验I的优点是
A.可证明分子间有间隔 B.可证明分子的质量和体积都很小
C.节约药品,操作简单 D.可证明分子运动与温度有关
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组的同学对实验室里久置于空气中已变质的过氧化钠(Na2O2)固体的成分进行探究。
【查阅资料】
(1)过氧化钠化学性质很活泼,能与水、二氧化碳反应。
相关化学方程式为: ;
;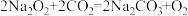
(2)Ba(NO3)2溶液、NaNO3溶液均为中性溶液。
【猜想与假设】猜想I:固体为Na2O2、NaOH、Na2CO3
猜想Ⅱ:固体为NaOH、Na2CO3
猜想Ⅲ:固体为NaOH
猜想IV:固体为Na2CO3
【实验推断】
【查阅资料】
(1)过氧化钠化学性质很活泼,能与水、二氧化碳反应。
相关化学方程式为:
 ;
;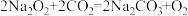
(2)Ba(NO3)2溶液、NaNO3溶液均为中性溶液。
【猜想与假设】猜想I:固体为Na2O2、NaOH、Na2CO3
猜想Ⅱ:固体为NaOH、Na2CO3
猜想Ⅲ:固体为NaOH
猜想IV:固体为Na2CO3
【实验推断】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体于试管中,加水振荡直至完全溶解 | 猜想一不成立 | |
| ②取少量①的溶液于试管中,滴加过量的Ba(NO3)2溶液 | 产生白色沉淀 | 证明有 |
| ③取少量②的溶液于试管中,滴加无色酚酞 | 溶液变红 | 证明有NaOH存在 |
| 综合以上实验现象,说明猜想Ⅱ是成立的 | ||
您最近一年使用:0次



