金属蚀刻是利用金属与蚀刻剂发生反应,形成所需图案的工艺。化学兴趣小组的同学对金属蚀刻画的制作进行了如下探究。
【交流讨论】
(1)同学们通过交流认为:如果使用银板,则不能选择稀盐酸或稀硫酸作蚀刻液,原因是___________ 。
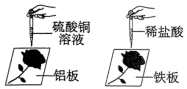
【实验1】小组同学选用两个金属板,将金属板打磨并贴上保护膜后刻画出“玫瑰花”图案,再对裸露出金属板的“玫瑰花”进行如图所示的“开花”操作。
(2)首先对金属板进行打磨,其目的是___________ 。
(3)所得铝板蚀刻画中“玫瑰花”的颜色为___________ 色。
(4)对蚀刻好的铁板进行冲洗,观察到冲洗后的废液呈浅绿色,则废液中一定含有的溶质是___________ 。
【提出问题】铁板蚀刻画清洗后的废液中是否还含有其他成分?
【作出猜想】废液中可能含有稀盐酸。
【实验2】同学们设计了如下方案进行探究:
【反思交流】
(5)方案I中发生反应的化学方程式为___________ 。
(6)同学们认为通过方案Ⅱ不能得出废液中含有稀盐酸的结论,理由是___________ 。
【交流讨论】
(1)同学们通过交流认为:如果使用银板,则不能选择稀盐酸或稀硫酸作蚀刻液,原因是
【实验1】小组同学选用两个金属板,将金属板打磨并贴上保护膜后刻画出“玫瑰花”图案,再对裸露出金属板的“玫瑰花”进行如图所示的“开花”操作。
(2)首先对金属板进行打磨,其目的是
(3)所得铝板蚀刻画中“玫瑰花”的颜色为
(4)对蚀刻好的铁板进行冲洗,观察到冲洗后的废液呈浅绿色,则废液中一定含有的溶质是
【提出问题】铁板蚀刻画清洗后的废液中是否还含有其他成分?
【作出猜想】废液中可能含有稀盐酸。
【实验2】同学们设计了如下方案进行探究:
| 实验方案 | 实验现象 | 实验结论 |
| I.取少量氧化铁于试管中,向其中加入足量废液 | 红棕色固体消失 | 废液中含有稀盐酸 |
| Ⅱ.另取少量废液于试管中,滴加几滴硝酸银溶液 | 有白色沉淀生成 |
(5)方案I中发生反应的化学方程式为
(6)同学们认为通过方案Ⅱ不能得出废液中含有稀盐酸的结论,理由是
更新时间:2024-05-23 23:51:05
|
相似题推荐
科学探究题
|
适中
(0.65)
名校
【推荐1】创新能力是现代经济社会发展对学生提出的最迫切要求。如图一是教材探究燃烧的条件的原型实验,图二、图三是某学生的创新实验:
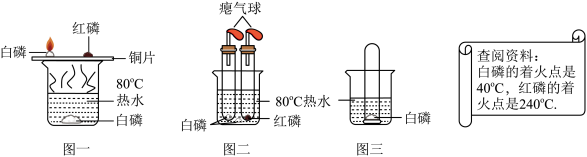
图一中热水在此实验中的作用有下列说法,其中正确的是________________ 。
①隔绝空气 ②加热使铜片温度升高
A.只有① B.只有② C.是①和②
(2) 欲使图二中的红磷燃烧,可将试管从水中取出,擦干后进行加热;红磷燃烧的化学方程式为_______________ 。
(3) 将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三),结果观察到了“水火相容”的奇观,则大试管所装气体可能是_____________________ 。
(4) 下列是同学们对该创新实验的判断和评价,你认为合理的是_____________ 。
A、改进后实验(图二)可防止生成物污染空气,更环保
B、改进后实验(图三)可防止白磷四处移动,实验效果更好
C、图二中气球没有任何作用

图一中热水在此实验中的作用有下列说法,其中正确的是
①隔绝空气 ②加热使铜片温度升高
A.只有① B.只有② C.是①和②
(2) 欲使图二中的红磷燃烧,可将试管从水中取出,擦干后进行加热;红磷燃烧的化学方程式为
(3) 将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三),结果观察到了“水火相容”的奇观,则大试管所装气体可能是
(4) 下列是同学们对该创新实验的判断和评价,你认为合理的是
A、改进后实验(图二)可防止生成物污染空气,更环保
B、改进后实验(图三)可防止白磷四处移动,实验效果更好
C、图二中气球没有任何作用
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计实验探究:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】①氢氧化钠能与CO2反应但不产生沉淀,实验时常用于除CO2②白色无水CuSO4粉末遇水变蓝色③CO与人体内的血红蛋白结合会造成人中毒缺氧。
【猜想与假设】
猜想一:CO2、H2O
猜想二:CO、H2O
猜想三:_____
【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:
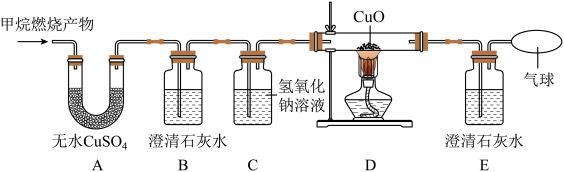
(1)实验过程中观察到A中白色粉末变为蓝色,B、E中澄清石灰水变浑浊,D中黑色粉末变成红色,由此推断猜想_____ 成立。
(2)实验过程中B装置的作用是_____ 。
(3)D装置中发生反应的化学方程式是_____ 。
(4)实验过程中用纯净O2而不用空气的原因是_____ 。
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】①氢氧化钠能与CO2反应但不产生沉淀,实验时常用于除CO2②白色无水CuSO4粉末遇水变蓝色③CO与人体内的血红蛋白结合会造成人中毒缺氧。
【猜想与假设】
猜想一:CO2、H2O
猜想二:CO、H2O
猜想三:
【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:

(1)实验过程中观察到A中白色粉末变为蓝色,B、E中澄清石灰水变浑浊,D中黑色粉末变成红色,由此推断猜想
(2)实验过程中B装置的作用是
(3)D装置中发生反应的化学方程式是
(4)实验过程中用纯净O2而不用空气的原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】妈妈和小昊在制作松软醇香的蛋糕时添加了一种单一膨松剂,小昊与同学们对家中的膨松剂进行下列探究。
【查阅资料】单一膨松剂的种类有:硫酸铝钾[KAl(SO4)2]、碳酸氢铵(俗称臭粉)、碳酸氢钠(俗名:______ )。膨松剂使面包松软的原理为制作过程中产生大量气体,如碳酸氢铵受热分解产生氨气、水和二氧化碳,该反应的化学方程式为______ 。
【进行实验】小昊将家中制作蛋糕的膨松剂带到实验室进行实验。
【拓展交流】为增强家中膨松剂的效果,可在制作过程中加入活性酵母,发酵过程中温度要控制在50℃以下,其目的是______ ;另外也可适量添加的物质为______ (填序号)。
A.氯化钠 B.食用油 C.食醋 D.淀粉
【查阅资料】单一膨松剂的种类有:硫酸铝钾[KAl(SO4)2]、碳酸氢铵(俗称臭粉)、碳酸氢钠(俗名:
【进行实验】小昊将家中制作蛋糕的膨松剂带到实验室进行实验。
实验步骤 | 实验现象 | 实验结论 |
步骤一:取少量膨松剂于试管中 并加水溶解,滴加稀盐酸 | 该膨松剂一定 不是硫酸铝钾 | |
步骤二:另取少量膨松剂于试管中并加水溶解, 再加入足量的氢氧化钠溶液,然后将一小片湿润的 红色石蕊试纸伸人试管中 | 有大量气泡产生,红色石 蕊试纸变为 | 该膨松剂是 |
【拓展交流】为增强家中膨松剂的效果,可在制作过程中加入活性酵母,发酵过程中温度要控制在50℃以下,其目的是
A.氯化钠 B.食用油 C.食醋 D.淀粉
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】钛(Ti)是一种重要的航天金属材料。某学习小组对三种金属Ti、Al、Cu的金属活动性顺序进行探究。过程如下:
(提出假设)A.Ti金属活动性比Al强,B.Al金属活动性比Ti强
(查阅资料)钛能与盐酸反应。
(实验设计)同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象。
(操作分析)三种金属加入盐酸前都先用砂布将表面擦光亮,其目的是_____ 。
(实验现象)
(实验结论)(1)原假设中_____ 不正确(填:“A”、“B”或“AB”)。
(2)三种金属的金属活动性由强到弱的顺序为____ 。
(结论应用)能否用铝制容器来盛装波尔多液(含硫酸铜),______ (填“能”或“否”),理由是______ (化学方程式表示)。
(拓展延伸)非金属单质也具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的从其盐溶液中置换出来,可发生下列反应:
Cl2+2NaBr=2NaCl+Br2;I2+Na2S=2NaI+S↓; Br2+2KI=2KBr+I2
(1)S、Cl2、I2、Br2活动性由强到弱顺序是_____ 。
(2)下列化学方程式书写错误的是______
A.Cl2+2NaI=2NaCl+I2 B.I2+2KBr=2KI+Br2
C.Br2+Na2S=2NaBr+S↓ D.Cl2+K2S=2KCl+S↓
(提出假设)A.Ti金属活动性比Al强,B.Al金属活动性比Ti强
(查阅资料)钛能与盐酸反应。
(实验设计)同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象。
(操作分析)三种金属加入盐酸前都先用砂布将表面擦光亮,其目的是
(实验现象)
| 金属 | Ti | A1 | Cu |
| 与盐酸反应现象 | 反应缓慢 | 反应剧烈 |
(实验结论)(1)原假设中
(2)三种金属的金属活动性由强到弱的顺序为
(结论应用)能否用铝制容器来盛装波尔多液(含硫酸铜),
(拓展延伸)非金属单质也具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的从其盐溶液中置换出来,可发生下列反应:
Cl2+2NaBr=2NaCl+Br2;I2+Na2S=2NaI+S↓; Br2+2KI=2KBr+I2
(1)S、Cl2、I2、Br2活动性由强到弱顺序是
(2)下列化学方程式书写错误的是
A.Cl2+2NaI=2NaCl+I2 B.I2+2KBr=2KI+Br2
C.Br2+Na2S=2NaBr+S↓ D.Cl2+K2S=2KCl+S↓
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某初中化学“魔法课堂”社团的活动丰富多彩,下面是他们围绕“神奇的金属”为主题的探究活动。
(1)活泼金属与酸的反应
【提出问题】锌与稀硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸溶液的浓度有关;b.可能与锌的形状有关。
【设计并实验】小兵用不同浓度的硫酸和不同形状的锌进行如下实验。
小兵用如图装置收集并测量氢气的体积,氢气应从______ (填c或f或g)管通入。要比较不同浓度的硫酸对反应快慢的影响,应选择的实验编号是______ 。
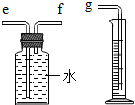
【评价与反思】下表是小兵第①组实验的详细数据。
请描述锌与硫酸2分钟以后反应速度变慢的原因:______ 。
(2)如图为Mn和CuSO4溶液反应的示意图,回答下列问题:

①实际与Mn反应的粒子是______ 。
②反应中失去电子的粒子是______ 。
③由反应可知金属的活泼性:Mn______ Cu(填“>”或“<”);
④该反应中化合价没有改变的元素或根是______ (填对应选项的字母)。
A.锰元素 B.铜元素 C.硫酸根
(1)活泼金属与酸的反应
【提出问题】锌与稀硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸溶液的浓度有关;b.可能与锌的形状有关。
【设计并实验】小兵用不同浓度的硫酸和不同形状的锌进行如下实验。
| 实验编号 | 硫酸的浓度(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |

【评价与反思】下表是小兵第①组实验的详细数据。
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
(2)如图为Mn和CuSO4溶液反应的示意图,回答下列问题:

①实际与Mn反应的粒子是
②反应中失去电子的粒子是
③由反应可知金属的活泼性:Mn
④该反应中化合价没有改变的元素或根是
A.锰元素 B.铜元素 C.硫酸根
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】学习完金属的化学性质,兴趣小组进行了如图所示的实验。

【实验一】同学们进行如图一所示的实验,验证铁、锌、铜、银四种金属活动性强弱。
(1)试管①中观察到的实验现象是铁粉表面有红色固体,溶液由______ 。
(2)试管③中反应的化学方程式是______ 。
(3)你认为通过上述图一所示的三个实验能否验证铁、锌、铜、银四种金属在溶液中的活动性强弱______ (填“能”或“不能”)。
【实验二】在完成实验一的过程中,同学们将试管①②③内反应后的物质都倒入废液缸中(如图二)。小组同学对废液缸中混合物的成分产生了探究兴趣。待混合物充分反应后,过滤,得到滤渣和浅绿色滤液。
(4)小明将铁丝放入浅绿色滤液中,一段时间后,铁丝表面没有发生变化。由此判断滤液中一定含有的溶质是______ (填化学式)。
(5)探究滤渣的成分
【提出问题】滤渣的成分是什么?
【作出猜想】小明的猜想:银、铜、铁、锌
你的猜想:猜想I______ ; 猜想II:银、铜、铁
【分析思考】同学们认为小明的猜想不正确,结合上述的实验现象分析,小明的猜想不正确的原因是______ 。(请用方程式解释)
【进行实验】实验证明猜想II正确,请你完成下列实验方案。
【拓展应用】
为继续研究金属的化学性质,学习小组同学向一定质量的硝酸银和硝酸铜的混合溶液中加入锌粉,溶液质量与加入锌的质量关系如图所示。那么,在b点时,溶液中存在的金属阳离子是______ (写离子符号);d点的固体的成分为______ (写名称)。


【实验一】同学们进行如图一所示的实验,验证铁、锌、铜、银四种金属活动性强弱。
(1)试管①中观察到的实验现象是铁粉表面有红色固体,溶液由
(2)试管③中反应的化学方程式是
(3)你认为通过上述图一所示的三个实验能否验证铁、锌、铜、银四种金属在溶液中的活动性强弱
【实验二】在完成实验一的过程中,同学们将试管①②③内反应后的物质都倒入废液缸中(如图二)。小组同学对废液缸中混合物的成分产生了探究兴趣。待混合物充分反应后,过滤,得到滤渣和浅绿色滤液。
(4)小明将铁丝放入浅绿色滤液中,一段时间后,铁丝表面没有发生变化。由此判断滤液中一定含有的溶质是
(5)探究滤渣的成分
【提出问题】滤渣的成分是什么?
【作出猜想】小明的猜想:银、铜、铁、锌
你的猜想:猜想I
【分析思考】同学们认为小明的猜想不正确,结合上述的实验现象分析,小明的猜想不正确的原因是
【进行实验】实验证明猜想II正确,请你完成下列实验方案。
| 实验步骤 | 实验现象 | 结论 |
| 取少量滤渣样品,加入稀盐酸。 | 有气泡,溶液变成浅绿色。 | 猜想 |
为继续研究金属的化学性质,学习小组同学向一定质量的硝酸银和硝酸铜的混合溶液中加入锌粉,溶液质量与加入锌的质量关系如图所示。那么,在b点时,溶液中存在的金属阳离子是

您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】为了探究金属活动性,将锌和铜放入稀硫酸中,铜不反应而锌的表面有气泡产生,写出锌和稀硫酸反应的化学方程式:_____ 。铜和稀硫酸虽然不反应,但铜和浓硫酸在加热的条件下却能反应且产生气体。对产生的气体成分有下列几种猜想。
猜想一:氢气; 猜想二:二氧化硫; 猜想三:氢气和二氧化硫的混合物。
【查阅资料】
(1)二氧化硫可以使品红溶液褪色。
(2)二氧化硫能和氢氧化钾溶液反应:SO2+2KOH=K2SO3+H2O。
(3)浓硫酸有吸水性,可以干燥某些气体。
【实验探究】师生设计了如下装置进行实验(部分仪器省略),请完成下列表格。
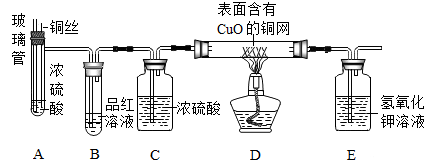
【表达交流】
(1)在步骤③中,鼓入空气的目的是_____ 。
(2)请完成铜与浓硫酸反应的化学方程式:Cu+2H2SO4(浓) CuSO4+SO2↑+
CuSO4+SO2↑+_____ 。
【反思拓展】
(3)若将装置A中铜丝换成锌片,随着反应的进行,硫酸的浓度逐渐变小,装置D玻璃管中看到的现象是_____ ,C装置的作用是:_____ 。
猜想一:氢气; 猜想二:二氧化硫; 猜想三:氢气和二氧化硫的混合物。
【查阅资料】
(1)二氧化硫可以使品红溶液褪色。
(2)二氧化硫能和氢氧化钾溶液反应:SO2+2KOH=K2SO3+H2O。
(3)浓硫酸有吸水性,可以干燥某些气体。
【实验探究】师生设计了如下装置进行实验(部分仪器省略),请完成下列表格。

| 主要实验步骤 | 主要现象 | 解释或结论 |
| ①加热装置A一段时间 | 装置B中的现象是 | 有二氧化硫生成 |
| ②点燃装置D处酒精灯 | 装置D玻璃管中无明显现象 | 猜想 |
| ③停止加热,将铜丝上提,向装置A中玻璃管鼓入空气 | ||
| ④冷却,将A中液体用水稀释 | A中液体变为 | 有硫酸铜生成 |
(1)在步骤③中,鼓入空气的目的是
(2)请完成铜与浓硫酸反应的化学方程式:Cu+2H2SO4(浓)
 CuSO4+SO2↑+
CuSO4+SO2↑+【反思拓展】
(3)若将装置A中铜丝换成锌片,随着反应的进行,硫酸的浓度逐渐变小,装置D玻璃管中看到的现象是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】金属在生产生活中用途广泛。某化学小组进行金属和酸反应的实验探究。
实验探究一:
(1)取形状、大小相同的纯锌片和纯铜片,用砂纸打磨,打磨的目的是_______ ,然后同时放入稀硫酸中,如图1所示。
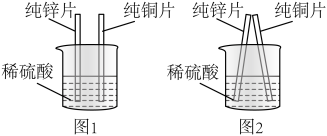
(2)图1观察到的现象是:锌片表面产生气泡,铜片表面_______ 。实验时甲同学不小心将两种金属片触碰到了一起(如图2),意外地发现铜片表面产生了气泡。
实验探究二:
【提出问题】图2中产生的气体是什么?铜是否发生了化学反应?
【作出猜想】猜想I:二氧化硫;猜想Ⅱ:氧气,猜想Ⅲ:氢气。
(3)提出以上猜想的依据是_______ 。
【查阅资料】①将锌片、铜片用导线连接后平行插入稀硫酸中,金属失去的电子通过导线发生了转移。
②二氧化硫能使品红溶液褪色。
(4)【进行实验】同学们将纯锌片和纯铜片用导线连接,放入装有稀硫酸的U形管中,铜片表面有气泡产生,在右侧导管口处检验生成的气体(如图3)。

①甲同学将生成的气体通入装有品红溶液的试管中,观察到_______ ;猜想Ⅰ不成立。
②乙同学将带火星木条放在右侧导管口,木条不复燃,猜想Ⅱ_______ (填“成立”或“不成立”)。
③丙同学将___ 放在右侧导管口,气体被点燃,猜想Ⅲ成立。写出气体燃烧的化学方程式___ 。
【教师释疑】图1实验中,锌与稀硫酸反应,锌失去电子,酸溶液中的H+在锌片表面获得电子生成H2。
【学生感悟】(5)图3实验中,酸溶液中的H+从铜片表面获得_______ (填“锌”或“铜”)失去的电子生成了H2。
【得出结论】图2中两种金属触碰后铜没有发生化学反应。
【延伸应用】(6)轮船是由钢铁制造的,易被海水侵蚀。船壳的吃水线以下会安装一定数量的某种金属块,让金属块被腐蚀来保护船壳。这种金属可以是_______ (填字母)。
A.锌 B.铜 C.银
实验探究一:
(1)取形状、大小相同的纯锌片和纯铜片,用砂纸打磨,打磨的目的是

(2)图1观察到的现象是:锌片表面产生气泡,铜片表面
实验探究二:
【提出问题】图2中产生的气体是什么?铜是否发生了化学反应?
【作出猜想】猜想I:二氧化硫;猜想Ⅱ:氧气,猜想Ⅲ:氢气。
(3)提出以上猜想的依据是
【查阅资料】①将锌片、铜片用导线连接后平行插入稀硫酸中,金属失去的电子通过导线发生了转移。
②二氧化硫能使品红溶液褪色。
(4)【进行实验】同学们将纯锌片和纯铜片用导线连接,放入装有稀硫酸的U形管中,铜片表面有气泡产生,在右侧导管口处检验生成的气体(如图3)。

①甲同学将生成的气体通入装有品红溶液的试管中,观察到
②乙同学将带火星木条放在右侧导管口,木条不复燃,猜想Ⅱ
③丙同学将
【教师释疑】图1实验中,锌与稀硫酸反应,锌失去电子,酸溶液中的H+在锌片表面获得电子生成H2。
【学生感悟】(5)图3实验中,酸溶液中的H+从铜片表面获得
【得出结论】图2中两种金属触碰后铜没有发生化学反应。
【延伸应用】(6)轮船是由钢铁制造的,易被海水侵蚀。船壳的吃水线以下会安装一定数量的某种金属块,让金属块被腐蚀来保护船壳。这种金属可以是
A.锌 B.铜 C.银
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某化学探究小组的同学从实验废液中回收铜,得到的铜样品中含有少量的铁粉。为测定样品中铜的质量分数,同学们按下述两种方案分别进行实验。
方案一:铜样品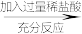 过滤,将得到的固体洗涤、干燥、称量。
过滤,将得到的固体洗涤、干燥、称量。
方案二:铜样品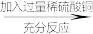 过滤,将得到的固体洗涤、干燥、称量
过滤,将得到的固体洗涤、干燥、称量
(1)请写出两个方案中发生反应的化学方程式:_____ ,______ 。
(2)方案一中反应进行完毕时的现象是_______ 。
(3)用上述两种方案进行实验都_____ (填“能”或“不能”)测得样品中铜的质量分数,理由是_____ 。
(4)将一定质量氧化铜加入稀硫酸中完全溶解后,再加入铁粉充分反应,过滤,再将滤渣加入足量稀硫酸中,有气泡冒出,充分反应后,剩余固体物质的质量为6.4 g,原氧化铜的质量为______ g。
方案一:铜样品
 过滤,将得到的固体洗涤、干燥、称量。
过滤,将得到的固体洗涤、干燥、称量。方案二:铜样品
 过滤,将得到的固体洗涤、干燥、称量
过滤,将得到的固体洗涤、干燥、称量(1)请写出两个方案中发生反应的化学方程式:
(2)方案一中反应进行完毕时的现象是
(3)用上述两种方案进行实验都
(4)将一定质量氧化铜加入稀硫酸中完全溶解后,再加入铁粉充分反应,过滤,再将滤渣加入足量稀硫酸中,有气泡冒出,充分反应后,剩余固体物质的质量为6.4 g,原氧化铜的质量为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】实验室里,同学完成了粗盐提纯实验后,得到了白色固体,于老师提出白色固体中除了NaCl外,还含有CaCl2 MgCl2 和Na2SO4,于是十七同学继续实验,提纯氯化钠。
【提出问题】如何除去三种可溶性杂质获得纯净的NaCl
于老师提供药品:A:Na2CO3溶液;B:NaOH溶液;C:BaCl2溶液;D:稀盐酸
【实验探究】
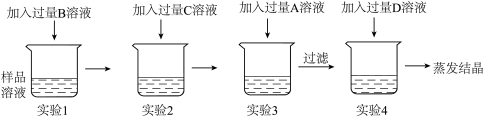
【表达交流】
(1)实验1的反应现象:_______ ;
实验2发生的化学方程式_______ ;
实验3 A溶液过量的目的_______ ;
实验4在滴加过量的D溶液的过程中,下图a表示的是_______ (填符号)。
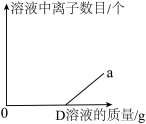
【实验结论】
(2)同学_______ (填“能”或“不能”)达到除杂目的。
【总结归纳】
(3)除去样品中三种可溶性杂质顺序还可以是_______ (填序号字母),过滤,再加过量的D溶液,蒸发结晶即可得到纯净的NaCl。通过上述实验,启示我们除去混合物溶液中的多种杂质时,加入除杂试剂时应注意_______ 。且不能引入新的杂质(离子)。
【提出问题】如何除去三种可溶性杂质获得纯净的NaCl
于老师提供药品:A:Na2CO3溶液;B:NaOH溶液;C:BaCl2溶液;D:稀盐酸
【实验探究】

【表达交流】
(1)实验1的反应现象:
实验2发生的化学方程式
实验3 A溶液过量的目的
实验4在滴加过量的D溶液的过程中,下图a表示的是

【实验结论】
(2)同学
【总结归纳】
(3)除去样品中三种可溶性杂质顺序还可以是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】pH-12的溶液中可能含有Fe3+、K+、SO42- 、CO32-、NO3-等离子中的一种或几种,为了检验该溶液中含有的离子,进行如下实验并分析:
(1)该溶液pH= 12,证明不存在的离子是_____ 。
(2)取少量该溶液于试管中,滴加适量氯化钡溶液,产生白色沉淀,再加入过量的稀盐酸,沉淀部分溶解。写出沉淀溶解的化学方程式:_____ 。
(3)该溶液中一定存在的离子是_____ ,可能存在的离子是_____ 。
(1)该溶液pH= 12,证明不存在的离子是
(2)取少量该溶液于试管中,滴加适量氯化钡溶液,产生白色沉淀,再加入过量的稀盐酸,沉淀部分溶解。写出沉淀溶解的化学方程式:
(3)该溶液中一定存在的离子是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】同学们为探究氢氧化钙的化学性质,取少量氢氧化钙溶液于四支试管中,做了如下实验:
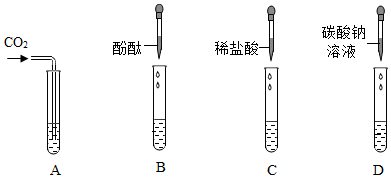
(1)A种观察到的现象是______ ,B中观察到的现象是______ 。
(2)D中反应后溶液显______ (填“酸性”“碱性”或“中性”)。
(3)C中反应的化学方程式为______ 。
实验结束后,小组同学把A、D试管中反应后的废液倒入同一个烧杯中,观察到沉淀明显增多,将沉淀过滤得到无色滤液。同学们对所得无色滤液中溶质成分进行了探究。
【提出问题】所得无色滤液中溶质成分是什么?
【猜想】猜想Ⅰ:NaOH 猜想Ⅱ:NaOH和Na2CO3 猜想Ⅲ:______ 。
【实验探究】

(1)A种观察到的现象是
(2)D中反应后溶液显
(3)C中反应的化学方程式为
实验结束后,小组同学把A、D试管中反应后的废液倒入同一个烧杯中,观察到沉淀明显增多,将沉淀过滤得到无色滤液。同学们对所得无色滤液中溶质成分进行了探究。
【提出问题】所得无色滤液中溶质成分是什么?
【猜想】猜想Ⅰ:NaOH 猜想Ⅱ:NaOH和Na2CO3 猜想Ⅲ:
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量所得无色滤液于试管中,加足量稀盐酸 | 无明显现象 | 猜想 |
| ②另取少量所得无色滤液于试管中,加适量碳酸钠溶液 | 猜想Ⅲ正确 |
您最近一年使用:0次



