生活处处皆化学,厨房中蕴含着许多化学知识。
(1)厨房中常见到的下列物质中,可溶于水形成溶液的是___________ 。
a.面粉 b.芝麻油 c.白砂糖 d.鸡蛋壳
(2)山药中含有碱性皂角素,皮肤沾上会奇痒难忍,可涂抹食醋来止痒,这是因为食醋中含有较多的___________ 离子。
(3)用铁锅将饭煮熟,主要是利用了金属铁的___________ 性,同时还可补充人体所需的铁元素,若铁元素摄入量过少,会导致的疾病是___________ 。
(4)家用燃气为天然气,天然气主要成分燃烧的化学方程式为___________ 。
若炒菜时油锅不慎着火,可用锅盖盖灭,其灭火原理是什么___________ ?
若在厨房中闻到了燃气逸出的气味,首先应该采取安全措施是什么?___________
(5)焙制糕点所用发酵粉的主要成分是小苏打,小苏打受热时会发生分解反应,生成碳酸钠、水和二氧化碳。为测定某发酵粉中小苏打的含量,取12g发酵粉充分加热至质量不再减少(假设其他物质不反应),冷却称量剩余固体物质质量为8.9g,试计算该发酵粉中含小苏打的质量分数。
(1)厨房中常见到的下列物质中,可溶于水形成溶液的是
a.面粉 b.芝麻油 c.白砂糖 d.鸡蛋壳
(2)山药中含有碱性皂角素,皮肤沾上会奇痒难忍,可涂抹食醋来止痒,这是因为食醋中含有较多的
(3)用铁锅将饭煮熟,主要是利用了金属铁的
(4)家用燃气为天然气,天然气主要成分燃烧的化学方程式为
若炒菜时油锅不慎着火,可用锅盖盖灭,其灭火原理是什么
若在厨房中闻到了燃气逸出的气味,首先应该采取安全措施是什么?
(5)焙制糕点所用发酵粉的主要成分是小苏打,小苏打受热时会发生分解反应,生成碳酸钠、水和二氧化碳。为测定某发酵粉中小苏打的含量,取12g发酵粉充分加热至质量不再减少(假设其他物质不反应),冷却称量剩余固体物质质量为8.9g,试计算该发酵粉中含小苏打的质量分数。
2024·河南商丘·三模 查看更多[2]
更新时间:2024-06-18 14:48:12
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】在实验室中可选择下图装置制取气体。
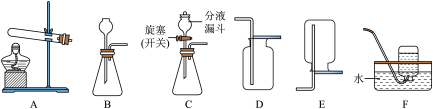
(1)若选择A、F组合一套装置制取了某气体,请写出有关反应的化学方程式:_________ 。
(2)选择C、F组合一套装置也可制取上述气体,请写出有关反应的化学方程式:________ 。
(3)若用金属锌与硫酸反应来制取氢气,发生装置可选择____ (填字母);收集装置可选择_____ (填字母);实验室制取氢气反应的化学方程式为__________ 。
(4)氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。在实验室常用氯化铵固体与碱石灰固体共同加热制取氨气。实验室制取氨气的发生装置应选择装置______ (填字母),收集装置应选择装置_____ (填字母)。
(5)为测定某石灰石样品中碳酸钙的质量分数,称取10g石灰石(杂质不参加反应)放入烧杯中,加入100g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为106.7g。请计算该样品中碳酸钙的质量分数。

(1)若选择A、F组合一套装置制取了某气体,请写出有关反应的化学方程式:
(2)选择C、F组合一套装置也可制取上述气体,请写出有关反应的化学方程式:
(3)若用金属锌与硫酸反应来制取氢气,发生装置可选择
(4)氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。在实验室常用氯化铵固体与碱石灰固体共同加热制取氨气。实验室制取氨气的发生装置应选择装置
(5)为测定某石灰石样品中碳酸钙的质量分数,称取10g石灰石(杂质不参加反应)放入烧杯中,加入100g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为106.7g。请计算该样品中碳酸钙的质量分数。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】金属及其化合物与人们的生产、生活密切相关。
(1)如图是的在元素周期表中的信息及原子结构示意图,下列说法错误的是 。(填字母)

(2)铁制品非常容易生锈,严重影响了使用和美观。铁生锈的原因是铁与空气中的________ 同时反应;写出一种在生活中防止铁制品生锈的方法:________ 。
(3)铁在自然界中以化合物的形式存在。实验室利用如图装置炼铁。
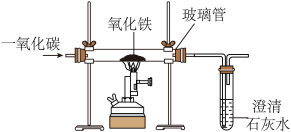
①写出玻璃管内发生反应的化学方程式________ 。
②写出一种尾气处理方法________ 。
(4)将一定量的锌粉加入硝酸银和硝酸铜的混合溶液中,充分反应后过滤,得到滤液和滤渣。
①向滤渣中加入稀盐酸,有气泡冒出,写出滤渣中含有的成分________ 。
②写出会使溶液质量增大的反应的化学方程式________ 。
(5)25g石灰石与一定质量的稀盐酸恰好完全反应(杂质与盐酸不反应,也不溶于水),生成8.8g二氧化碳,求该石灰石中碳酸钙的质量分数?
(1)如图是的在元素周期表中的信息及原子结构示意图,下列说法错误的是 。(填字母)

| A.钠原子的质子数为11 |
| B.钠的相对原子质量为22.99g |
| C.钠位于元素周期表第三周期 |
| D.钠原子在化学变化中易失去电子 |
(2)铁制品非常容易生锈,严重影响了使用和美观。铁生锈的原因是铁与空气中的
(3)铁在自然界中以化合物的形式存在。实验室利用如图装置炼铁。

①写出玻璃管内发生反应的化学方程式
②写出一种尾气处理方法
(4)将一定量的锌粉加入硝酸银和硝酸铜的混合溶液中,充分反应后过滤,得到滤液和滤渣。
①向滤渣中加入稀盐酸,有气泡冒出,写出滤渣中含有的成分
②写出会使溶液质量增大的反应的化学方程式
(5)25g石灰石与一定质量的稀盐酸恰好完全反应(杂质与盐酸不反应,也不溶于水),生成8.8g二氧化碳,求该石灰石中碳酸钙的质量分数?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】小柯为了测定某钙片中碳酸钙的质量分数,用如图甲装置进行如下实验

①取研碎后的钙片4克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置的总质量275.58g。
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置的总质量274.7g。(钙片中其它成分不与盐酸反应)
③整理相关数据并画出了如图乙总质量随时间变化的曲线A。
实验评价:
(1)该实验中,对装置中的固态干燥剂的性质有何要求?_____ 。
(2)忽略反应前后容器内的气体质量差,结合实验数据,则该钙片中碳酸钙的质量分数_____ 。
(3)小敏进行同样的实验,忘记了将4克钙片碾碎。实验过程中,他画出了总质量随时间变化的曲线B.分析乙图,钙片和稀盐酸反应快慢与哪两个因素有关?_____ 。

①取研碎后的钙片4克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置的总质量275.58g。
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置的总质量274.7g。(钙片中其它成分不与盐酸反应)
③整理相关数据并画出了如图乙总质量随时间变化的曲线A。
实验评价:
(1)该实验中,对装置中的固态干燥剂的性质有何要求?
(2)忽略反应前后容器内的气体质量差,结合实验数据,则该钙片中碳酸钙的质量分数
(3)小敏进行同样的实验,忘记了将4克钙片碾碎。实验过程中,他画出了总质量随时间变化的曲线B.分析乙图,钙片和稀盐酸反应快慢与哪两个因素有关?
您最近一年使用:0次
【推荐1】水和溶液在城市建设、生产生活中应用广泛。
Ⅰ、水——生命的源泉
(1)电解水的实验说明水是由______ (填元素符号)组成的。
(2)长期饮用硬水对人体健康不利,可向水样中加入适量的______ 来鉴别软水和硬水,生活中常用______ 方法降低水的硬度。
(3)机场、车站等公共场所设有许多直饮水机,其处理水的过程如下图所示。
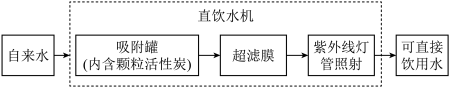
过程中活性炭主要起______ 作用,紫外线灯管照射的作用是______ 。
(4)每一位公民都要爱惜水资源,请你任举一例节约用水的措施______ 。
Ⅱ、水——重要的溶剂
(5)下列家庭常用厨房用品,其中与水混合不能形成溶液的是______。
(6)如图是物质甲和乙的溶解度曲线,请根据图示回答问题

①两种物质中溶解度受温度的影响较大的是______ 。
②图中M点的含义是______ 。
③将乙的不饱和溶液转化为饱和溶液的方法是______ (写一种)。
④t2℃时,将50g甲放入50g水中所得溶液质量为______ g。
⑤t2℃时,等质量的甲、乙饱和溶液,其中所含溶剂质量较多的是______ (填“甲”或“乙”)的饱和溶液。
Ⅰ、水——生命的源泉
(1)电解水的实验说明水是由
(2)长期饮用硬水对人体健康不利,可向水样中加入适量的
(3)机场、车站等公共场所设有许多直饮水机,其处理水的过程如下图所示。

过程中活性炭主要起
(4)每一位公民都要爱惜水资源,请你任举一例节约用水的措施
Ⅱ、水——重要的溶剂
(5)下列家庭常用厨房用品,其中与水混合不能形成溶液的是______。
| A.植物油 | B.食盐 | C.米醋 | D.白砂糖 |
(6)如图是物质甲和乙的溶解度曲线,请根据图示回答问题

①两种物质中溶解度受温度的影响较大的是
②图中M点的含义是
③将乙的不饱和溶液转化为饱和溶液的方法是
④t2℃时,将50g甲放入50g水中所得溶液质量为
⑤t2℃时,等质量的甲、乙饱和溶液,其中所含溶剂质量较多的是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】水是生命的源泉,是人类最宝贵的资源
(1)自来水净化天然水的主要步骤如图所示:试剂X可以用_____ ,净化后的水是_____ (选填“纯净物”或“混合物”)

(2)水是一种最常用的溶剂,将下列生活中的物质分别放入水中,能形成溶液的是_____
A面粉 B冰块 C冰糖 D花生油
(3)某化学兴趣小组的同学利用以下两个实验验证水的组成
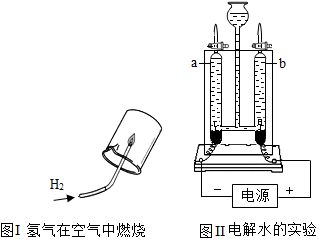
①实验Ⅰ:点燃氢气前,应先_____ ,请你写出氢气在空气中燃烧的化学方程式________
②实验Ⅱ:往水电解器中加入100g溶质质量分数为2%的硫酸钠溶液(碳酸钠不参与反应,仅起增加水的导电性的作用),接通直流电源一段时间后,玻璃管b内产生的气体是_____ ,该试管内产生约10mL气体时,玻璃管a内产生的气体约为_____ mL
(1)自来水净化天然水的主要步骤如图所示:试剂X可以用

(2)水是一种最常用的溶剂,将下列生活中的物质分别放入水中,能形成溶液的是
A面粉 B冰块 C冰糖 D花生油
(3)某化学兴趣小组的同学利用以下两个实验验证水的组成

①实验Ⅰ:点燃氢气前,应先
②实验Ⅱ:往水电解器中加入100g溶质质量分数为2%的硫酸钠溶液(碳酸钠不参与反应,仅起增加水的导电性的作用),接通直流电源一段时间后,玻璃管b内产生的气体是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】水是人类宝贵的自然资源,与人类的生产、生活密切相关。
(1)水是常见的溶剂,将下列生活中的物质分别放入水中,不能形成溶液的是_________ 。
A 蔗糖 B 纯碱 C 食盐 D 花生油
用质量分数为20%的氢氧化钠溶液配制5%的氢氧化钠溶液100g,需要水_________ g。
(2)净化水的常用方法有:①消毒杀菌②过滤③蒸馏④活性炭吸附⑤加明矾吸附沉降。天然水中往往含有许多杂质,要把天然水净化成生活中的自来水,所选用的净化方法按净化过程排序是(填序号)_________ 。
(3)漂白粉可用于水的杀菌消毒,其有效成分是次氯酸钙【化学式为Ca(ClO)2】。次氯酸钙可发生如下反应: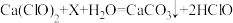 ,则X的化学式为
,则X的化学式为_________ 。
(4)一种新型净水剂高铁酸钾(K2FeO4),具有高效消毒作用,该高铁酸钾中铁元素的化合价为_________ 。
(5)工业上可用海水提取粗盐后的母液来提取金属镁,其流程如下:

该流程中,加溶液A时所发生的反应方程式为_________ ,其中没有发生的基本反应类型为化合反应和_________ 。
(1)水是常见的溶剂,将下列生活中的物质分别放入水中,不能形成溶液的是
A 蔗糖 B 纯碱 C 食盐 D 花生油
用质量分数为20%的氢氧化钠溶液配制5%的氢氧化钠溶液100g,需要水
(2)净化水的常用方法有:①消毒杀菌②过滤③蒸馏④活性炭吸附⑤加明矾吸附沉降。天然水中往往含有许多杂质,要把天然水净化成生活中的自来水,所选用的净化方法按净化过程排序是(填序号)
(3)漂白粉可用于水的杀菌消毒,其有效成分是次氯酸钙【化学式为Ca(ClO)2】。次氯酸钙可发生如下反应:
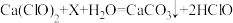 ,则X的化学式为
,则X的化学式为(4)一种新型净水剂高铁酸钾(K2FeO4),具有高效消毒作用,该高铁酸钾中铁元素的化合价为
(5)工业上可用海水提取粗盐后的母液来提取金属镁,其流程如下:

该流程中,加溶液A时所发生的反应方程式为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】正常情况下人的胃液pH为0.8—1.5,相应含氯化氢的质量分数为0.2%—0.4%,胃液中氯化氢过多过少都不利于健康。某人出现反胃、吐酸水的症状,经检查其胃液中氯化氢的质量分数为1.495%(胃液密度约为1g/cm3)。
(1)正常情况下,人的胃液显_________ 性。
(2)若人的胃液总量为100mL,正常胃液中HCl的质量范围为___________________ g。
(3)服用碱性物质可以治疗胃液中HCl含量过多,你认为该患者___________ (填能或不能)服用熟石灰来治疗胃酸过多,理由是 ______________________________________ 。
(4)医生给患者开的药是胃舒平[有效成分是Al(OH)3],每片胃舒平含Al(OH)3 的质量为0.39g。请根据化学方程式计算该患者至少服用________ 片胃舒平,胃液才能恢复正常? (请写出计算过程)
(1)正常情况下,人的胃液显
(2)若人的胃液总量为100mL,正常胃液中HCl的质量范围为
(3)服用碱性物质可以治疗胃液中HCl含量过多,你认为该患者
(4)医生给患者开的药是胃舒平[有效成分是Al(OH)3],每片胃舒平含Al(OH)3 的质量为0.39g。请根据化学方程式计算该患者至少服用
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】氢氧化钠是化学实验室中常用的试剂,也是重要的化工原料。回答下列问题:
(1)氢氧化钠具有强烈的腐蚀性。如果不慎将氢氧化钠沾到皮肤上,应立即用大量的水冲 洗,然后涂上_____ (填“碳酸氢钠”“硫酸”“硼酸”之一)溶液,以防灼伤皮肤。
(2)工业上常以纯碱和石灰石为原料制备氢氧化钠,转化流程示意图如图:

①写出上述转化流程步骤②中所发生反应的化学方程式:______ 。
②步骤③中用熟石灰和水配制石灰水时所需的玻璃仪器有胶头滴管、烧杯、量筒 和_______ 。
(3)实验小组同学要测定某种硫酸铜溶液的溶质质量分数,现取 50g 硫酸铜溶液倒入烧杯 中,慢慢向烧杯中加入溶质质量分数为 10%的氢氧化钠溶液,反应过程中产生沉淀的 质量与所加入氢氧化钠溶液的质量关系如图所示。试回答:

①当加入 NaOH 溶液 40g 时(即图中 B 点),烧杯中 溶液里大量存在的阳离子是______ (填离子符号)。
②当加入 NaOH 溶液 20g 时(即图中 A 点),恰好完全 反应,试通过计算求硫酸铜溶液的溶质质量分数_____ 。(计算结果精确至 1%)
(1)氢氧化钠具有强烈的腐蚀性。如果不慎将氢氧化钠沾到皮肤上,应立即用大量的水冲 洗,然后涂上
(2)工业上常以纯碱和石灰石为原料制备氢氧化钠,转化流程示意图如图:

①写出上述转化流程步骤②中所发生反应的化学方程式:
②步骤③中用熟石灰和水配制石灰水时所需的玻璃仪器有胶头滴管、烧杯、量筒 和
(3)实验小组同学要测定某种硫酸铜溶液的溶质质量分数,现取 50g 硫酸铜溶液倒入烧杯 中,慢慢向烧杯中加入溶质质量分数为 10%的氢氧化钠溶液,反应过程中产生沉淀的 质量与所加入氢氧化钠溶液的质量关系如图所示。试回答:

①当加入 NaOH 溶液 40g 时(即图中 B 点),烧杯中 溶液里大量存在的阳离子是
②当加入 NaOH 溶液 20g 时(即图中 A 点),恰好完全 反应,试通过计算求硫酸铜溶液的溶质质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】中和反应在日常生活、工农业生产和科学实验中有着广泛的应用。
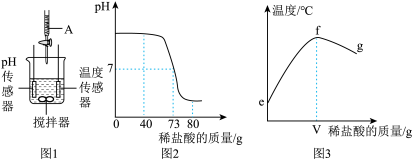
(1)辣椒最适宜在pH为6.2~7.2范围的土壤中种植,若某地区土壤pH=5.2,说明该地区土壤呈______ (填“酸性”、“碱性”或“中性”),想种植辣椒,可以加入适量______ (填物质的俗称)调节土壤pH。
(2)某同学利用图1装置研究中和反应的过程。取50g氢氧化钠溶液,滴加稀盐酸进行实验,并用pH和温度传感器测量反应过程中pH和温度的变化情况,得到图2和图3。已知:所选稀.盐酸的溶质质量分数为10%。
①图3表明,中和反应是______ (填“放热”或“吸热”)反应。
②滴加稀盐酸质量为40g时,溶液中的溶质是______ (写化学式)。
③计算所用氢氧化钠溶液的溶质质量分数_____ 。

(1)辣椒最适宜在pH为6.2~7.2范围的土壤中种植,若某地区土壤pH=5.2,说明该地区土壤呈
(2)某同学利用图1装置研究中和反应的过程。取50g氢氧化钠溶液,滴加稀盐酸进行实验,并用pH和温度传感器测量反应过程中pH和温度的变化情况,得到图2和图3。已知:所选稀.盐酸的溶质质量分数为10%。
①图3表明,中和反应是
②滴加稀盐酸质量为40g时,溶液中的溶质是
③计算所用氢氧化钠溶液的溶质质量分数
您最近一年使用:0次
【推荐1】中华文明源远流长、博大精深,是中华民族独特的精神标识,也是中国文化创新的宝藏——增强历史自觉,坚定文化自信!
【认识海盐】连云港是中国海盐文化重要发源地,历史人文底蕴深厚。
(1) 是由
是由_______ (填粒子符号)构成的。
(2) 是人的正常生理活动所必不可少的,随着社会进步、科技发展,开发了更多的功能性食盐,如可供食用的加碘盐、加锌盐、低钠盐等,这里的“碘”“锌”“钠”指的是
是人的正常生理活动所必不可少的,随着社会进步、科技发展,开发了更多的功能性食盐,如可供食用的加碘盐、加锌盐、低钠盐等,这里的“碘”“锌”“钠”指的是_______ (选填“元素”“原子”)。
【见证历史】“煮海为盐”,造福一方。
明朝宋应星所著《天工开物》记载:“凡煎盐锅古谓之‘牢盆’……以铁打成叶……其下列灶燃……共煎此盘。”“牢盆煎炼海卤”场景如图所示。
(4)“其下列灶燃薪”,灶民将柴草架空燃烧,其原理是_______ 。
(5)展厅陈列的煎盐工具上锈蚀明显,而文物是历史的见证,弥足珍贵。下列措施有利于文物保护的是_______(填字母序号)。
【精制海盐】从海水中获取的粗盐中含有多种杂质,通过进一步处理可得到精盐。兴趣小组同学购买含有泥沙、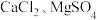 等杂质的海盐,设计如下图所示实验方案,在实验室进行精制提纯。
等杂质的海盐,设计如下图所示实验方案,在实验室进行精制提纯。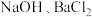 和
和_______ (填化学式)。
(7)溶液B显_______ (选填“酸性”“碱性”)。加入Y后发生的其中一个反应的化学方程式为_______ 。
(8)操作I中玻璃棒的作用是_______ 。
(9)我国食盐产品一般都添加适量碘酸钾,这是因为人体中缺少碘元素,会引起_______ 。
【认识海盐】连云港是中国海盐文化重要发源地,历史人文底蕴深厚。
(1)
 是由
是由(2)
 是人的正常生理活动所必不可少的,随着社会进步、科技发展,开发了更多的功能性食盐,如可供食用的加碘盐、加锌盐、低钠盐等,这里的“碘”“锌”“钠”指的是
是人的正常生理活动所必不可少的,随着社会进步、科技发展,开发了更多的功能性食盐,如可供食用的加碘盐、加锌盐、低钠盐等,这里的“碘”“锌”“钠”指的是【见证历史】“煮海为盐”,造福一方。
明朝宋应星所著《天工开物》记载:“凡煎盐锅古谓之‘牢盆’……以铁打成叶……其下列灶燃……共煎此盘。”“牢盆煎炼海卤”场景如图所示。

| A.导电性 | B.导热性 | C.延展性 |
(4)“其下列灶燃薪”,灶民将柴草架空燃烧,其原理是
(5)展厅陈列的煎盐工具上锈蚀明显,而文物是历史的见证,弥足珍贵。下列措施有利于文物保护的是_______(填字母序号)。
| A.保持文物表面洁净和干燥 |
| B.禁止拍照和触摸 |
C.置文物于密封展柜中以隔绝 等物质 等物质 |
【精制海盐】从海水中获取的粗盐中含有多种杂质,通过进一步处理可得到精盐。兴趣小组同学购买含有泥沙、
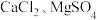 等杂质的海盐,设计如下图所示实验方案,在实验室进行精制提纯。
等杂质的海盐,设计如下图所示实验方案,在实验室进行精制提纯。
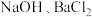 和
和(7)溶液B显
(8)操作I中玻璃棒的作用是
(9)我国食盐产品一般都添加适量碘酸钾,这是因为人体中缺少碘元素,会引起
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】南通有漫长的海岸线,海洋蕴藏着丰富的资源。请按要求填空。
(1)海洋为我们提供了营养丰富的食材。海带富含的______ 元素可以预防甲状腺肿大。
(2)今年5月我国在海域可燃冰开采技术领域取得重大突破。可燃冰主要含有甲烷水合物,还含少量CO2等气体,可燃冰属于______ (选填“纯净物”或“混合物”)。若甲烷大量泄露到大气中,会导致使全球气候变暖。
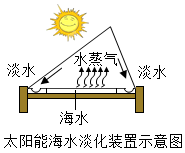
(3)海水淡化可缓解淡水资源匮乏问题。利用如图装置得到淡水的方法与实验室通过______ (填操作名称)净化水的方法原理相同。
(4)海水淡化可缓解淡水资源匮乏问题。水变成水蒸气的过程中,发生变化的是______ 。
A 分子个数B 分子质量C 分子间隔
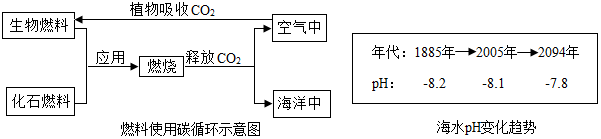
(5)海水碳储存,可以缓解空气中CO2过多的问题,但海水的pH也在逐渐减逐渐软化、变薄、缩小。
①根据海水pH变化趋势判断:2000年时海水呈______ 性。
②“海洋酸化”的原因可用化学方程式表示为______ 。
③软体生物贝壳软化、变薄的原因是______ 。
(1)海洋为我们提供了营养丰富的食材。海带富含的
(2)今年5月我国在海域可燃冰开采技术领域取得重大突破。可燃冰主要含有甲烷水合物,还含少量CO2等气体,可燃冰属于
(3)海水淡化可缓解淡水资源匮乏问题。利用如图装置得到淡水的方法与实验室通过

(4)海水淡化可缓解淡水资源匮乏问题。水变成水蒸气的过程中,发生变化的是
A 分子个数B 分子质量C 分子间隔

(5)海水碳储存,可以缓解空气中CO2过多的问题,但海水的pH也在逐渐减逐渐软化、变薄、缩小。
①根据海水pH变化趋势判断:2000年时海水呈
②“海洋酸化”的原因可用化学方程式表示为
③软体生物贝壳软化、变薄的原因是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】西汉时期的刘安在《淮南万毕术》中写到“曾青得铁则化为铜”,这句话告诉了当时冶炼金属铜的方法属于“湿法炼铜”。为了重现该方法,某同学开展了实验来进行验证。
(1)取一节铁丝时,发现铁丝已生锈。
①铁锈的主要成分是_______ (写化学式)。
②生活中缺铁容易患______ 。
(2)实验操作时,将装有硫酸铜溶液的试剂瓶置于面前,取下试剂瓶瓶塞并倒放,________ ,盖好瓶塞,将试剂瓶放回原位。再将处理好的铁丝缓慢放入试管内的溶液中,一段时间后,可观察到的现象是________ 。
(3)根据化学方程式计算,要得到铜3.2克,理论上需要硫酸铜多少克_______ ?
(1)取一节铁丝时,发现铁丝已生锈。
①铁锈的主要成分是
②生活中缺铁容易患
(2)实验操作时,将装有硫酸铜溶液的试剂瓶置于面前,取下试剂瓶瓶塞并倒放,
(3)根据化学方程式计算,要得到铜3.2克,理论上需要硫酸铜多少克
您最近一年使用:0次



