“侯氏制碱法”是我国著名制碱专家侯德榜做出的杰出贡献,原理可表示为:NH3+NaCl+NaHCO3=NH4Cl+Na2CO3,其最大的优点是降低了成本,提高了NaCl的利用率。
(1)氨气中氮元素的质量分数为______ 。(结果精确至0.1%)
(2)用117 t NaCl(其利用率在96%以上)制碱,至少能生成的Na2CO3质量是多少?(写出计算过程)
(1)氨气中氮元素的质量分数为
(2)用117 t NaCl(其利用率在96%以上)制碱,至少能生成的Na2CO3质量是多少?(写出计算过程)
更新时间:2024-05-26 21:17:43
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】为测定某大理石样品(杂质不溶于水也不参加化学反应)中碳酸钙的含量,取50 g 样品放入烧杯中,再向烧杯中加入适量稀盐酸恰好完全反应,经测定生成二氧化碳的质量为8.8g(产生的气体全部逸出),请计算。
(1)生成氯化钙的质量。
(2)样品中碳酸钙的质量分数。
(1)生成氯化钙的质量。
(2)样品中碳酸钙的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】烧碱有部分变质,测定烧碱的纯度(假设样品中只有氢氧化钠和碳酸钠这两种成分,且碳酸钠是变质产生的),做了如下实验:取烧碱样品20 g,分四次加入36.5 g一定浓度的稀盐酸,数据如表所示:
请根据提供的数据,回答下列问题:
(1)表格数据显示,盐酸在第______ 次反应中耗尽。
(2)表格中m的数值为______ 。
(3)请计算烧碱样品中NaOH的质量分数。
实验次数 | 1 | 2 | 3 | 4 |
每次加入样品的质量/g | 5 | 5 | 5 | 5 |
反应后剩余物质的总质量/g | 40.4 | 44.3 | m | 54.3 |
生成CO2质量/g | 1.1 | 1.1 | 0 | 0 |
(1)表格数据显示,盐酸在第
(2)表格中m的数值为
(3)请计算烧碱样品中NaOH的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】维生素C含片是保健食品,如图是已破损的维生素C片剂的说明书信息。已知维生素C由C、H、O三种元素组成,请回答:

(1)维生素C的化学式______ ;
(2)维生素C在人体内代谢最终产物是CO2和H2O(即维生素C中的碳元素全部转化到最终产物CO2中去了),按成人每日的服用量计算,代谢产物CO2的质量为多少?(写出计算过程)

(1)维生素C的化学式
(2)维生素C在人体内代谢最终产物是CO2和H2O(即维生素C中的碳元素全部转化到最终产物CO2中去了),按成人每日的服用量计算,代谢产物CO2的质量为多少?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】取一定质量的碳和氧气盛于密闭的容器中,高温条件下发生反应,直到恰好完全反应,测得容器中气体的质量为50g,加入足量的澄清石灰水充分反应后,得到白色沉淀50g。
求:
(1)容器中的气体中二氧化碳的质量是______ 克?
(2)容器中的气体中含碳元素的质量是_____ 克?
求:
(1)容器中的气体中二氧化碳的质量是
(2)容器中的气体中含碳元素的质量是
您最近一年使用:0次

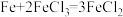 (杂质不参加反应,也不溶于水),当溶液的颜色不再发生变化后,过滤,得到滤液的质量为105.6g。求:
(杂质不参加反应,也不溶于水),当溶液的颜色不再发生变化后,过滤,得到滤液的质量为105.6g。求:

