学习了金属的有关知识后,同学们知道了如何鉴别黄金和黄铜(铜锌合金,俗名“愚人金”),为进一步定量分析黄铜的成分,某同学进行了如下实验:称量黄铜样品20g放入锥形瓶中,向其中不断加入稀硫酸,收集生产的气体与所加稀硫酸的质量关系如图所示。求:
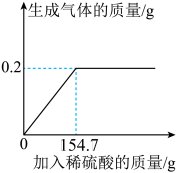
(1)黄铜样品中锌的质量
(2)恰好完全反应时,所得溶液中溶质的质量分数。

(1)黄铜样品中锌的质量
(2)恰好完全反应时,所得溶液中溶质的质量分数。
2015·山东菏泽·中考真题 查看更多[15]
2015年初中毕业升学考试(山东菏泽卷)化学2016届河北省保定市高阳县九年级上学期期末考试化学试卷2017届山东省菏泽市巨野县麒麟镇第一中学九年级3月月考化学试卷鲁教版2018届九年级下册化学同步练习:单元测试(三) 金属山东省平邑县蒙阳新星学校2017届九年级化学专题复习:金属和金属材料人教版2018届九年级下册化学同步课时练习:第九单元 溶液 课题3 溶液的浓度甘肃省武威十七中2019届九年级下学期第一次月考化学试题山东省临沂市蒙阴县第三中学2019届九年级下学期中考二模化学试题鲁教版九年级下册第九单元 核心素养评价卷2019年潍坊市初中化学学业水平考试滚动检测卷(二)2020中考化学章节强化训练——专题二十一:化学方程式2019年5月湖北省宜昌市中考模拟化学试题山东省淄博市周村区第二中学2020-2021学年九年级上学期12月月考化学试题山东省东营市广饶县乐安街道乐安中学等三校2021-2022学年九年级上学期第二次月考化学试题四川省达州市第一中学2022-2023学年九年级下学期第一次月考化学试题
更新时间:2019/01/30 18:14:09
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】为防止金属制品被腐蚀,常在金属表面加上镀层。含铁5%~20%的Zn-Fe合金镀层,具有良好的可焊性、加工性,防护装饰性比镀锌层好,广泛应用于航天航空、船舶、电子电工、机械等领域。
(1)Zn-Fe合金的硬度比纯锌的硬度_______________ 。
(2)含铁20%的Zn-Fe合金中,数目最多的微粒是_______________ 。
(3)自然界中铁元素常以化合物形式存在于矿物中,铁的矿物有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、菱铁矿(FeCO3)等。模拟工业上用赤铁矿炼铁的实验如图所示:
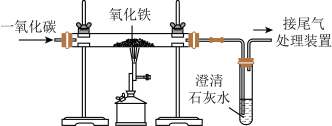
①为确保实验安全,应先_______________ (填“通入CO”或“加热”)。
②硬质玻璃管内发生的主要反应为_______________ (用化学方程式表示)。
③观察到澄清石灰水变浑浊,可推测硬质玻璃管内固体质量的变化是_______________ ,理由是_______________ 。
(4)某机构调研得出,钢铁工业碳排放量能达到全球碳排放量的5%,为减少碳排放,下列炼铁工艺的改进方法,理论上可行的是____ 。
(5)Zn-Fe合金在使用过程中也会被氧化,首先被氧化的是锌。未被完全氧化的Zn-Fe合金可与CuSO4溶液反应制备Cu,可能发生的反应为_______________ (写一个化学方程式即可)。为研究含铁10%的Zn-Fe合金的氧化规律,取28g合金放置一段时间,加入足量的稀盐酸,测得产生0.6g氢气,通过分析,锌未完全氧化,分析思路是_______________ 。
(1)Zn-Fe合金的硬度比纯锌的硬度
(2)含铁20%的Zn-Fe合金中,数目最多的微粒是
(3)自然界中铁元素常以化合物形式存在于矿物中,铁的矿物有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、菱铁矿(FeCO3)等。模拟工业上用赤铁矿炼铁的实验如图所示:

①为确保实验安全,应先
②硬质玻璃管内发生的主要反应为
③观察到澄清石灰水变浑浊,可推测硬质玻璃管内固体质量的变化是
(4)某机构调研得出,钢铁工业碳排放量能达到全球碳排放量的5%,为减少碳排放,下列炼铁工艺的改进方法,理论上可行的是
| A.选择菱铁矿作为炼铁原料 |
| B.用氢气代替焦炭 |
| C.将产生的CO2注入地下进行地质封存 |
| D.将产生的CO2转化为化工产品 |
(5)Zn-Fe合金在使用过程中也会被氧化,首先被氧化的是锌。未被完全氧化的Zn-Fe合金可与CuSO4溶液反应制备Cu,可能发生的反应为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2022年“世界水日”的主题为“珍惜地下水,珍视隐藏的资源”。
(1)自来水厂的净化过程中加入___________ 吸附色素和异味。
(2)生活中,检测生活用水是硬水还是软水可用___________ 。
(3)下列做法能实现爱护水资源的是___________(填序号)。
(4)用如图所示的装置进行电解水实验,下列说法正确的是___________(填序号)。
(5)钠是一种很活泼的金属,既能与酸反应也能与水反应,钠在酸溶液中先与酸反应再与水反应,钠与硫酸、水反应的方程式如下: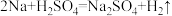 、
、 ,4.6gNa与100g溶质质量分数为4.9%的稀硫酸反应,理论上生成氢气的质量为
,4.6gNa与100g溶质质量分数为4.9%的稀硫酸反应,理论上生成氢气的质量为___________ 。
(1)自来水厂的净化过程中加入
(2)生活中,检测生活用水是硬水还是软水可用
(3)下列做法能实现爱护水资源的是___________(填序号)。
| A.淘米水浇花 | B.禁止使用化肥和农药 |
| C.农业上滴灌改为漫灌 | D.工业废水达标后排放 |
(4)用如图所示的装置进行电解水实验,下列说法正确的是___________(填序号)。
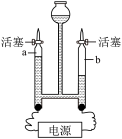
| A.试管a中的气体具有可燃性 |
| B.试管b中的气体是氢气 |
| C.试管a和b中气体的质量比为2:1 |
| D.该实验说明,水不是由一种元素组成的 |
(5)钠是一种很活泼的金属,既能与酸反应也能与水反应,钠在酸溶液中先与酸反应再与水反应,钠与硫酸、水反应的方程式如下:
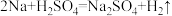 、
、 ,4.6gNa与100g溶质质量分数为4.9%的稀硫酸反应,理论上生成氢气的质量为
,4.6gNa与100g溶质质量分数为4.9%的稀硫酸反应,理论上生成氢气的质量为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】 是一种重要的化工原料。
是一种重要的化工原料。
Ⅰ.粗盐中含可溶性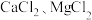 等杂质。学习小组设计了如下方案提纯粗盐:
等杂质。学习小组设计了如下方案提纯粗盐:______ (填化学式)。
(2)“操作X”的名称为_______ 。溶解、过滤、操作X均用到的实验仪器是______ 。
Ⅱ.工业上可通过电解饱和食盐水获得氢氧化钠、 和
和 。
。
(3)写出上述反应的化学方程式:______ 。
(4)上述方法获得的烧碱样品常含有 和
和 等杂质,用“离子交换膜法”生产的碱样品质量主要标准如下表所示:
等杂质,用“离子交换膜法”生产的碱样品质量主要标准如下表所示:
①你认为烧碱样品中含有 的原因是
的原因是_______ (用方程式表示);检验碱样品中是否含有 ,下列试剂中可选择使用的是
,下列试剂中可选择使用的是______ (填序号)。
a.酚酞 b.稀盐酸 c.澄清石灰水
②李老师设计和完成了如下实验来判断碱样品的等级。
称取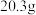 碱样品,加足量水溶解,再加入足量的氯化钡溶液,充分反应后,过滤得到滤渣和滤液;将滤渣洗涤、干燥得到碳酸钡
碱样品,加足量水溶解,再加入足量的氯化钡溶液,充分反应后,过滤得到滤渣和滤液;将滤渣洗涤、干燥得到碳酸钡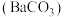 固体
固体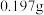 ;向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5%的稀盐酸
;向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5%的稀盐酸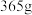 。该碱样品的等级是
。该碱样品的等级是______ 。(不考虑其它杂质参加反应)
 是一种重要的化工原料。
是一种重要的化工原料。Ⅰ.粗盐中含可溶性
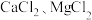 等杂质。学习小组设计了如下方案提纯粗盐:
等杂质。学习小组设计了如下方案提纯粗盐: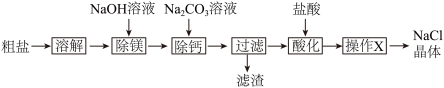
(2)“操作X”的名称为
Ⅱ.工业上可通过电解饱和食盐水获得氢氧化钠、
 和
和 。
。(3)写出上述反应的化学方程式:
(4)上述方法获得的烧碱样品常含有
 和
和 等杂质,用“离子交换膜法”生产的碱样品质量主要标准如下表所示:
等杂质,用“离子交换膜法”生产的碱样品质量主要标准如下表所示:| 等级 | 氢氧化钠含量 | 碳酸钠含量 |
| 优等品 | 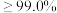 | 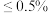 |
| 一等品 |  | 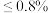 |
| 合格品 | 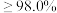 | 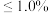 |
 的原因是
的原因是 ,下列试剂中可选择使用的是
,下列试剂中可选择使用的是a.酚酞 b.稀盐酸 c.澄清石灰水
②李老师设计和完成了如下实验来判断碱样品的等级。
称取
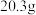 碱样品,加足量水溶解,再加入足量的氯化钡溶液,充分反应后,过滤得到滤渣和滤液;将滤渣洗涤、干燥得到碳酸钡
碱样品,加足量水溶解,再加入足量的氯化钡溶液,充分反应后,过滤得到滤渣和滤液;将滤渣洗涤、干燥得到碳酸钡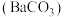 固体
固体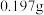 ;向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5%的稀盐酸
;向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5%的稀盐酸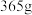 。该碱样品的等级是
。该碱样品的等级是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】木炭还原氧化铜实验后的混合粉末中含有铜、氧化铜、木炭粉,某化学兴趣小组设计回收铜的方案如下:
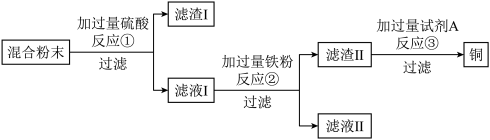
(1)过滤操作中玻璃棒的作用是________ 。
(2)反应①的化学方程式为_________ 。
(3)滤液I中的溶质为_______ (填化学式)。
(4)试剂A可选用下列选项中的________ (选填序号)。
①H2SO4溶液 ②CuSO4溶液 ③MgSO4溶液
(5)为了完善实验方案,可对滤渣I中的_______ 进行回收。

(1)过滤操作中玻璃棒的作用是
(2)反应①的化学方程式为
(3)滤液I中的溶质为
(4)试剂A可选用下列选项中的
①H2SO4溶液 ②CuSO4溶液 ③MgSO4溶液
(5)为了完善实验方案,可对滤渣I中的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
【推荐2】某兴趣小组的同学从实验室收集一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案。结合实验方案回答下列问题:
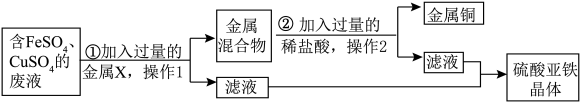
(1)步骤①中加入的金属X是_____ ,写出该反应的化学方程式 ______ ;
(2)操作1和操作2的名称都是_______ ,在该操作中用到的主要玻璃仪器包括玻璃棒、烧杯、 ______ 。
(3)步骤②中,加入过量稀硫酸的目的是______ 。

(1)步骤①中加入的金属X是
(2)操作1和操作2的名称都是
(3)步骤②中,加入过量稀硫酸的目的是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
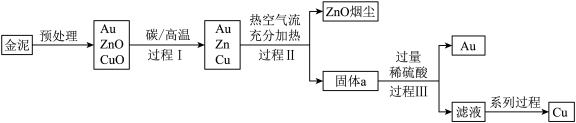
【推荐3】某同学以金泥(含有Au、CuS、ZnS等)为原料制备Au和Cu的流程如图所示。
①预处理的主要目的是将含硫化合物转化为氧化物。
②热空气流充分加热的目的是将Cu、Zn转化为氧化物,并完全分离出ZnO烟尘。
(1)“预处理”中会产生SO2,若SO2直接排放会形成___________ 腐蚀建筑物。
(2)“过程Ⅱ”产生的固体a中,除CuO外一定还有的物质是___________ 。
(3)“过程Ⅲ”分离Au的操作用到了玻璃棒,其主要作用是___________ ,加入过量稀硫酸的目的是___________ 。
(4)“系列进程”中有一步是向滤液中加入过量铁粉,这一步生成气体的化学方程式为___________ ,该反应属于___________ 反应(填基本反应类型)。
(5)ZnO烟尘可用NaOH溶液吸收,反应生成偏锌酸钠(Na2ZnO2)和H2O,该反应的化学方程式为___________ 。
①预处理的主要目的是将含硫化合物转化为氧化物。
②热空气流充分加热的目的是将Cu、Zn转化为氧化物,并完全分离出ZnO烟尘。
(1)“预处理”中会产生SO2,若SO2直接排放会形成
(2)“过程Ⅱ”产生的固体a中,除CuO外一定还有的物质是
(3)“过程Ⅲ”分离Au的操作用到了玻璃棒,其主要作用是
(4)“系列进程”中有一步是向滤液中加入过量铁粉,这一步生成气体的化学方程式为
(5)ZnO烟尘可用NaOH溶液吸收,反应生成偏锌酸钠(Na2ZnO2)和H2O,该反应的化学方程式为
您最近一年使用:0次



