有A、B、C三瓶失去标签的无色溶液,它们分别是盐酸、澄清石灰水和碳酸钠溶液中的一种.为了鉴别它们,各取少量溶液两两混合,实验结果如下表所示.表中“↓”表示有沉淀产生;“↑”表示有气体产生;“﹣”表示观察不到明显的现象变化.
回答下列问题:
(1)A中溶质的化学式是_____________ ,A与C反应的基本类型是_____________ ;
(2)A与B、B与C反应的化学方程式分别是____________ 、_______________ .
| A | B | C | |
| A | ↑ | ﹣ | |
| B | ↑ | ↓ | |
| C | ﹣ | ↓ |
(1)A中溶质的化学式是
(2)A与B、B与C反应的化学方程式分别是
更新时间:2016-11-28 13:39:01
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】已知某混合粉末中含有铜、氧化铜、木炭粉,化学实验小组的同学设计回收铜的方案如下:
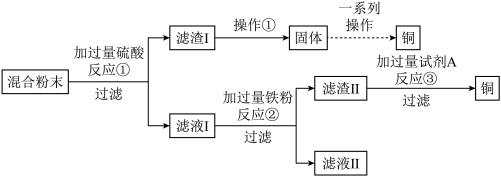
(1)过滤操作中必须用到的玻璃仪器有烧杯、玻璃棒和_______ 。
(2)写出反应②中发生的反应的方程式________ 。
(3)滤液II中的溶质为_______ (填化学式)。
(4)经过一系列的操作后可以将滤渣I中的铜回收起来,其中操作①方法是_______ 。

(1)过滤操作中必须用到的玻璃仪器有烧杯、玻璃棒和
(2)写出反应②中发生的反应的方程式
(3)滤液II中的溶质为
(4)经过一系列的操作后可以将滤渣I中的铜回收起来,其中操作①方法是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】A~G是初中化学常见的物质,已知A、D、F均为单质,其中D是日常生产生活中使用最多的金属,B是一种黑色固体,C是一种常见的酸,E(相对分子质量为160)的水溶液呈蓝色,它们相互转化关系如图所示(部分生成物和反应条件已略去)。试回答下列问题:
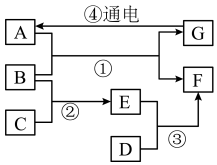
(1)B的化学式:______ 。
(2)F在生产生活中的一种用途______ 。
(3)反应②的化学方程式______ 。
(4)反应③的化学方程式______ 。

(1)B的化学式:
(2)F在生产生活中的一种用途
(3)反应②的化学方程式
(4)反应③的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐1】A~G均为初中常见的物质,其中B是人体胃液中的一种酸,F是改良酸性土壤的碱,它们之间有如下图的相互转化关系(图中部分生成物已略去),请回答下列问题:
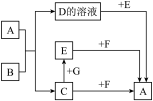
(1)C物质的固体物质在实际生活中的一种用途是:________________ 。
(2)E与F反应的化学方程式是__________________________________ 。
(3)反应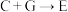 的化学方程式是
的化学方程式是 _____________________________ 。

(1)C物质的固体物质在实际生活中的一种用途是:
(2)E与F反应的化学方程式是
(3)反应
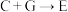 的化学方程式是
的化学方程式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】东晋葛洪《食肉方》(即去除黑痣的药方)记载:“取白炭灰、获灰等分,煎令如膏……可去黑子。此不宜预作,十日则歇”。其意思主要为:取等质量“白炭灰”和“获灰”(即草木灰,含K2CO3),用水煎煮,去渣浓缩,得到的反应产物KOH可去除黑痣。此药不适宜提前制出来,否则放置十多天就会失效。
(1)用水煎煮时,溶液中Ca(OH)2与K2CO3,发生反应,该反应的化学方程式为_______________ ,该反应属于的基本反应类型是____________ 。
(2)上述过程涉及的实验操作除加热外,还有_____ 、____ (写两个)。
(3)KOH与NaOH具有相似的性质,KOH能去除黑痣是因为_________ ;《食肉方》中“不宜预作,十日则歇”的原因可能是________________ 。
(1)用水煎煮时,溶液中Ca(OH)2与K2CO3,发生反应,该反应的化学方程式为
(2)上述过程涉及的实验操作除加热外,还有
(3)KOH与NaOH具有相似的性质,KOH能去除黑痣是因为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】下表是氢氧化钙和氢氧化钠的溶解度数据。请回答下列问题:
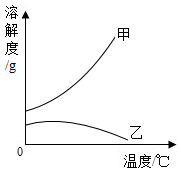
① 氢氧化钠溶解度曲线是____ (选填“甲”或“乙”)
② 把接近饱和的氢氧化钙溶液变成饱和溶液的方法是______ 。
③ 20 ℃时,10 g水中溶解______ 克氢氧化钠恰好饱和。
④ 20 ℃时,分别在100克水中加入m克氢氧化钠和氢氧化钙固体,可得到质量分数相同的两种溶液,则m的取值范围是______ 。
⑤ 60 ℃时,氢氧化钠的饱和溶液中含少量氢氧化钙,把其降温,结晶后过滤,对滤渣、滤液成分分析正确的是______ 。
Ⅰ.滤渣中只有氢氧化钠
Ⅱ.滤渣中一定有氢氧化钠,可能有氢氧化钙
Ⅲ.滤液中一定有氢氧化钙,可能有氢氧化钠
Ⅳ.滤液中一定有氢氧化钠和氢氧化钙
⑥ 氢氧化钙溶液和氢氧化钠溶液都是无色溶液,都能与二氧化碳发生反应。氢氧化钠与二氧化碳反应的方程式为: 2NaOH + CO2 Na2CO3+H2O。氢氧化钙与二氧化碳反应的方程式为
Na2CO3+H2O。氢氧化钙与二氧化碳反应的方程式为______________ 。
根据以上信息,你认为____ (选填“能”或“不能”)用二氧化碳来鉴别这两种溶液。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g/100gH2O) | 氢氧化钙 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| 氢氧化钠 | 31 | 91 | 111 | 129 | 313 | 336 | |

① 氢氧化钠溶解度曲线是
② 把接近饱和的氢氧化钙溶液变成饱和溶液的方法是
③ 20 ℃时,10 g水中溶解
④ 20 ℃时,分别在100克水中加入m克氢氧化钠和氢氧化钙固体,可得到质量分数相同的两种溶液,则m的取值范围是
⑤ 60 ℃时,氢氧化钠的饱和溶液中含少量氢氧化钙,把其降温,结晶后过滤,对滤渣、滤液成分分析正确的是
Ⅰ.滤渣中只有氢氧化钠
Ⅱ.滤渣中一定有氢氧化钠,可能有氢氧化钙
Ⅲ.滤液中一定有氢氧化钙,可能有氢氧化钠
Ⅳ.滤液中一定有氢氧化钠和氢氧化钙
⑥ 氢氧化钙溶液和氢氧化钠溶液都是无色溶液,都能与二氧化碳发生反应。氢氧化钠与二氧化碳反应的方程式为: 2NaOH + CO2
 Na2CO3+H2O。氢氧化钙与二氧化碳反应的方程式为
Na2CO3+H2O。氢氧化钙与二氧化碳反应的方程式为根据以上信息,你认为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】有一包固体,可能合有NaCl、NaOH、Na2CO3、Na2SO4、MgCl2中的一种或几种,为确定其组成,取少量固体加足量水溶解得到无色溶液M,进行如图实验:

(1)写出生成白色沉淀A的化学方程式_____ ;
(2)原固体中一定含有的物质是_____ ;
(3)写出无色滤液2中一定含有的阳离子的符号_____ ;
(4)实验方案不能完全确定混合物的组成,只需改进实验流程中的一处就能达到实验目的,改进的简要方法是_____ 。

(1)写出生成白色沉淀A的化学方程式
(2)原固体中一定含有的物质是
(3)写出无色滤液2中一定含有的阳离子的符号
(4)实验方案不能完全确定混合物的组成,只需改进实验流程中的一处就能达到实验目的,改进的简要方法是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】甲同学设计了以贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱的实验,过程如下。
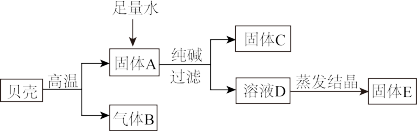
(1)高温煅烧贝壳时发生反应的化学方程式是_______________ 。
(2)固体E的成分存在____________ 种可能。为测定其成分,取少量固体E于试管中,滴加足量稀盐酸,有气泡产生,则固体E的成分是_______________ 。
(3)为得到较纯净的烧碱,乙同学提出了两种方案。
方案一:除去固体E中的杂质:将固体E溶解,加入适量_______ 溶液,过滤,将滤液蒸发结晶。
方案二:重新实验通过称量__________ 的质量,计算加入纯碱的质量。

(1)高温煅烧贝壳时发生反应的化学方程式是
(2)固体E的成分存在
(3)为得到较纯净的烧碱,乙同学提出了两种方案。
方案一:除去固体E中的杂质:将固体E溶解,加入适量
方案二:重新实验通过称量
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组用碳酸钠溶液鉴别稀盐酸、氯化钠溶液和澄清石灰水。进行实验如下表:
写出a试管中发生反应的化学方程式___________ 。把c试管反应后的物质进行过滤,得到滤液。
[提出问题]滤液中溶质的成分是什么?
猜想一: Na2CO3和NaOH; 猜想二: NaOH; 猜想三:NaOH和Ca(OH)2。
[实验过程]为了证明哪种猜想正确,进行了如下实验:
写出上述有白色沉淀生成的化学方程式____________ 。
| 实验步骤 | 实验现象 | 实验结论 |
| 分别用a、b、c三支试管取样,各加入一定量碳酸钠溶液 | a中有气泡产生 | a中物质是稀盐酸 |
| b中无明显现象 | b中物质是氯化钠溶液 | |
| c中 | c中物质是澄清石灰水 |
[提出问题]滤液中溶质的成分是什么?
猜想一: Na2CO3和NaOH; 猜想二: NaOH; 猜想三:NaOH和Ca(OH)2。
[实验过程]为了证明哪种猜想正确,进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取一定量滤液于试管中,加入一种盐溶液(写溶质化学式) | 有白色沉淀 | 猜想一正确 |
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】某敞口放置的氢氧化钠溶液已变质,用化学方程式表示其变质的原因______ 。为证明该瓶氢氧化钠溶液未完全变质,设计了如下实验,请将表格填写完整。
| 实验操作 | 现象 | 结论或化学方程式 |
| 取少量该样品,滴加足量的某溶液,充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为 |
| 在滤液中滴加酚酞溶液 | 样品未完全变质,仍含有氢氧化钠 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】某种矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用它制备氢氧化镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸反应)

请回答下列问题:
(1)写出矿石中的任意一种金属氧化物与稀盐酸反应的化学方程式______ (只写一个)。
(2)在过滤操作中,玻璃棒的作用是______ 。
(3)在溶液A中加入熟石灰调节溶液的pH可以使溶液中的金属阳离子逐步转化为沉淀。在该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,所得溶液B的pH的取值范围为______
(4)写出在溶液B中加入熟石灰发生的化学反应方程式: ______ 。

请回答下列问题:
(1)写出矿石中的任意一种金属氧化物与稀盐酸反应的化学方程式
(2)在过滤操作中,玻璃棒的作用是
(3)在溶液A中加入熟石灰调节溶液的pH可以使溶液中的金属阳离子逐步转化为沉淀。在该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,所得溶液B的pH的取值范围为
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 8.6 |
| 完全沉淀的pH | 3.2 | 6.7 | 11.1 |
您最近一年使用:0次





