氢氧化钠和氢氧化钙是两种常见的碱,小林将两种碱的溶液分别装入试管A、B 中,进行如下实验。

(1)实验l 中,两支试管的溶液都变成_____ 色.
(2)实验2中,若B盛装的是氢氧化钠溶液,发生反应的化学方程式是_____ .
(3)实验3中,小林向两支试管中吹气,A中有白色沉淀生成,发生反应的化学方程式是_____ .B中无现象,为探究吹气后B中溶质的成分,小林进行如下探究:
【提出猜想】猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
【实验和结论】
【反思与评价】老师评价小林得出的结论不正确,是因为_____ 。
如果要验证猜想3成立,你的改进意见是_____ 。

(1)实验l 中,两支试管的溶液都变成
(2)实验2中,若B盛装的是氢氧化钠溶液,发生反应的化学方程式是
(3)实验3中,小林向两支试管中吹气,A中有白色沉淀生成,发生反应的化学方程式是
【提出猜想】猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
【实验和结论】
| 实验 | 实验现象 | 结论 |
| 取B中少量溶液,加入澄清石灰水至不再产生沉淀为止,过滤后取上层清液,向其中加几滴酚酞溶液。 | 产生白色沉淀,溶液呈现红色 | 猜想3成立 |
【反思与评价】老师评价小林得出的结论不正确,是因为
如果要验证猜想3成立,你的改进意见是
更新时间:2016-11-28 14:00:14
|
相似题推荐
科学探究题
|
较难
(0.4)
【推荐1】在溶液中,酸、碱、盐之间发生复分解反应需要一定的条件。小勤对此进行了实验探究:
(1)测试溶液的导电性。
经导电性实验,发现H2SO4、KOH、NaCl、Na2CO3、Ba(NO3)2溶液均能导电,酸、碱、盐在水中均会解离出离子。如NaCl会解离出Na+和____________ 。
(2)判断复分解反应的发生。
将稀硫酸分别加入下表几种溶液中,结合物质溶解性,根据复分解反应的条件,判断反应情况。
表中,判断依据X应为________________________ 。
【查阅资料】:酸、碱、盐溶液中存在溶质离子,发生复分解反应时,某些反应物离子大量减少。如:反应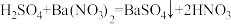 ,反应中SO42-和Ba2+因生成BaSO4沉淀而大量减少,而H+和NO3-仍然在溶液中。
,反应中SO42-和Ba2+因生成BaSO4沉淀而大量减少,而H+和NO3-仍然在溶液中。
稀硫酸与Na2CO3溶液的反应的化学方程式为_____________________________ ,该反应中大量减少的两种离子是____________ 和____________ (填符号)。
(3)实验证明判断。
“依据Y,判断H2SO4不能与NaCI发生复分解反应”,对此,小勤设计了以下实验证明其判断。
①设计思路:
思路甲:混合稀硫酸与NaCl溶液,通过检验H2SO4未被消耗证明二者不反应。
思路乙:混合稀硫酸与NaCI溶液,通过检验未生成HCl证明二者不反应。
②实验证明:根据思路甲,进行下列实验。

根据以上现象分析推理,可判断H2SO4不能与NaCl发生复分解反应。该实验中试剂M可能是____ 。
③方案评价:根据思路乙证明“H2SO4不能与NaCl发生复分解反应”是否可行?对此,请做出判断并说明理由_________ 。
(1)测试溶液的导电性。
经导电性实验,发现H2SO4、KOH、NaCl、Na2CO3、Ba(NO3)2溶液均能导电,酸、碱、盐在水中均会解离出离子。如NaCl会解离出Na+和
(2)判断复分解反应的发生。
将稀硫酸分别加入下表几种溶液中,结合物质溶解性,根据复分解反应的条件,判断反应情况。
| KOH溶液 | NaCl溶液 | Na2CO3溶液 | Ba(NO3)2溶液 | |
| 能否与硫酸反应 | 能 | 不能 | 能 | 能 |
| 判断依据 | X | Y | 有气体生成 | 有沉淀生成 |
【查阅资料】:酸、碱、盐溶液中存在溶质离子,发生复分解反应时,某些反应物离子大量减少。如:反应
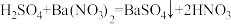 ,反应中SO42-和Ba2+因生成BaSO4沉淀而大量减少,而H+和NO3-仍然在溶液中。
,反应中SO42-和Ba2+因生成BaSO4沉淀而大量减少,而H+和NO3-仍然在溶液中。稀硫酸与Na2CO3溶液的反应的化学方程式为
(3)实验证明判断。
“依据Y,判断H2SO4不能与NaCI发生复分解反应”,对此,小勤设计了以下实验证明其判断。
①设计思路:
思路甲:混合稀硫酸与NaCl溶液,通过检验H2SO4未被消耗证明二者不反应。
思路乙:混合稀硫酸与NaCI溶液,通过检验未生成HCl证明二者不反应。
②实验证明:根据思路甲,进行下列实验。

根据以上现象分析推理,可判断H2SO4不能与NaCl发生复分解反应。该实验中试剂M可能是
③方案评价:根据思路乙证明“H2SO4不能与NaCl发生复分解反应”是否可行?对此,请做出判断并说明理由
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】氮化镁是一种应用范围非常广泛的无机化合物,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物,制备特殊的陶瓷材料等。某兴趣小组用镁与氮气反应制备氮化镁(Mg3N2),并用实验方法测定氮化镁的纯度。
【制备氮化镁】制备氮化镁的装备示意图如下:
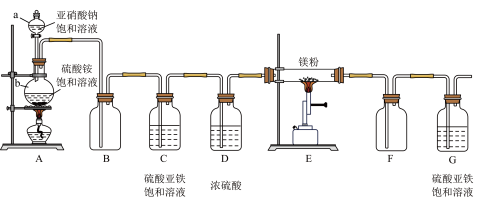
(1)仪器a的名称是_____ ,b的名称是 _____ ;
(2)D装置的作用是_____ ,G装置的作用是 _____ ;能否将C、D装置对调 _____ (填“能”或“否”);
(3)写出E装置中发生反应的化学方程式_____ ;
(4)检查整套装置气密性的方法是_____ ;
(5)进行实验时先进行_____ (选择“A”或“E”)处加热,理由是 _____ ;
(6)A处加热片刻后,应移去酒精灯,理由是_____ 。
【测定氮化镁的含量】
(7)定性测定:
步骤一、取少量氮化镁样品于试管中,加足量蒸馏水,试管底部有沉淀生成,试管口闻到有刺激性气味的气体生成;
步骤二、弃去上层清液,加入稀盐酸,观察到沉淀全溶且冒气泡。
①检验刺激性气味气体的方法是_____ ;
②写步骤二中产生气泡的反应的化学方程式:_____ ;
(8)定量测定:按下图装置进行实验。
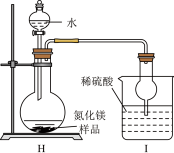
①球形干燥管的作用是_____ ;
②取氮化镁样品16克进行实验,I装置增重3.4克,则该样品中氮化镁的质量分数为_________ ;
③导致该样品中氮化镁含量测定结果偏低的可能原因是_____ 。
| 资料一:氮化镁是浅黄色粉末,极易与水反应生成氢氧化镁沉淀和氨气; 资料二:  ,该反应为放热反应; ,该反应为放热反应;资料三:饱和硫酸亚铁溶液能吸收部分氧气; 资料四:在常温下或温度不高的条件下镁几乎与水不反应。 |

(1)仪器a的名称是
(2)D装置的作用是
(3)写出E装置中发生反应的化学方程式
(4)检查整套装置气密性的方法是
(5)进行实验时先进行
(6)A处加热片刻后,应移去酒精灯,理由是
【测定氮化镁的含量】
(7)定性测定:
步骤一、取少量氮化镁样品于试管中,加足量蒸馏水,试管底部有沉淀生成,试管口闻到有刺激性气味的气体生成;
步骤二、弃去上层清液,加入稀盐酸,观察到沉淀全溶且冒气泡。
①检验刺激性气味气体的方法是
②写步骤二中产生气泡的反应的化学方程式:
(8)定量测定:按下图装置进行实验。

①球形干燥管的作用是
②取氮化镁样品16克进行实验,I装置增重3.4克,则该样品中氮化镁的质量分数为
③导致该样品中氮化镁含量测定结果偏低的可能原因是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】常用的消毒液双氧水。
项目学习小组探究双氧水消毒液储存与使用注意事项时,提出两个任务,并开展实验。
【任务1】探究浓度、温度、酸碱性对双氧水分解的影响
【任务2】探究pH对双氧水消毒液消毒效果的影响
【任务1】
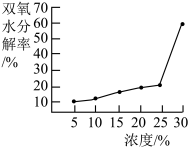
[实验1]60°C时,取6mL30%的双氧水稀释成不同浓度的溶液,控制溶液pH为7.0
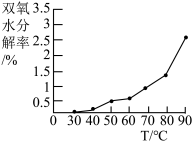
[实验2]取6mL30%的双氧水,控制溶液的pH为7.0,改变体系的温度
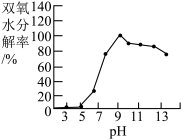
[实验3]60°C时,取6mL30%的双氧水,调节pH从3.1变化到13.2
获得1小时内双氧水的分解率分别见图1、2、3、
【任务2】
20°C时, 取6mL 10%的双氧水溶液, 调节pH从2.0变化到8.0, 在10min、30min、50min 时测定双氧水对枯草杆菌黑色变种芽孢的杀灭作用,结果见下表。
回答下列问题:
(1)写出二氧化锰催化条件下双氧水分解的反应方程式________ 。
(2)用30%的双氧水配制6mL15%的双氧水(密度取1.0g/mL),需要30%的双氧水的质量为_______ g。
(3)据图可知双氧水浓度与分解率的关系是_______ ;温度在90°C内、双氧水分解率受温度的影响情况_______ (填“较大”、“较小”或“无影响”);pH为______ (填数字)时,30%的双氧水分解率最高。
(4)任务2的实验结论:_______ 。
(5)实验反思:除了上述因素会影响双氧水的分解率外,________ (写一种物质)也会影响双氧水的分解率,请写出你的实验方案_______ 。
(6)任务小结:保持在酸性条件下常温储存;使用时避免与_______ 性物质混合使用。
项目学习小组探究双氧水消毒液储存与使用注意事项时,提出两个任务,并开展实验。
【任务1】探究浓度、温度、酸碱性对双氧水分解的影响
【任务2】探究pH对双氧水消毒液消毒效果的影响
【任务1】
[实验1]60°C时,取6mL30%的双氧水稀释成不同浓度的溶液,控制溶液pH为7.0
[实验2]取6mL30%的双氧水,控制溶液的pH为7.0,改变体系的温度
[实验3]60°C时,取6mL30%的双氧水,调节pH从3.1变化到13.2
获得1小时内双氧水的分解率分别见图1、2、3、



【任务2】
20°C时, 取6mL 10%的双氧水溶液, 调节pH从2.0变化到8.0, 在10min、30min、50min 时测定双氧水对枯草杆菌黑色变种芽孢的杀灭作用,结果见下表。
pH | 灭菌率(%) | ||
10min | 30min | 50min | |
2.0 | 76.31 | 99.06 | 99.97 |
6.0 | 49.84 | 96.73 | 99.90 |
8.0 | 34.46 | 91.84 | 94.90 |
(1)写出二氧化锰催化条件下双氧水分解的反应方程式
(2)用30%的双氧水配制6mL15%的双氧水(密度取1.0g/mL),需要30%的双氧水的质量为
(3)据图可知双氧水浓度与分解率的关系是
(4)任务2的实验结论:
(5)实验反思:除了上述因素会影响双氧水的分解率外,
(6)任务小结:保持在酸性条件下常温储存;使用时避免与
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】化学小组为验证某些酸、碱、盐之间能否发生反应,做了如下探究。
【查阅资料】(1)碳酸钠溶液显碱性,硝酸钡、硝酸钠、硫酸钠溶液均呈中性。
(2)碱性溶液中含有大量OH-,且 pH≥8.2的溶液才能使无色酚酞溶液变红色。
(3)碳酸钡、硫酸钡均是不溶于水的白色沉淀,且硫酸钡不溶于酸。
【探究一】如图所示,分别向三支盛有稀硫酸的试管中滴加不同溶液,边滴加边振荡。

【现象与分析】
向试管①中滴入一定量氢氧化钠溶液,没有观察到明显现象。甲同学发现忘记加酚酞试剂了,于是向其中滴入几滴酚酞试剂,观察到溶液变红色。
(1)试管②中的现象是______ 。
(2)试管③中出现白色沉淀,反应的化学方程式为______ 。
【反思交流】
(3)甲同学根据“试管①中溶液呈红色”,认为硫酸与氢氧化钠恰好完全中和。乙同学否认了甲同学的观点,理由是______ 。
【废液处理】实验后,同学们将上述三支试管的“废液”全部倒入一洁净的大烧杯中,充分 混合后静置,发现烧杯底部有白色沉淀,上层清液呈红色。
【讨论交流】
(4)静置后的上层清液中一定大量含有的离子有______ 。(填离子符号)。
【探究二】
(5)丙同学为进一步确定上层清液中可能含有的溶质成分,进行了如下实验:
【得出结论】
(6)综合以上实验及现象,上层清液中所含的溶质(除酚酞外)有______ (填化学式)。
酸、碱、盐之间若发生反应,则有沉淀、气体或水生成。
【查阅资料】(1)碳酸钠溶液显碱性,硝酸钡、硝酸钠、硫酸钠溶液均呈中性。
(2)碱性溶液中含有大量OH-,且 pH≥8.2的溶液才能使无色酚酞溶液变红色。
(3)碳酸钡、硫酸钡均是不溶于水的白色沉淀,且硫酸钡不溶于酸。
【探究一】如图所示,分别向三支盛有稀硫酸的试管中滴加不同溶液,边滴加边振荡。

【现象与分析】
向试管①中滴入一定量氢氧化钠溶液,没有观察到明显现象。甲同学发现忘记加酚酞试剂了,于是向其中滴入几滴酚酞试剂,观察到溶液变红色。
(1)试管②中的现象是
(2)试管③中出现白色沉淀,反应的化学方程式为
【反思交流】
(3)甲同学根据“试管①中溶液呈红色”,认为硫酸与氢氧化钠恰好完全中和。乙同学否认了甲同学的观点,理由是
【废液处理】实验后,同学们将上述三支试管的“废液”全部倒入一洁净的大烧杯中,充分 混合后静置,发现烧杯底部有白色沉淀,上层清液呈红色。
【讨论交流】
(4)静置后的上层清液中一定大量含有的离子有
【探究二】
(5)丙同学为进一步确定上层清液中可能含有的溶质成分,进行了如下实验:
实验操作 | 实验现象 |
取少量上层清液于试管中,加入稍过量 的硝酸钡溶液,振荡。 | 产生白色沉淀,溶液为红色 |
再向试管中加入过量的 | 白色沉淀部分溶解,有气泡产生,溶液为无色 |
【得出结论】
(6)综合以上实验及现象,上层清液中所含的溶质(除酚酞外)有
酸、碱、盐之间若发生反应,则有沉淀、气体或水生成。
您最近一年使用:0次
【推荐2】化学兴趣小组的同学对碱的化学性质的学习展开了一系列的问题探究:

任务一:碱和指示剂的反应(如图 A 所示)
向氢氧化钠溶液中滴入几滴酚酞溶液并振荡,溶液由无色变为______ ;
任务二:碱和非金属氧化物的反应
【实验过程与结论】(如图 B 所示)
【讨论交流与改进】
同学们通过讨论认为实验 2 的结论不正确,改进后的实验方案如下:
【改进与拓展】(如图 C 所示)
任务三:碱和酸的反应
【实验过程与微观分析】(如图 D 所示)
任务四:碱和盐的反应(如图 E 所示)
向氢氧化钠溶液中滴入几滴硫酸铜溶液,现象是______ ,该反应的化学方程式为______ 。

任务一:碱和指示剂的反应(如图 A 所示)
向氢氧化钠溶液中滴入几滴酚酞溶液并振荡,溶液由无色变为
任务二:碱和非金属氧化物的反应
【实验过程与结论】(如图 B 所示)
| 实验操作 | 实验现象 | 实验结论 |
| 实验 1:向澄清的石灰水中通入 CO2 | 澄清石灰水 | 石灰水与 CO2发生反应 |
| 实验 2:向氢氧化钠溶液中通入 CO2 | 无明显现象 | 氢氧化钠溶液与 CO2不发生反应 |
同学们通过讨论认为实验 2 的结论不正确,改进后的实验方案如下:
| 实验操作 | 实验现象 | 实验结论 |
| 向上述实验2中已经通入CO2的氢氧化钠溶液中再滴入几滴稀盐酸 | 溶液中有 | 氢氧化钠溶液与CO2发生反应 |
| 实验操作 | 实验现象 |
| 向装满 CO2的瓶中滴加氢氧化钠溶液 | 气球会 |
【实验过程与微观分析】(如图 D 所示)
| 实验操作 | 实验现象 | 微观分析 |
| 向氢氧化钙溶液中先滴入几滴 | 溶液颜色变化:无色→红色→无色 | 该反应过程中减少的粒子是 |
向氢氧化钠溶液中滴入几滴硫酸铜溶液,现象是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
【推荐3】小军家的下水管道堵了,爸爸买回一种“管道通”,使用后堵塞的管道畅通无阻了。小军对此很好奇,于是想探究“管道通”中的物质成分。
【提出问题】“管道通”中的物质是什么?
【查阅资料】主要内容如下:
(1)下水管道里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西,常用于疏通管道。
(3)铝粉为银灰色固体,铝粉与酸、碱溶液都能反应放出氢气,反应时放出大量热。
①铝与盐酸反应的化学方程式是____
②铝与氢氧化钠溶液反应的化学方程式是:2A1+2NaOH+2H2O=2NaAlO2+3H2↑。
【猜想与验证】小军打开一盒“管道通”,内有袋白色固体颗粒和一袋银灰色粉末。
(1)猜想:白色固体颗粒为氢氧化钠。
结论:白色固体颗粒为氢氧化钠。
(2)猜想:银灰色粉末为铝粉。
【结论】银灰色粉末为铝粉。
【反思】①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似。要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在;
②根据本实验分析,使用“管道通”时,应注意的事项有____ (填一条即可)。
【提出问题】“管道通”中的物质是什么?
【查阅资料】主要内容如下:
(1)下水管道里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西,常用于疏通管道。
(3)铝粉为银灰色固体,铝粉与酸、碱溶液都能反应放出氢气,反应时放出大量热。
①铝与盐酸反应的化学方程式是
②铝与氢氧化钠溶液反应的化学方程式是:2A1+2NaOH+2H2O=2NaAlO2+3H2↑。
【猜想与验证】小军打开一盒“管道通”,内有袋白色固体颗粒和一袋银灰色粉末。
(1)猜想:白色固体颗粒为氢氧化钠。
| 实验操作 | 实验现象 |
| ①将几粒白色固体颗粒放在表面皿上,放置一会儿 | |
| ②将适量白色固体颗粒放入盛有适量水的试管中,并用手触摸试管外壁 | 试管外壁发烫 |
| ③向步骤②得到的溶液中放入一段羊毛线,加热一段时间 | 羊毛线逐渐消失 |
(2)猜想:银灰色粉末为铝粉。
| 实验操作 | 实验现象 |
①按照下图安装两套仪器 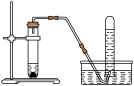 | |
| ②一套仪器中加入银灰色粉末和稀盐酸;另一套仪器中加入银灰色粉末和 | 都产生大量无色气体,试管外壁温度明显升高 |
| ③待导管口有气泡均匀持续冒出时,分别收集1试管气体,验纯 | 用拇指堵住试管口,移近酒精灯火焰,松开拇指, |
| ④在导管口点燃气体 | 火焰颜色为 |
【反思】①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似。要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在;
②根据本实验分析,使用“管道通”时,应注意的事项有
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐1】潜水艇内“氧再生剂”的主要成分是过氧化钠,通过化学反应 ,
, 为潜水员提供氧气。现对“氧气再生剂”进行探究。
为潜水员提供氧气。现对“氧气再生剂”进行探究。
【提出问题一】呼出的气体中有哪些物质与过氧化钠(Na2O2)发生反应,且生成物是什么?
【查阅资料】
①呼出的气体主要含有氮气、二氧化碳、水蒸气和氧气
②过氧化钠与氮气、氧气不反应
③过氧化钠为淡黄色固体粉末
【探究一】H2O 与 Na2O2反应。
【探究二】CO2与Na2O2反应。
【提出问题二】使用后剩余固体成分是什么?
【作出猜想】根据人体呼出的气体中含有较多的 CO2和 H2O。对剩余固体的成分做出如下猜想:
猜想 1:只有氢氧化钠;
猜想 2:______ ;
猜想 3:含有氢氧化钠和碳酸钠。
【探究三】使用“氧气再生剂”呼吸后的产物。
【得出结论】猜想 3 成立。
【交流与讨论】
(1)操作(1)中加入过量的 CaCl2溶液的目的是______ 。
(2)操作(1)中能代替 CaCl2溶液的试剂是______ (写填字母)。
A.NaCl 溶液 B.Ca(NO3)2溶液 C.BaCl2溶液
(3)“氧气再生剂”应______ 保存。
 ,
, 为潜水员提供氧气。现对“氧气再生剂”进行探究。
为潜水员提供氧气。现对“氧气再生剂”进行探究。【提出问题一】呼出的气体中有哪些物质与过氧化钠(Na2O2)发生反应,且生成物是什么?
【查阅资料】
①呼出的气体主要含有氮气、二氧化碳、水蒸气和氧气
②过氧化钠与氮气、氧气不反应
③过氧化钠为淡黄色固体粉末
【探究一】H2O 与 Na2O2反应。
| 步骤一 | 步骤二 | 步骤三 | |
| 实验操作 | 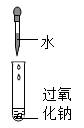 | 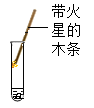 |  |
| 实验现象 | 有气泡产生 | 带火星的木条复燃 | 出现 |
| 实验结论 | H2O能'与Na2O2反应,产生氧气和NaOH | ||
| 步骤一 | 步骤二 | |
| 实验操作 | 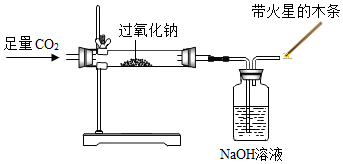 | 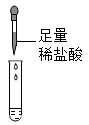 |
| 实验现象 | 淡黄色粉末逐渐变成白色粉末,带火星的木条复燃 | 固体溶解出现 |
| 实验结论 | CO2能与Na2O2反应,产生氧气和Na2CO3 | |
【作出猜想】根据人体呼出的气体中含有较多的 CO2和 H2O。对剩余固体的成分做出如下猜想:
猜想 1:只有氢氧化钠;
猜想 2:
猜想 3:含有氢氧化钠和碳酸钠。
【探究三】使用“氧气再生剂”呼吸后的产物。
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量剩余固体溶于水后,加入过量的 CaCl2溶液 | 含有 Na2CO3 | |
| (2)将上述反应后的混合物过滤,取滤液滴加 | 产生白色沉淀 |
【交流与讨论】
(1)操作(1)中加入过量的 CaCl2溶液的目的是
(2)操作(1)中能代替 CaCl2溶液的试剂是
A.NaCl 溶液 B.Ca(NO3)2溶液 C.BaCl2溶液
(3)“氧气再生剂”应
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐2】足球比赛中让意外昏迷的球员快速恢复意识会用到“嗅盐”。同学们对“嗅盐”产生了好奇,并对其成分进行如下探究。
【查阅资料】①嗅盐是由一种盐类物质和香料(不参与下列探究中的任何反应)组成,能释放出氨味气体,对人体神经会产生强烈的刺激作用,但过量吸入会危害健康。
②氯化钙稀溶液与碳酸氢铵稀溶液不发生反应。
③氨气能与硫酸化合生成硫酸铵。
【提出问题】嗅盐中盐类物质是什么?
【实验探究】填写表中空格。
【质疑】小英认为小军的实验结论不严谨。小英通过补做一个实验(方案见上表),进而确认了小军的结论。小英的实验目的是排除嗅盐中含有___________ 离子的可能性。
【继续探究】同学们利用如图装置进一步测定嗅盐中碳酸铵的质量分数。
反应原理:(NH4)2CO3+2NaOH=X+2NH3↑+2H2O,其中X的化学式为___________ 。

【数据记录】实验称取样品质量为m1,反应前后装有氢氧化钠固体的球形干燥管的总质量分别为m2和m3,反应前后烧杯及烧杯内溶液的总质量分别为m4和m5。(忽略水分的蒸发和空气中水蒸气的干扰)
【数据处理】通过测得数据计算出嗅盐中碳酸铵的质量分数为___________ 。
【反思与评价】关于该实验的说法正确的是___________ 。
A.倒置漏斗可以增大吸收面积同时防止倒吸
B.可以用浓硫酸替代稀硫酸
C.停止加热后要通入一段时间空气,否则测定结果会偏小
【查阅资料】①嗅盐是由一种盐类物质和香料(不参与下列探究中的任何反应)组成,能释放出氨味气体,对人体神经会产生强烈的刺激作用,但过量吸入会危害健康。
②氯化钙稀溶液与碳酸氢铵稀溶液不发生反应。
③氨气能与硫酸化合生成硫酸铵。
【提出问题】嗅盐中盐类物质是什么?
【实验探究】填写表中空格。
| 实验 | 小军的实验 | 小英的实验 | |
实验一: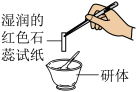 | 实验二: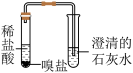 | 实验三: | |
| 现象 | 实验一现象:有刺激性气味产生,湿润的红色石蕊试纸 | 实验二现象: | 溶液变浑浊 |
| 结论 | 嗅盐中含有 | 嗅盐中含 | 确认了小军的实验结论 |
| 证明嗅盐中盐类物质是碳酸铵 | |||
【继续探究】同学们利用如图装置进一步测定嗅盐中碳酸铵的质量分数。
反应原理:(NH4)2CO3+2NaOH=X+2NH3↑+2H2O,其中X的化学式为

【数据记录】实验称取样品质量为m1,反应前后装有氢氧化钠固体的球形干燥管的总质量分别为m2和m3,反应前后烧杯及烧杯内溶液的总质量分别为m4和m5。(忽略水分的蒸发和空气中水蒸气的干扰)
【数据处理】通过测得数据计算出嗅盐中碳酸铵的质量分数为
【反思与评价】关于该实验的说法正确的是
A.倒置漏斗可以增大吸收面积同时防止倒吸
B.可以用浓硫酸替代稀硫酸
C.停止加热后要通入一段时间空气,否则测定结果会偏小
您最近一年使用:0次
科学探究题
|
较难
(0.4)
真题
【推荐3】认真阅读下列材料,回答有关问题
材料一:融雪剂又称“化冰盐”,它以氯化钙和氯化钠为主要原料,并可根据需要调整配比,广泛应用于冬季道路、停车场、广场等场所的融雪和防冻,以保证人们出行安全。
材料二:节日燃放的烟花,是很多金属化合物在灼烧时呈现出的各种艳丽色彩。实验中用铂丝蘸取某些金属化合物灼烧时发现:含钠元素的火焰呈黄色,含钙元素的火焰呈砖红色。
I、研究“融雪剂”成分
结合上述材料,某兴趣小组按下图步骤进行实验,并记录实验现象。
(1)上述实验验证了样品中含有氯化钙,所依据的实验现象是______ 。该反应的化学方程式是______ 。
(2)同学们认为仅通过上述实验,无法确定样品中是否含有氯化钠,理由是______ 。
Ⅱ、拓展探究
(3)【提出问题】反应后上层清液的溶质成分是什么?
【进行猜想】
猜想一:______ ;
猜想二:氯化钠和碳酸钠;
猜想三:氯化钠和氯化钙。
【实验验证】
为进一步确定该上层清液的溶质成分,兴趣小组继续设计实验并请你一起完成下面报告
【交流讨论】以上实验是利用化合物之间发生复分解反应产生明显现象来判断物质的存在,复分解反应发生的条件是有气体或______ 或水生成。
Ⅲ、定量分析
取氯化钠和碳酸钠的固体混合物14.4克于烧杯中,再加入足量的稀盐酸,充分反应,产生气体的质量与稀盐酸的质量关系如图所示。请回答下列问题______ 克。
(5)固体混合物中碳酸钠的质量是多少?(写出具体的解题过程,下同)
(6)A点所示溶液中溶质的质量分数是多少?(计算结果精确到0.1%)
材料一:融雪剂又称“化冰盐”,它以氯化钙和氯化钠为主要原料,并可根据需要调整配比,广泛应用于冬季道路、停车场、广场等场所的融雪和防冻,以保证人们出行安全。
材料二:节日燃放的烟花,是很多金属化合物在灼烧时呈现出的各种艳丽色彩。实验中用铂丝蘸取某些金属化合物灼烧时发现:含钠元素的火焰呈黄色,含钙元素的火焰呈砖红色。
I、研究“融雪剂”成分
结合上述材料,某兴趣小组按下图步骤进行实验,并记录实验现象。
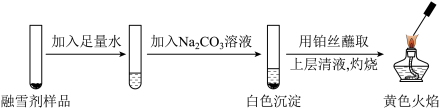
(1)上述实验验证了样品中含有氯化钙,所依据的实验现象是
(2)同学们认为仅通过上述实验,无法确定样品中是否含有氯化钠,理由是
Ⅱ、拓展探究
(3)【提出问题】反应后上层清液的溶质成分是什么?
【进行猜想】
猜想一:
猜想二:氯化钠和碳酸钠;
猜想三:氯化钠和氯化钙。
【实验验证】
为进一步确定该上层清液的溶质成分,兴趣小组继续设计实验并请你一起完成下面报告
| 实验操作 | 实验现象 | 实验结论 |
| 取少量上层清液于试管中,滴加 | 猜想二成立 |
Ⅲ、定量分析
取氯化钠和碳酸钠的固体混合物14.4克于烧杯中,再加入足量的稀盐酸,充分反应,产生气体的质量与稀盐酸的质量关系如图所示。请回答下列问题
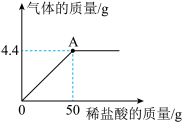
(5)固体混合物中碳酸钠的质量是多少?(写出具体的解题过程,下同)
(6)A点所示溶液中溶质的质量分数是多少?(计算结果精确到0.1%)
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
【推荐1】化学是以实验为基础的科学,实验是科学探究的重要手段。47 中某化学兴趣小组在一次活动中 想选择一种试剂鉴别 “稀盐酸、氯化钠溶液和澄清石灰水”。现将三种无色溶液分别标记为A、B、C。
[实验探究1]:甲同学认为可以选择一种有色溶液鉴别,他选择的试剂为_____ ,乙同学选择用碳酸钠溶液鉴别,实验如图所示:

A试管中发生反应的化学方程式为_____ 。
实验结束后,乙同学先将B试管溶液倒入废液缸,再将A试管溶液倒入废液缸,观察到有气泡冒出,最后将C试管滤液倒入废液缸时,立即产生白色沉淀,则C试管滤液中含有的阳离子为_____ 。
[实验探究2]:对上述反应后的废液进行过滤,同学们对上述滤液中的溶质成分产生了兴趣。
[提出问题]:反应后的溶液中含有哪些溶质呢?
[猜想与假设]:
小峰同学认为溶质是: NaCl、 NaOH 、Na2CO3
小马同学认为溶质是: NaCl、NaOH
小谢同学认为溶质是: NaCl 、Na2CO3、 Ca(OH)2
[交流与评价]:经讨论小谢同学的猜想一定不正确, 理由是_____ 。
[活动与探究]小峰同学想证明自己的猜想正确,于是他取滤液少许,向其中加入足量的稀盐酸,却未观察到气泡,于是他得出结论:自己的猜想错误,小马同学的猜想是正确的。请对小峰同学的结论进行评价_____ 。最后经过同学们合作探究最终证明了溶质的成分。现在小瀛同学带领小组同学一起讨论,此滤液在排放前应如何进行处理,讨论的结果是_____ 。
[总结与提升]通过上述实验,若用一种试剂一次性鉴别多种物质时,要求加入的试剂_____ 。
[实验探究1]:甲同学认为可以选择一种有色溶液鉴别,他选择的试剂为

A试管中发生反应的化学方程式为
实验结束后,乙同学先将B试管溶液倒入废液缸,再将A试管溶液倒入废液缸,观察到有气泡冒出,最后将C试管滤液倒入废液缸时,立即产生白色沉淀,则C试管滤液中含有的阳离子为
[实验探究2]:对上述反应后的废液进行过滤,同学们对上述滤液中的溶质成分产生了兴趣。
[提出问题]:反应后的溶液中含有哪些溶质呢?
[猜想与假设]:
小峰同学认为溶质是: NaCl、 NaOH 、Na2CO3
小马同学认为溶质是: NaCl、NaOH
小谢同学认为溶质是: NaCl 、Na2CO3、 Ca(OH)2
[交流与评价]:经讨论小谢同学的猜想一定不正确, 理由是
[活动与探究]小峰同学想证明自己的猜想正确,于是他取滤液少许,向其中加入足量的稀盐酸,却未观察到气泡,于是他得出结论:自己的猜想错误,小马同学的猜想是正确的。请对小峰同学的结论进行评价
[总结与提升]通过上述实验,若用一种试剂一次性鉴别多种物质时,要求加入的试剂
您最近一年使用:0次
科学探究题
|
较难
(0.4)
真题
解题方法
【推荐2】NaHCO3是初中化学教材中重点介绍的一种盐,俗名____ ,NaHCO3溶液呈碱性。某化学兴趣小组要制取一瓶NaHCO3溶液,他们向NaOH溶液中通入了一定量的CO2,然后对反应后所得到的溶液进行探究。
【提出问题】
反应后溶液中溶质的组成是什么?
【查阅资料】
(1)NaHCO3不仅可以与盐酸反应,也可以与NaOH溶液反应。与NaOH溶液反应的化学方程式为: NaHCO3+NaOH=Na2CO3+H2O。
(2)向NaOH溶液中通入少量CO2,反应的化学方程式为:CO2+2NaOH =Na2CO3+H2O。继续通入过量CO2,反应的化学方程式为:Na2CO3+H2O+CO2=2NaHCO3。
【猜想与假设】
猜想一:含有NaOH、Na2CO3;
猜想二:只含有____ ;
猜想三:含有Na2CO3、NaHCO3;
猜想四:只含有NaHCO3。
【设计实验】
【结论与反思】(1)有同学认为实验①观察到的现象及结论足以证明溶液中有NaOH。你是否同意?请说出理由_____ 。
(2)写出实验③中产生气体的化学方程式____ 。
(3)通过实验①、②、③所观察到的现象及结论,最终得出猜想__ 是正确的。
【拓展与提升】实验室现有一瓶NaOH溶液和足量CO2气体,要制取一瓶溶质只有Na2CO3的溶液,请完善以下实验方案,仪器可以任意选择。
实验方案:先用量筒将NaOH溶液均匀分成两等份,____ 。
【提出问题】
反应后溶液中溶质的组成是什么?
【查阅资料】
(1)NaHCO3不仅可以与盐酸反应,也可以与NaOH溶液反应。与NaOH溶液反应的化学方程式为: NaHCO3+NaOH=Na2CO3+H2O。
(2)向NaOH溶液中通入少量CO2,反应的化学方程式为:CO2+2NaOH =Na2CO3+H2O。继续通入过量CO2,反应的化学方程式为:Na2CO3+H2O+CO2=2NaHCO3。
【猜想与假设】
猜想一:含有NaOH、Na2CO3;
猜想二:只含有
猜想三:含有Na2CO3、NaHCO3;
猜想四:只含有NaHCO3。
【设计实验】
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取少量样品于试管中,滴加几滴无色酚酞试液。 | 溶液呈红色。 | 证明溶液显碱性。 |
| ②另取少量样品于试管中,加入足量的BaCl2溶液,反应完全后,静置过滤。 | 加入BaCl2溶液时观察到的现象 | 证明溶质中有Na2CO3。 |
| ③向实验②所得的滤液中滴加稀盐酸。 | 有无色无味的气体产生,该气体能使澄清石灰水变浑浊。 | 证明实验②所得的滤液中有 |
【结论与反思】(1)有同学认为实验①观察到的现象及结论足以证明溶液中有NaOH。你是否同意?请说出理由
(2)写出实验③中产生气体的化学方程式
(3)通过实验①、②、③所观察到的现象及结论,最终得出猜想
【拓展与提升】实验室现有一瓶NaOH溶液和足量CO2气体,要制取一瓶溶质只有Na2CO3的溶液,请完善以下实验方案,仪器可以任意选择。
实验方案:先用量筒将NaOH溶液均匀分成两等份,
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】小明同学对家中久置的袋装固体食品防腐剂的成分产生了兴趣(品名和成分如图所示),于是和同学一起,设计实验进行探究:

[提出问题]久置固体食品防腐剂的成分是什么?
[查阅资料]铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
[作出猜想]久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3 。
[实验探究]甲同学的探究方案如下表:
[交流与反思]
(1)“504双吸剂”中的铁粉可以吸收空气中的_____ 、_____ 。
(2)实验操作(2)的实验现象里“有大量无色气体产生”,根据甲同学的整体探究方案推测,无色气体的成分应当是_____ 、_____ 。
(3)小明同学认为久置固体食品防腐剂中是否含Fe还可以用_____ 检验。
(4)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是_____ 。
(5)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是_____ 。

[提出问题]久置固体食品防腐剂的成分是什么?
[查阅资料]铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
[作出猜想]久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3 。
[实验探究]甲同学的探究方案如下表:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红。 | 固体中一定含有 |
| (2)另取少量固体放于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 | 固体中一定含有Fe,一定不含 Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 固体中一定含有CaCO3 |
[交流与反思]
(1)“504双吸剂”中的铁粉可以吸收空气中的
(2)实验操作(2)的实验现象里“有大量无色气体产生”,根据甲同学的整体探究方案推测,无色气体的成分应当是
(3)小明同学认为久置固体食品防腐剂中是否含Fe还可以用
(4)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是
(5)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是
您最近一年使用:0次



