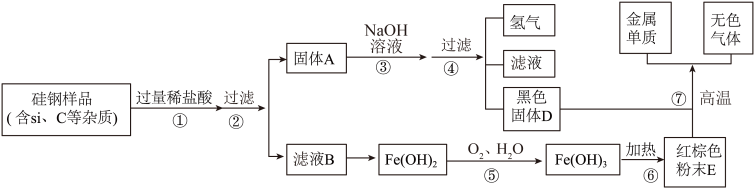
人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如图的实验流程(有些反应的部分反应物和生成物已省略)。
查阅资料发现:
常温下,单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应(Si+2NaOH+H2O=Na2SiO3+2H2↑)。
根据以上信息,回答下列问题:
(1)固体A的成分为______ ,E的化学式为 __________ 。
(2)滤液B中的金属阳离子符号为_______ 。
(3)在过滤操作时,若发现滤液浑浊,应________________ 。
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式_____________________________ 。

查阅资料发现:
常温下,单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应(Si+2NaOH+H2O=Na2SiO3+2H2↑)。
根据以上信息,回答下列问题:
(1)固体A的成分为
(2)滤液B中的金属阳离子符号为
(3)在过滤操作时,若发现滤液浑浊,应
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式
更新时间:2016-11-28 14:01:56
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;铜离子完全沉淀的pH是5左右,铁离子完全沉淀的pH是2左右.以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:
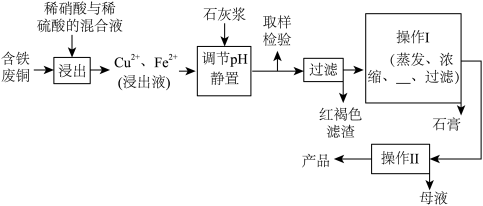
胆矾和石膏在不同温度下的溶解度(g/100g水)如表。
请回答下列问题:
(1)红褐色滤渣的主要成分是____________ ;
(2)石灰浆调pH大约要调节到__________
A. 2 B. 5 C. 7 D.10
(3)含铁的废铜和稀硫酸反应的化学方程式________________________________ ;
(4)操作I最后温度应该控制在___________ ℃左右;
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、__________ 、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是 _________________ 。

胆矾和石膏在不同温度下的溶解度(g/100g水)如表。
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红褐色滤渣的主要成分是
(2)石灰浆调pH大约要调节到
A. 2 B. 5 C. 7 D.10
(3)含铁的废铜和稀硫酸反应的化学方程式
(4)操作I最后温度应该控制在
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】在2.8g铁粉中,先逐滴加入一定量的硝酸铜溶液,充分反应后再逐滴加入硝酸银溶液,剩余固体质量与所加溶液总质量的关系如图所示。

(1)到b点时,生成铜的质量______ m1(填“>”、“=”或“<”);
(2)bc段反应的化学方程式为______ ;
(3)到达e点时,固体除外,溶液中含有的物质有Fe(NO3)2、______ 和______ 等(填化学式);
(4)m3的数值应该为______ 。

(1)到b点时,生成铜的质量
(2)bc段反应的化学方程式为
(3)到达e点时,固体除外,溶液中含有的物质有Fe(NO3)2、
(4)m3的数值应该为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】钨呈银白色,是熔点最高的金属,常用作灯丝。工业上用白钨矿(主要成分是CaWO4、CaO和SiO2)生产钨的流程如图1所示:

【查阅资料】①SiO2不溶于水也不溶于酸。②钨酸(H2WO4)不溶于水。
回答下列问题:
(1)白钨矿反应前要进行粉碎,其目的是_______ 。
(2)操作2所得滤液中一定含有的阳离子是_______ (填离子符号)。
(3)操作3的名称是_______ 。
(4)根据以上信息,推测H2WO4与NaOH溶液反应的方程式为_______ 。
(5)写出流程中WO3生成纯钨的化学反应方程式:_______ 。
(6)要生产184t纯钨,理论上至少需要CaWO4纯度为80%的白钨矿_______ t。
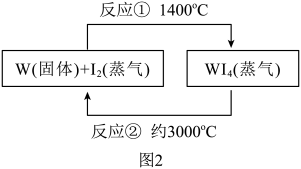
(7)灯丝中的钨在使用过程中缓慢挥发,使灯丝变细,加入I2可以延长灯管的使用寿命,其反应原理表示为图2。下列说法正确的是 (可多选)。

【查阅资料】①SiO2不溶于水也不溶于酸。②钨酸(H2WO4)不溶于水。
回答下列问题:
(1)白钨矿反应前要进行粉碎,其目的是
(2)操作2所得滤液中一定含有的阳离子是
(3)操作3的名称是
(4)根据以上信息,推测H2WO4与NaOH溶液反应的方程式为
(5)写出流程中WO3生成纯钨的化学反应方程式:
(6)要生产184t纯钨,理论上至少需要CaWO4纯度为80%的白钨矿
(7)灯丝中的钨在使用过程中缓慢挥发,使灯丝变细,加入I2可以延长灯管的使用寿命,其反应原理表示为图2。下列说法正确的是 (可多选)。

| A.反应②属于化合反应 |
| B.该灯管内的I2可循环使用 |
| C.WI4在灯丝上分解,使灯管使用寿命延长 |
| D.该灯管中的钨既发生物理变化又发生化学变化 |
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】A~F是初中化学常见的六种物质,其中A是一种理想清洁的高能燃料,B是生活中常用的灭火剂,E是黑色固体,F溶液呈蓝色,它们之间存在如图所示的关系。图中“一”表示相连的物质间能相互反应,“→”表示一种物质能转化成另一种物质(部分反应物、生成物及反应条件已略去)。回答问题:
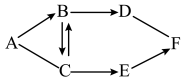
(1)A的化学式____________________ 。
(2)C→E反应的基本类型___________________ 。
(3)写出D与F反应的化学方程式___________________ 。

(1)A的化学式
(2)C→E反应的基本类型
(3)写出D与F反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
【推荐2】根据下列实验图示回答问题
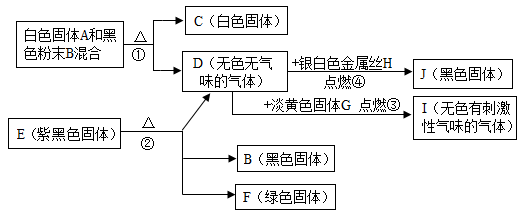
⑴试填写有关物质的化学式:A_____ J_________ ;
⑵写出有关反应的文字或符号表达式 ,并在括号里注明所属反应基本类型
①________________________ ( )
③_________________________ ( )
④__________________________

⑴试填写有关物质的化学式:A
⑵写出有关反应的文字或符号表达式 ,并在括号里注明所属反应基本类型
①
③
④
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
【推荐1】A~J均为初中化学常见的十种化学物质,它们之间存在如下图所示的关系(图中的“—”表示相连两物质之间可以发生反应,图中的“→”表示一种物质可以通过一步转化为另一种物质,反应条件、部分反应物和生成物已略去),其中A和G、B和H、C和D、E和F、I和J分别为相同类别的物质,且A、B、C、E、I类别各不相同。固态B物质常用于人工降雨,J物质是目前世界上年产量最高的金属单质。
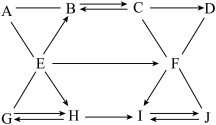
(1)写出B物质的化学式____________ ;
(2)写出E→F的化学方程式_____________ 。

(1)写出B物质的化学式
(2)写出E→F的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】绿矾是含有一定量结晶水的硫酸亚铁,是治疗缺铁性贫血的特效药。化学兴趣小组的同学对绿矾进行探究。
(一)在实验室由铁、铜合金制备绿矾。
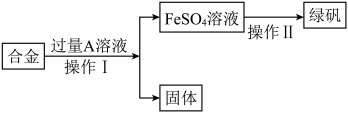
(1)A溶液是_____________ 。
(2)操作II的顺序为蒸发浓缩、冷却结晶、_____________________ 、洗涤、干燥。
(二)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验(B内装固体防止外界空气进入装置A)。

(3)硫酸亚铁容易与氧气反应生成硫酸铁。
将下列实验操作步骤正确排序 d → a →_______ → _____ → ________ →e(填序号);重复上述步骤,直至A恒重,记为m3g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
(4)根据实验记录,计算绿矾中结晶水质量百分含量x=__________________ (列式表示)。若实验时按a、d次序操作,则使x_______________________ (填“偏大”“偏小”或“无影响”)。
(三)硫酸亚铁高温分解的化学方程式2FeSO4 Fe2O3+SO2↑+SO3↑,为验证其气体产物将(3)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末(Fe2O3)。
Fe2O3+SO2↑+SO3↑,为验证其气体产物将(3)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末(Fe2O3)。

查阅资料:
①SO2、SO3和CO2的化学性质相似,都能与碱反应,写出SO3与NaOH反应的化学方程式______ 。
②SO2能使品红溶液褪色,但与BaCl2不反应;SO3与水反应生成H2SO4。
(5)C、D中的溶液依次为___________ 、______________ (填序号)。
a.品红 b.NaOH c.BaCl2 d.浓H2SO4
C、D中有气泡冒出,并可观察到的现象分别为____________ 、_______ 。
(一)在实验室由铁、铜合金制备绿矾。

(1)A溶液是
(2)操作II的顺序为蒸发浓缩、冷却结晶、
(二)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验(B内装固体防止外界空气进入装置A)。

(3)硫酸亚铁容易与氧气反应生成硫酸铁。
将下列实验操作步骤正确排序 d → a →
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
(4)根据实验记录,计算绿矾中结晶水质量百分含量x=
(三)硫酸亚铁高温分解的化学方程式2FeSO4
 Fe2O3+SO2↑+SO3↑,为验证其气体产物将(3)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末(Fe2O3)。
Fe2O3+SO2↑+SO3↑,为验证其气体产物将(3)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末(Fe2O3)。
查阅资料:
①SO2、SO3和CO2的化学性质相似,都能与碱反应,写出SO3与NaOH反应的化学方程式
②SO2能使品红溶液褪色,但与BaCl2不反应;SO3与水反应生成H2SO4。
(5)C、D中的溶液依次为
a.品红 b.NaOH c.BaCl2 d.浓H2SO4
C、D中有气泡冒出,并可观察到的现象分别为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】2020年7月23日,长征五号运载火箭在中国文昌航天发射场点火起飞,成功将天问一号火星探测器送入预定轨道,中国迈出了行星探测的第一步---奔向火星。
(1)长征五号系列火箭采用无毒无污染的液氧、液氢和煤油作为推进剂。航天煤油可由化石燃料中的_______ 分离得到。
(2)“祝融号”上使用了我国自主研发的砷化镓(GaAs)太阳能电池,该电池将______ 转化为电能。(CH3)3Ga和AsH3在700℃的条件下反应,可制得砷化镓并生成一种最简单的有机物,请写出该反应的化学方程式_____ 。
(3)某金属粉末含有Mg、A1、Cu、Ag中的一种或几种,取24g该金属粉末与足量稀盐酸反应产生2g氢气,则该金属粉末的组成有_______ 种情况。
(1)长征五号系列火箭采用无毒无污染的液氧、液氢和煤油作为推进剂。航天煤油可由化石燃料中的
(2)“祝融号”上使用了我国自主研发的砷化镓(GaAs)太阳能电池,该电池将
(3)某金属粉末含有Mg、A1、Cu、Ag中的一种或几种,取24g该金属粉末与足量稀盐酸反应产生2g氢气,则该金属粉末的组成有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】奥运会奖牌制作原料来自电子垃圾中提炼出来的金属。从废线路板中提炼贵重金属和制备硫酸铜晶体的一种工艺流程如图:
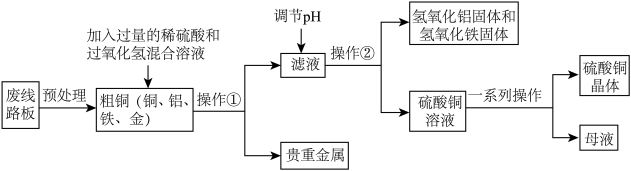
已知:①在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子。
③部分离子沉淀的pH如下表所示。
(1)操作①中玻璃棒的作用是______ 。
(2)提炼出的贵重金属可制作奖牌,其成分是______ 。
(3)调节pH的主要目的是除去滤液中的______ (填金属离子符号),调节pH至______ 以下为最佳。
(4)写出粗铜中最活泼金属发生的一个置换反应的化学方程式:______ 。

已知:①在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子。
③部分离子沉淀的pH如下表所示。
| 对应离子 | Fe3+ | Al3+ | Cu2+ |
| 开始沉淀时的pH | 1.8 | 3.0 | 4.3 |
| 完全沉淀时的pH | 3.0 | 4.2 | 6.7 |
(2)提炼出的贵重金属可制作奖牌,其成分是
(3)调节pH的主要目的是除去滤液中的
(4)写出粗铜中最活泼金属发生的一个置换反应的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】氯化钡是一种可溶性重金属盐,广泛应用于化工领域。用毒重石(主要成分为BaCO3)制备氯化钡晶体工艺流程如下:
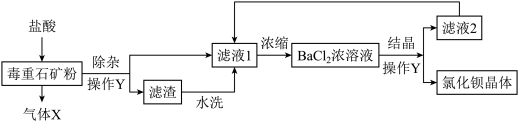
(1)毒重石要进行粉碎的目的是____ 。气体X的化学式为____ 。
(2)操作Y的名称是____ 。该操作中用到的玻璃仪器有烧杯,玻璃棒和____ ,其中玻璃棒作用____ 。滤液2中可循环利用的物质除水外还有____ 。洗涤氯化钡晶体最适宜的洗涤剂是____ (填字母)。
A.30℃水 B.30℃饱和氯化钠溶液 C.30℃饱和氯化钡溶液
(3)滤渣水洗的目的是_____________ 和 ______________ 。
(4)取一定量的产物配成100 g 质量分数为5.2%的溶液,需要溶质的质量为________ g,若量取水时俯视读数,则溶质质量分数将________ (填“偏大”、“偏小”“不变”)。

(1)毒重石要进行粉碎的目的是
(2)操作Y的名称是
A.30℃水 B.30℃饱和氯化钠溶液 C.30℃饱和氯化钡溶液
(3)滤渣水洗的目的是
(4)取一定量的产物配成100 g 质量分数为5.2%的溶液,需要溶质的质量为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
【推荐3】铜和铁是生活、生产中广泛使用的金属.
(1)工业上常用赤铁矿(主要成分为氧化铁)炼铁,反应的化学方程式为__ .
(2)铜也像铁一样表面易生锈,生成的铜绿其主要成分是碱式碳酸铜〔Cu2(OH)2CO3〕,它由__ 种元素组成,从组成上看,铜生锈除了跟空气中的氧气、水有关外,还可能跟空气中的 __ 有关.
铜绿受热后会变成黑色粉末,从黑色粉末中回收铜可通过下列途径实现:

①操作a的名称是_____________ ;
铜绿受热变成黑色粉末的反应,属于基本反应类型中的_____________ ;
③蓝色溶液中加入过量铁粉所发生反应的化学方程式为____________ ;
④证明B过量的方法是_____________ .
(1)工业上常用赤铁矿(主要成分为氧化铁)炼铁,反应的化学方程式为
(2)铜也像铁一样表面易生锈,生成的铜绿其主要成分是碱式碳酸铜〔Cu2(OH)2CO3〕,它由
铜绿受热后会变成黑色粉末,从黑色粉末中回收铜可通过下列途径实现:

①操作a的名称是
铜绿受热变成黑色粉末的反应,属于基本反应类型中的
③蓝色溶液中加入过量铁粉所发生反应的化学方程式为
④证明B过量的方法是
您最近一年使用:0次




