某化学兴趣小组对胃药“碳酸氢钠片”进行了探究,具体做法如下:
Ⅰ.取1片胃药研碎,加水完全溶解得到100g溶液;
Ⅱ.配制100g 0.365%的稀盐酸作为模拟胃酸;
Ⅲ.取上述一种溶液20g于锥形瓶中,再将另一种溶液逐滴加入锥形瓶内,反应后溶液的pH变化情况如图所示.
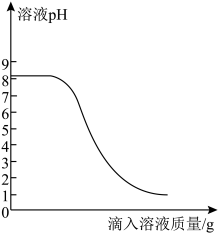
请回答下列问题:
(1)碳酸氢钠属于______(填“酸”“碱”或“盐”);
(2)步骤Ⅲ中,当滴入另一种溶液的质量为10g时,锥形瓶内物质恰好完全反应(胃药中其它成分不参加反应),请根据实验数据计算每片胃药中碳酸氢钠的质量,写出必要的计算过程__________________。
Ⅰ.取1片胃药研碎,加水完全溶解得到100g溶液;
Ⅱ.配制100g 0.365%的稀盐酸作为模拟胃酸;
Ⅲ.取上述一种溶液20g于锥形瓶中,再将另一种溶液逐滴加入锥形瓶内,反应后溶液的pH变化情况如图所示.

请回答下列问题:
(1)碳酸氢钠属于______(填“酸”“碱”或“盐”);
(2)步骤Ⅲ中,当滴入另一种溶液的质量为10g时,锥形瓶内物质恰好完全反应(胃药中其它成分不参加反应),请根据实验数据计算每片胃药中碳酸氢钠的质量,写出必要的计算过程__________________。
2016·湖北武汉·中考真题 查看更多[3]
更新时间:2016-11-28 14:09:38
|
相似题推荐
计算题
|
较难
(0.4)
真题
【推荐1】我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某班同学实验后收集到含有碳酸钠和氢氧化钠的混合废液5.11kg,一个兴趣小组用废弃的溶质质量分数为19.6%的硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求:
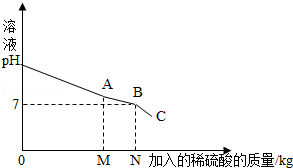
(1)通过如图可知,当反应进行至图中 点时(填“A”、“B”或“C”),废液恰好处理完(即碳酸钠和氢氧化钠混合废液刚好完全转化成硫酸钠溶液).
(2)当向混合液中加入稀硫酸至N点时,加入的稀硫酸质量为5kg,此时溶液总质量为10kg.求此时所得溶液中溶质的质量分数(写出计算过程,溶于水的气体忽略不计).

(1)通过如图可知,当反应进行至图中 点时(填“A”、“B”或“C”),废液恰好处理完(即碳酸钠和氢氧化钠混合废液刚好完全转化成硫酸钠溶液).
(2)当向混合液中加入稀硫酸至N点时,加入的稀硫酸质量为5kg,此时溶液总质量为10kg.求此时所得溶液中溶质的质量分数(写出计算过程,溶于水的气体忽略不计).
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保小组的同学进行了以下实验。取废水500g,向其中加入溶质质量分数为20%的氢氧化钠溶液。测得沉淀质量与所加入的氢氧化钠溶液的质量关系如图。根据图中所得数据计算:

(1)反应生成的Cu(OH)2的质量为________ g;
(2)该废水中硫酸的溶质质量分数是___________ ;(请写出计算过程)
(3)废水中所含硫酸的质量为________ g;当加入120g氢氧化钠溶液恰好完全反应后,所得溶液中溶质的质量分数是________ 。(结果精确到0.1%)

(1)反应生成的Cu(OH)2的质量为
(2)该废水中硫酸的溶质质量分数是
(3)废水中所含硫酸的质量为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】下图烧杯中装有100g硫酸和硫酸镁的混合溶液,向该溶液中加入10%的氢氧化钠溶液至恰好反应完全时,生成沉淀5. 8g。请回答:
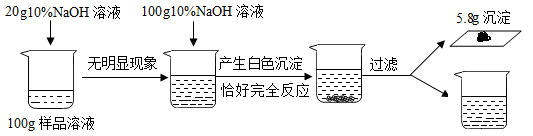
(1)若配制实验所用的氢氧化钠溶液,则需要24%的氢氧化钠溶液的质量为_____。
(2)写出第一次实验时反应的化学方程式_____。
(3)列出求解原混合溶液中含有硫酸镁质量(x)的比例式_____。
(4)第一次加完NaOH溶液后,溶液中溶质的成分为:_____。
(5)向过滤后所得溶液中蒸发72. 2g水后,所得溶液中溶质的质量分数为_____。

(1)若配制实验所用的氢氧化钠溶液,则需要24%的氢氧化钠溶液的质量为_____。
(2)写出第一次实验时反应的化学方程式_____。
(3)列出求解原混合溶液中含有硫酸镁质量(x)的比例式_____。
(4)第一次加完NaOH溶液后,溶液中溶质的成分为:_____。
(5)向过滤后所得溶液中蒸发72. 2g水后,所得溶液中溶质的质量分数为_____。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】小艾同学用纯碱样品(含少量氯化钠),进行如图所示的实验。请计算:
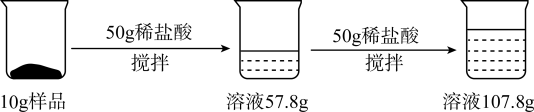
(1)产生二氧化碳气体的总质量为 。
(2)计算所加稀盐酸的溶质质量分数。(计算结果精确到0.1%)(反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑)

(1)产生二氧化碳气体的总质量为 。
(2)计算所加稀盐酸的溶质质量分数。(计算结果精确到0.1%)(反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑)
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐3】某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图
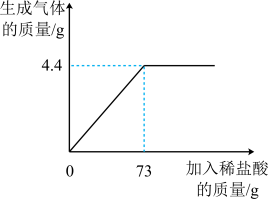
(1)纯碱恰好完全反应时,生成CO2的质量为___g
(2)计算该样品中含杂质的质量分数是多少?(计算结果保留一位小数,下同)____________
(3)计算当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数是多少?____________

(1)纯碱恰好完全反应时,生成CO2的质量为___g
(2)计算该样品中含杂质的质量分数是多少?(计算结果保留一位小数,下同)____________
(3)计算当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数是多少?____________
您最近一年使用:0次





