曾经有一段时期,个别餐饮店和学校食堂发生的食物中毒事件,经卫生部门检验鉴定,是就餐者食用了含“毒鼠强”的食品所致。已知“毒鼠强”的化学式为C4H8N4S2O4。
(1)“毒鼠强”的相对分子质量为_____ 。
(2)“毒鼠强”中碳与氢原子的个数比为_____ 。
(3)“毒鼠强”中碳元素与氮元素的质量比为_____ 。
(4)“毒鼠强”中氧元素的质量分数为_____ 。
(5)1000克“毒鼠强”中含氧多少克_______ g?
(1)“毒鼠强”的相对分子质量为
(2)“毒鼠强”中碳与氢原子的个数比为
(3)“毒鼠强”中碳元素与氮元素的质量比为
(4)“毒鼠强”中氧元素的质量分数为
(5)1000克“毒鼠强”中含氧多少克
更新时间:2016-11-28 14:11:22
|
相似题推荐
【推荐1】感悟化学应用之广
(1)“加铁酱油”可预防贫血,其中的“铁”是指______ (填“元素”或“原子”)。
(2)冰箱中放活性炭除去异味,这是利用了活性炭的______ 性。
(3)我国率先用CO2人工合成淀粉,淀粉分解产物为葡萄糖(化学式C6H12O6)。葡萄糖由______ 种元素组成,其中碳、氢元素质量比为______ ,质量分数最高的元素是______ ,90g葡萄糖中约含氧原子______ 个(用科学记数法表示)。
(1)“加铁酱油”可预防贫血,其中的“铁”是指
(2)冰箱中放活性炭除去异味,这是利用了活性炭的
(3)我国率先用CO2人工合成淀粉,淀粉分解产物为葡萄糖(化学式C6H12O6)。葡萄糖由
您最近一年使用:0次
【推荐2】多角度认识二氧化碳。
(1)认识二氧化碳的组成和构成
①从宏观上看,二氧化碳由_______ (填“元素”、“原子”或“分子”,下同)组成。
②从微观上看,二氧化碳由_______ 构成。
(2)认识二氧化碳的性质
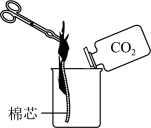
将蘸有酒精的棉芯点燃后放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到烧杯中的棉芯自下而上熄灭(如图)。说明二氧化碳具有的性质有_______ ,由此可推知的灭火原理是_______ 。若使棉芯下半段恢复燃烧,操作方法是_______ 。
(3)辩证地认识二氧化碳
①量变引起质变。例如:碳在充足氧气中燃烧生成二氧化碳,在不充足的氧气中燃烧生成_______ (写化学式)。
②功过相对论。从“二氧化碳导致温室效应”的事实分析,“过”:使全球气候变暖导致海平面上升等;“功”:_______ (举一例)。
(1)认识二氧化碳的组成和构成
①从宏观上看,二氧化碳由
②从微观上看,二氧化碳由
(2)认识二氧化碳的性质
将蘸有酒精的棉芯点燃后放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到烧杯中的棉芯自下而上熄灭(如图)。说明二氧化碳具有的性质有

(3)辩证地认识二氧化碳
①量变引起质变。例如:碳在充足氧气中燃烧生成二氧化碳,在不充足的氧气中燃烧生成
②功过相对论。从“二氧化碳导致温室效应”的事实分析,“过”:使全球气候变暖导致海平面上升等;“功”:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图为某分子的结构模型,请回答下列问题:

(1)该物质是食醋的主要成分,相对分子质量为__________ 。
(2)该物质的碳、氢、氧元素质量比为__________ 。
(3)计算该物质中碳元素的质量分数__________ 。

(1)该物质是食醋的主要成分,相对分子质量为
(2)该物质的碳、氢、氧元素质量比为
(3)计算该物质中碳元素的质量分数
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】氨气(NH3)是一种无色、有刺激性气味的气体,极易溶于水,它的水溶液称为氨水,显碱性。氨气在化学工业中用途很广泛,例如制化肥、制纯碱等;近年来,氨气还用于环境治理。
(1)在400℃左右,有催化剂存在的条件下,用氨气可将有毒气体NO还原为N2和H2O。试写出该反应的化学方程式_____________________ 。
(2)“侯氏制碱法”关键一步的反应原理可表示为:NaCl+H2O+NH3+CO2=NaHCO3+NH4Cl,其生成物NH4Cl的相对分子质量为_________ ,NH4Cl中氮元素的质量分数为_________ (精确到0.1%)。若上述NH4Cl中氮元素的质量为2.8t,则NH4Cl的质量为__________ t。(精确到0.1)
(3)在细菌作用下,用氨气处理含甲醇的工业废水,使其变为无毒的N2和CO2,从而清除对环境的污染,有关的反应为:6NH3+5CH3OH+12X 3N2+5CO2+19H2O,上述反应的X处应填入的化学式为
3N2+5CO2+19H2O,上述反应的X处应填入的化学式为_______ 。
(1)在400℃左右,有催化剂存在的条件下,用氨气可将有毒气体NO还原为N2和H2O。试写出该反应的化学方程式
(2)“侯氏制碱法”关键一步的反应原理可表示为:NaCl+H2O+NH3+CO2=NaHCO3+NH4Cl,其生成物NH4Cl的相对分子质量为
(3)在细菌作用下,用氨气处理含甲醇的工业废水,使其变为无毒的N2和CO2,从而清除对环境的污染,有关的反应为:6NH3+5CH3OH+12X
 3N2+5CO2+19H2O,上述反应的X处应填入的化学式为
3N2+5CO2+19H2O,上述反应的X处应填入的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列有关问题:
(1)氧化铁中铁元素和氧元素的质量比为______________ 。
(2)160克氧化铁中含铁元素质量为________________ 克。
(3)铁元素质量相等的氧化铁(Fe2O3)、氧化亚铁(FeO)、四氧化三铁(Fe3O4)中氧元素的质量比为_____ 。
(1)氧化铁中铁元素和氧元素的质量比为
(2)160克氧化铁中含铁元素质量为
(3)铁元素质量相等的氧化铁(Fe2O3)、氧化亚铁(FeO)、四氧化三铁(Fe3O4)中氧元素的质量比为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】中国茶,世界香。从古代丝绸之路、茶马古道,到今天丝绸之路经济带,茶穿越历史,跨越国界,深受世界各国人民喜爱。
I.了解茶叶
(1)茶叶中富含的茶多酚具有强血管、降血脂的作用。某种茶多酚的化学式为C17H19N3O,其氢、氮元素的质量比为___________ 。
(2))茶叶含氟较高,对预防龋齿有一定效果。这里的“氟”指的是___________ (填“元素”或“单质”)。
Ⅱ.种植茶树
(3)茶树适宜在pH为5~6的土壤中生长,该土壤浸出液能使紫色石蕊试液___________ 。
(4)茶树是叶用植物,需氮元素比一般植物多,大量施用氮肥加速了土壤的酸化,可施加___________ (填物质俗名)改良酸性土壤。
Ⅲ.冲泡茶汤
(5)水的矿化度(钙、镁离子含量)越低,茶汤的品质越高。生活中降低水的矿化度的方法为__ 。
(6)泡茶时可用茶漏将茶汤和茶渣分离,茶渣可通过脱水、炭化、活化形成活性炭。活性炭在净水过程中的主要作用是________ 。
IV.清洁茶具
(7)除垢原理
长期使用的茶具中易出现茶垢(主要成分碳酸钙),需定期处理。柠檬酸除茶垢:柠檬酸溶液能除茶垢的原理是___________ 。茶垢清洁剂除茶垢:清洁剂中的过碳酸钠遇热水产生大量氧气,分解茶垢。
(8)自制除垢剂
①将50g质量分数为30%的柠檬酸溶液稀释为除垢所需质量分数为10%的柠檬酸溶液,需加水___________ g。
②向饱和碳酸钠溶液中加入过氧化氢溶液的过程中,过碳酸钠的产率与反应温度的关系如下表:
分析数据,制备过碳酸钠的最佳温度范围是___________ ℃。温度过高,产率反而降低,从制备过碳酸钠原料的性质分析产率降低的原因是___________ 。
I.了解茶叶
(1)茶叶中富含的茶多酚具有强血管、降血脂的作用。某种茶多酚的化学式为C17H19N3O,其氢、氮元素的质量比为
(2))茶叶含氟较高,对预防龋齿有一定效果。这里的“氟”指的是
Ⅱ.种植茶树
(3)茶树适宜在pH为5~6的土壤中生长,该土壤浸出液能使紫色石蕊试液
(4)茶树是叶用植物,需氮元素比一般植物多,大量施用氮肥加速了土壤的酸化,可施加
Ⅲ.冲泡茶汤
(5)水的矿化度(钙、镁离子含量)越低,茶汤的品质越高。生活中降低水的矿化度的方法为
(6)泡茶时可用茶漏将茶汤和茶渣分离,茶渣可通过脱水、炭化、活化形成活性炭。活性炭在净水过程中的主要作用是
IV.清洁茶具
(7)除垢原理
长期使用的茶具中易出现茶垢(主要成分碳酸钙),需定期处理。柠檬酸除茶垢:柠檬酸溶液能除茶垢的原理是
(8)自制除垢剂
①将50g质量分数为30%的柠檬酸溶液稀释为除垢所需质量分数为10%的柠檬酸溶液,需加水
②向饱和碳酸钠溶液中加入过氧化氢溶液的过程中,过碳酸钠的产率与反应温度的关系如下表:
| 温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
| 过碳酸钠的产率/% | 84.49 | 85.78 | 88.38 | 83.01 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】目前,流感高发,磷酸奥司他韦能有效治疗甲型、乙型流感。磷酸奥司他韦的化学式为(C16H28N2O4H3PO4)。请计算:

(1)磷酸奥司他韦的相对分子质量是_____ ,分子中各原子个数比为C:H:O:N:P=_____ (填最简整数比)。
(2)列式计算磷酸奥司他韦中氮元素的质量分数是多少?(结果保留至0.01%)。

(1)磷酸奥司他韦的相对分子质量是
(2)列式计算磷酸奥司他韦中氮元素的质量分数是多少?(结果保留至0.01%)。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】2000年10月1日食用盐新标准将加碘浓度由40毫克/千克食盐调整为35毫克/千克食盐。
(1)加碘食盐中的碘是指______
(2)已知加碘食盐中的碘多以碘酸钾的形式存在,碘酸钾的化学符号和氯酸钾类似,请写出碘酸钾的化学式_________ ,其中碘的化合价为_______ 。
(3)某厂生产的食盐每袋(500g)含碘酸钾21.4mg,其中含碘____ mg,该食盐_____ (填合格或不合格)。
(1)加碘食盐中的碘是指
| A.碘单质 | B.碘原子 | C.碘分子 | D.碘元素 |
(3)某厂生产的食盐每袋(500g)含碘酸钾21.4mg,其中含碘
您最近一年使用:0次




