在现代生活中,人们越来越注重微量元素的摄取。碘元素对人体有着至关重要的作用。如图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答下列问题:

(1)碘酸钾(KIO3)中碘元素的化合价为_____;
(2)碘酸钾(KIO3)中钾元素、碘元素、氧元素的质量比是_____;
(3)碘酸钾(KIO3)中,碘元素的质量分数是_____;(计算结果精确到0.1%)
(4)若成人每天摄入5g这样的“碘盐”,至少补充碘元素_____mg?(简要写出求解过程)

(1)碘酸钾(KIO3)中碘元素的化合价为_____;
(2)碘酸钾(KIO3)中钾元素、碘元素、氧元素的质量比是_____;
(3)碘酸钾(KIO3)中,碘元素的质量分数是_____;(计算结果精确到0.1%)
(4)若成人每天摄入5g这样的“碘盐”,至少补充碘元素_____mg?(简要写出求解过程)
16-17九年级上·安徽阜阳·期中 查看更多[5]
2017届安徽省阜阳九中九年级上学期期中化学试卷(已下线)专题16 综合计算(预测题)-决胜2018中考化学压轴题全揭秘精品【县级联考】广东省揭阳市惠来县2019届九年级上学期期中考试化学试题山东省菏泽市郓城县2020-2021学年九年级上学期期中化学试题天津市第二中学2020-2021学年九年级上学期期中化学试题
更新时间:2016-12-13 02:50:40
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】小强同学在公共场所围墙上看到一则化肥广告(如图)。

(1)硝酸铵(NH4NO3)中氮、氢、氧三种元素的原子个数比为______ 。
(2)硝酸铵(NH4NO3)中氮、氢、氧三种元素的质量比为______ 。
(3)通过计算判断该广告属于虚假广告还是真实广告?(写出计算过程)
(4)小强认为此广告欺骗了农民,向有关部门反映,技术监督局对该产品取样分析,发现氮元素质量分数仅为 28%,则 100 吨这样的化肥与多少 CO(NH2)2(尿素)含氮量相同?

(1)硝酸铵(NH4NO3)中氮、氢、氧三种元素的原子个数比为
(2)硝酸铵(NH4NO3)中氮、氢、氧三种元素的质量比为
(3)通过计算判断该广告属于虚假广告还是真实广告?(写出计算过程)
(4)小强认为此广告欺骗了农民,向有关部门反映,技术监督局对该产品取样分析,发现氮元素质量分数仅为 28%,则 100 吨这样的化肥与多少 CO(NH2)2(尿素)含氮量相同?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】新型冠状肺炎在我国发生后,我省推出防治新冠肺炎的中医药“湖北方剂”成效明显。传统中药“金银花”的有效成分“绿原酸”具有抗菌杀毒的作用,其化学式为C16H18O9。请你计算:
(1)绿原酸的相对分子质量=________________ 。
(2)绿原酸中碳元素和氧元素的质量比为________________ 。
(3)100g绿原酸中含碳元素的质量是多少?(写出计算过程,结果精确到0.1g)。
(1)绿原酸的相对分子质量=
(2)绿原酸中碳元素和氧元素的质量比为
(3)100g绿原酸中含碳元素的质量是多少?(写出计算过程,结果精确到0.1g)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】科学家经过多年研究证明,有一些同学爱吃的小包装零食中,含一定量的有毒、有害、致病的化学物质,如某些油炸食品中含有致癌物质丙烯酰胺(C3H5NO)。请你根据丙烯酰胺(C3H5NO)的化学式计算后填写:
(1)丙烯酰胺(C3H5NO)的相对分子质量为_________ 。
(2)丙烯酰胺中碳元素和氧元素的质量比是________ 。
(3)355g丙烯酰胺中含氢元素的质量为_______ g。
(4)_______ g丙烯酰胺中与14g一氧化碳中所含碳元素质量相等。
(1)丙烯酰胺(C3H5NO)的相对分子质量为
(2)丙烯酰胺中碳元素和氧元素的质量比是
(3)355g丙烯酰胺中含氢元素的质量为
(4)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】维生素C的化学式是:C6H8O6,它主要存在于蔬菜,水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。试计算:
(1)维生素C的相对分子质量;
(2)维生素C中碳、氢两种元素的质量比(化成最简比);
(3)维生素C中碳元素的质量分数。
(1)维生素C的相对分子质量;
(2)维生素C中碳、氢两种元素的质量比(化成最简比);
(3)维生素C中碳元素的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】我国科学家屠呦呦因为发现青蒿素(化学式为C15H22O5).一种用于治疗疟疾的药物。挽救了全球数百万人的生命而荣获2015年诺贝尔生理学或医学奖。
(1)每个青蒿素分子中共含有______个原子 .其相对分子质量为_____________________。
(2)青蒿素由___________________种元素组成,其中碳.氢两种元素的质量比为______________________。
(3)计算141 g青蒿素中所含氧元素的质量。(写出计算过程)
(1)每个青蒿素分子中共含有______个原子 .其相对分子质量为_____________________。
(2)青蒿素由___________________种元素组成,其中碳.氢两种元素的质量比为______________________。
(3)计算141 g青蒿素中所含氧元素的质量。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】尿素[CO(NH2)2]是氮肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响。计算:
(1)CO(NH2)2中共含有_________ (写数字)种元素。
(2)CO(NH2)2的相对分子质量是_________ 。
(3)CO(NH2)2分子中各原子数目比为__________ 。
(4)CO(NH2)2中各元素间的质量比为___________ 。
(5)若CO(NH2)2中含有3 g氮元素,则该CO(NH2)2的质量为_________ g(计算结果精确到0.1)。
(6)若某农田需要60千克尿素[CO(NH2)2]作氮肥,现因缺货改用碳酸氢铵,
(NH4HCO3),问:需向田间施用多少千克碳酸氢铵﹖(需写出步骤)
(1)CO(NH2)2中共含有
(2)CO(NH2)2的相对分子质量是
(3)CO(NH2)2分子中各原子数目比为
(4)CO(NH2)2中各元素间的质量比为
(5)若CO(NH2)2中含有3 g氮元素,则该CO(NH2)2的质量为
(6)若某农田需要60千克尿素[CO(NH2)2]作氮肥,现因缺货改用碳酸氢铵,
(NH4HCO3),问:需向田间施用多少千克碳酸氢铵﹖(需写出步骤)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】过氧化氢的化学式为H2O2,俗称双氧水,外观为无色透明液体,是一种强氧化剂,其水溶液适用于医用伤口消毒及环境消毒和食品消毒,也能与高锰酸钾溶液反应如下: 2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5X+8H2O。
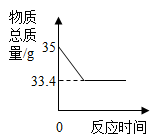
在一般情况下会分解成水和氧气,但分解速度极其慢,加快其反应速度的办法是加入催化剂——二氧化锰或用短波射线照射。实验室用34克过氧化氢水溶液和1克二氧化锰制取氧气,实验的相关数据如图。请回答:
(1)过氧化氢与高锰酸钾溶液反应中,X的化学式为_____ 。
(2)过氧化氢分解过程中氧元素的化合价是___ (填“升高”“降低”或“既有升高又有降低”)。
(3)二氧化锰作为催化剂在化学反应前后本身的___ 都没有发生变化。
(4)反应生成氧气的质量为____ g。
(5)计算34g过氧化氢水溶液中H2O2的质量_ g。(利用化学方程式计算,写出计算过程)
在一般情况下会分解成水和氧气,但分解速度极其慢,加快其反应速度的办法是加入催化剂——二氧化锰或用短波射线照射。实验室用34克过氧化氢水溶液和1克二氧化锰制取氧气,实验的相关数据如图。请回答:

(1)过氧化氢与高锰酸钾溶液反应中,X的化学式为
(2)过氧化氢分解过程中氧元素的化合价是
(3)二氧化锰作为催化剂在化学反应前后本身的
(4)反应生成氧气的质量为
(5)计算34g过氧化氢水溶液中H2O2的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某学校同学们暑期到江西宜丰具开展研学活动,参观智慧农场,了解水肥一体、自动滴灌等农业生产新技术。
(1)从爱护水资源方面分析、与大水漫灌相比,滴灌的优点是_______ 。
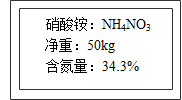
(2)水肥一体、也就是将化肥溶解在灌溉的水中,灌溉与施肥融为一体。同学们看到农场有一袋硝酸铵固体化肥,包装说明如图所示:
①NH4NO3中划线元素的化合价是_______
②写出硝酸铵中阴离子的符号:_______
③这袋化肥中含有的氮元素的质量为_______ kg。
④这袋化肥中硝酸铵的质量分数是多少?_______ (写出计算过程)
⑤这袋化肥属于_______ (选填“纯净物”或“混合物”)。
(1)从爱护水资源方面分析、与大水漫灌相比,滴灌的优点是
(2)水肥一体、也就是将化肥溶解在灌溉的水中,灌溉与施肥融为一体。同学们看到农场有一袋硝酸铵固体化肥,包装说明如图所示:

①NH4NO3中划线元素的化合价是
②写出硝酸铵中阴离子的符号:
③这袋化肥中含有的氮元素的质量为
④这袋化肥中硝酸铵的质量分数是多少?
⑤这袋化肥属于
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】钙及其化合物在生活生产中有广泛的应用。
项目三:增氧剂中的钙
(1)鱼类长途运输的增氧剂的主要成分为过氧化钙(CaO2),CaO2中氧元素的化合价为___________ ,它与水缓慢反应的方程式为2CaO2+2H2O=2Ca(OH)2+O2↑。为测定所用过氧化钙的质量分数,称取2.0g样品加入足量的水中,生成224mL氧气(其密度为1.43g/L),试计算所用样品中过氧化钙的质量分数______ (写出计算过程,精确到0.1%)。
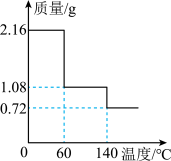
(2)2.16gCaO2•8H2O受热过程中质量随温度变化曲线如图,140℃完全脱水,试确定60℃时CaO2•xH2O中x=___________ 。
项目三:增氧剂中的钙
(1)鱼类长途运输的增氧剂的主要成分为过氧化钙(CaO2),CaO2中氧元素的化合价为
(2)2.16gCaO2•8H2O受热过程中质量随温度变化曲线如图,140℃完全脱水,试确定60℃时CaO2•xH2O中x=
您最近一年使用:0次



