(2011年广东,23题)学习了MnO2对过氧化氢有催化作用的知识后。某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究。
【猜想】Ⅰ. CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ. CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ. CuO是反应的催化剂,反应前后_______________________________ 。
【实验】用天平称量0.2gCuO,取5ml5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
(2)步骤①的目的_____________________ 。
(3)步骤④需用到的实验仪器有:铁甲台(带铁圈)、漏斗、烧杯、__________ 。
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为___________________ 。
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是______________ (写一种)。
【猜想】Ⅰ. CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ. CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ. CuO是反应的催化剂,反应前后
【实验】用天平称量0.2gCuO,取5ml5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
带火星的木条复燃 | 溶液中有气泡放出 | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(2)步骤①的目的
(3)步骤④需用到的实验仪器有:铁甲台(带铁圈)、漏斗、烧杯、
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是
更新时间:2017-06-11 10:56:58
|
相似题推荐
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】高锰酸钾在生产、生活中有广泛的应用。实验小组同学查阅资料得知,草酸(H2C2O4)可使滴有硫酸的高锰酸钾溶液褪色,但不同条件下褪色时间不同,即反应的速率不同。小组同学进行了如下探究。
【提出问题1】影响该反应反应速率的因素有哪些?
【作出猜想】影响该反应反应速率的因素有温度、催化剂、硫酸的浓度等。
【查阅资料]】硫酸锰(MnSO4)可作该反应的催化剂。
【进行实验】(如图)

取A、B、C、D4支试管,每支试管中分别加入4mL浓度为0.08%的KMnO4溶液、0.4mL的硫酸、1mL浓度为0.09%的H2C2O4溶液。
【实验记录】
【解释与结论】
(1)4支试管中作为对照实验的是________ (填序号)。
(2)探究催化剂对该反应反应速率影响的实验是_______ 。(填序号)
(3)设计实验A和B的目的是_______ 。
(4)对比实验B和C可得出的结论是________ 。
【提出问题1】影响该反应反应速率的因素有哪些?
【作出猜想】影响该反应反应速率的因素有温度、催化剂、硫酸的浓度等。
【查阅资料]】硫酸锰(MnSO4)可作该反应的催化剂。
【进行实验】(如图)

取A、B、C、D4支试管,每支试管中分别加入4mL浓度为0.08%的KMnO4溶液、0.4mL的硫酸、1mL浓度为0.09%的H2C2O4溶液。
【实验记录】
| 序号 | 所滴硫酸浓度 | 温度 | 催化剂 | 高锰酸钾完全褪色时间 |
| A | 98% | 室温 | 无 | 72s |
| B | 65% | 室温 | 无 | 129s |
| C | 65% | 50℃ | 无 | 16s |
| D | 65% | 室温 | MnSO4 | 112s |
(1)4支试管中作为对照实验的是
(2)探究催化剂对该反应反应速率影响的实验是
(3)设计实验A和B的目的是
(4)对比实验B和C可得出的结论是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】实验学校的同学们在学习了催化剂的知识后提出:氧化铁固体(Fe2O3,难溶于水)在双氧水制氧气的反应中能否起到类似二氧化锰的催化作用呢?于是进行了以下探究:
【猜想】
Ⅰ、Fe2O3既不是催化剂,也不是反应物,反应前后质量和化学性质不变;
Ⅱ、Fe2O3是反应物,要生成O2,反应前后质量和化学性质要改变;
Ⅲ、Fe2O3是该反应的催化剂,反应前后____________ ;
【实验】用天平称量1g Fe2O3固体,取10mL10%的双氧水于试管中,进行实验:
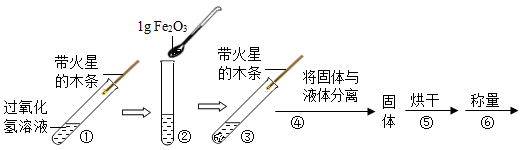
(1)实验过程中记录现象如下:
(2)老师指出上述实验不能证明Fe2O3是该反应的催化剂,理由是__________ ;
A、只有二氧化锰能起催化作用 B、未验证回收的固体是否仍是Fe2O3
C、未验证回收的固体的物理性质 D、未验证Fe2O3是否改变反应速率
(3)Fe2O3催化分解双氧水的化学反应式为____________ ;
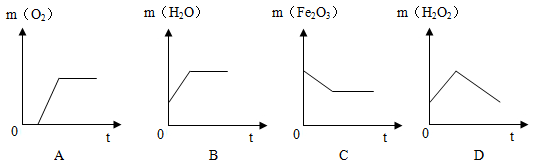
(4)步骤③中,试管中各物质质量随反应时间t变化曲线正确的是_________
【猜想】
Ⅰ、Fe2O3既不是催化剂,也不是反应物,反应前后质量和化学性质不变;
Ⅱ、Fe2O3是反应物,要生成O2,反应前后质量和化学性质要改变;
Ⅲ、Fe2O3是该反应的催化剂,反应前后
【实验】用天平称量1g Fe2O3固体,取10mL10%的双氧水于试管中,进行实验:

(1)实验过程中记录现象如下:
| 步骤①现象 | 步骤③现象 | 步骤⑥ | 结论 |
| 无明显变化 | 称得固体质量为1g | 猜想Ⅲ成立. |
(2)老师指出上述实验不能证明Fe2O3是该反应的催化剂,理由是
A、只有二氧化锰能起催化作用 B、未验证回收的固体是否仍是Fe2O3
C、未验证回收的固体的物理性质 D、未验证Fe2O3是否改变反应速率
(3)Fe2O3催化分解双氧水的化学反应式为
(4)步骤③中,试管中各物质质量随反应时间t变化曲线正确的是

您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】茶垢清洁剂能快速清除茶具上附着的茶垢,同时产生大量气体。某校化学兴趣小组的同学对茶垢清洁剂进行了探究。
【查阅资料】
(1)下图是某品牌茶垢清洁剂说明书中的部分内容:
(2)过碳酸钠具有碳酸钠和过氧化氢的双重性质。
(3)过碳酸钠水溶液中主要含有的微粒为Na+、 、
、 、H2O2和H2O。
、H2O2和H2O。
【提出问题I】茶垢清洁剂溶于水时有气泡产生,该气体是什么?
【猜想1】小军同学猜想是O2,他的依据是过碳酸钠水溶液中含有______ (填写微粒符号),受热会快速分解出氧气。
【猜想2】静静同学猜想是CO2,她的依据是过碳酸钠水溶液中有 ,遇到H+会生成CO2。
,遇到H+会生成CO2。
同学们一致认为她的猜想不正确,理由是过碳酸钠水溶液中含有______ (填写微粒符号),不可能有H+。
【实验、现象、结论】
【提出问题Ⅱ】茶垢清洁剂中过氧化氢迅速分解的原因除了温度外,还有其他因素吗?
【猜想】可能是过碳酸钠溶液中的某种微粒加快了过氧化氢的分解。
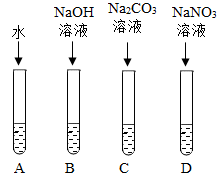
【实验及现象】如图所示向四支装有10毫升5%的过氧化氢溶液的试管中,分别加入水、NaOH溶液、Na2CO3溶液、NaNO3溶液。观察到A、D中没有明显变化,B、C中产生大量气泡。
【分析和结论】
(1)大家认为不需要做A实验,原因是______ 。
(2)对比实验现象可知:对过氧化氢分解有加快作用的微粒为______ 。
【拓展延伸】
茶垢清洁剂溶于水后,持续释放出大量的活性氧,活性氧在水中高速运动,与各种顽固污渍反应,最终达到清洁目的。
【查阅资料】
(1)下图是某品牌茶垢清洁剂说明书中的部分内容:
| 主要成分:过碳酸钠(化学式为:2Na2CO3·2H2O2) 去渍原理:过碳酸钠溶于水时能生成碳酸钠(俗称苏打)和过氧化氢 使用方法:产品与水(50℃左右的热水)按1:20比例配兑,水量以淹盖水垢为准 |
(2)过碳酸钠具有碳酸钠和过氧化氢的双重性质。
(3)过碳酸钠水溶液中主要含有的微粒为Na+、
 、
、 、H2O2和H2O。
、H2O2和H2O。【提出问题I】茶垢清洁剂溶于水时有气泡产生,该气体是什么?
【猜想1】小军同学猜想是O2,他的依据是过碳酸钠水溶液中含有
【猜想2】静静同学猜想是CO2,她的依据是过碳酸钠水溶液中有
 ,遇到H+会生成CO2。
,遇到H+会生成CO2。同学们一致认为她的猜想不正确,理由是过碳酸钠水溶液中含有
【实验、现象、结论】
| 实验操作 | 现象 | 结论 |
在左图所示的试管口塞上带导管的橡皮塞, 将产生的气体通入 | 该气体不是CO2 | ||
拔下橡胶塞,向试管中伸入带火星 的小木条 | 该气体为O2 |
【提出问题Ⅱ】茶垢清洁剂中过氧化氢迅速分解的原因除了温度外,还有其他因素吗?
【猜想】可能是过碳酸钠溶液中的某种微粒加快了过氧化氢的分解。
【实验及现象】如图所示向四支装有10毫升5%的过氧化氢溶液的试管中,分别加入水、NaOH溶液、Na2CO3溶液、NaNO3溶液。观察到A、D中没有明显变化,B、C中产生大量气泡。

【分析和结论】
(1)大家认为不需要做A实验,原因是
(2)对比实验现象可知:对过氧化氢分解有加快作用的微粒为
【拓展延伸】
茶垢清洁剂溶于水后,持续释放出大量的活性氧,活性氧在水中高速运动,与各种顽固污渍反应,最终达到清洁目的。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某化学课外小组的同学,在实验室实验时发现一瓶标签破损的无色溶液(如图所示)。

这瓶溶液是什么物质?在老师的指导下,同学们首先提出假设并进行了如下的探究活动。请在空白处完成相应内容。
[提出猜想]这瓶溶液是H2O2溶液。
[设计实验] 在试管中取少量黑色粉末二氧化锰,向其中滴入该无色溶液,立即产生大量气泡。并放出大量的热。
(1)用_____________ 法收集一试管纯净的气体。
(2)反应的化学符号表达式为_____________________ 。
(3)检验收集的气体的方法为______________________ 。
[实验现象]木条复燃。
[实验结论]由以上现象可知此气体是__________ ;该无色溶液是 ____________ ,原假设成立。

这瓶溶液是什么物质?在老师的指导下,同学们首先提出假设并进行了如下的探究活动。请在空白处完成相应内容。
[提出猜想]这瓶溶液是H2O2溶液。
[设计实验] 在试管中取少量黑色粉末二氧化锰,向其中滴入该无色溶液,立即产生大量气泡。并放出大量的热。
(1)用
(2)反应的化学符号表达式为
(3)检验收集的气体的方法为
[实验现象]木条复燃。
[实验结论]由以上现象可知此气体是
您最近一年使用:0次
【推荐2】学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝(Al2O3)是否也可作过氧化氢分解的催化剂。
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂。
(1)【实验验证】
(2)【得出结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂。
【反思提高】经过讨论,有的同学认为只有上述不能证明Al2O3能作过氧化氢分解的催化剂,其原因是催化剂的特点为______ ;因此还要补充一个探究实验三:目的是探究______ 。
(3)【实验三】①准确称量Al2O3(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、______ ;④对比反应前后Al2O3的质量。
(4)【交流讨论】Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
【深入反思】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验,实验的目的是探究______ 。该实验的操作方法为______ 。
(5)经过实验证明,Al2O3可作为过氧化氢分解的催化剂,用Al2O3作催化剂其反应文字表达式为______ 。
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂。
(1)【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 有少量气泡,木条不复燃 | 常温下过氧化氢溶液分解速率很慢。 | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3, 然后将带火星的木条伸入试管中 | 产生大量的气泡,木条复燃 |
(2)【得出结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂。
【反思提高】经过讨论,有的同学认为只有上述不能证明Al2O3能作过氧化氢分解的催化剂,其原因是催化剂的特点为
(3)【实验三】①准确称量Al2O3(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、
(4)【交流讨论】Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
【深入反思】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验,实验的目的是探究
(5)经过实验证明,Al2O3可作为过氧化氢分解的催化剂,用Al2O3作催化剂其反应文字表达式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小王进行H2O2溶液制O2的实验探究。结合下列过程,回答有关问题:
(1)MnO2(一种黑色难溶于水的粉末)作催化剂:向5mL5%的H2O2溶液中加入少量MnO2,产生大量气泡。该反应的文字表达式为___________________________ ,证明产生的气体是O2的方法是_____ 。
(2)FeC13溶液(一种黄色液体)作催化剂:向5mL5%的H2O2溶液中加入2滴一定浓度的 FeC13溶液,立即产生大量气泡。
【已知】 FeCl3溶液中主要含有三种微粒:H2O、Fe3+、Cl—
【问题】哪种微粒对H2O2溶液的分解起催化作用?
【假设】假设一:可能是H2O 假设二:可能是Fe3+ 假设三:可能是Cl—
【分析】①小李认为假设一不可能成立,其理由是__________________________ ;
【实验】
【结论】②假设__________ 成立,而假设一和另一种假设不成立。
(3)实验反思
①对于步骤3而言,步骤2主要是为了排除__________ (填微粒符号)对实验的影响。
②催化剂比较:从便于回收再利用的角度分析,___________________ 更适合做该反应的催化剂。
(1)MnO2(一种黑色难溶于水的粉末)作催化剂:向5mL5%的H2O2溶液中加入少量MnO2,产生大量气泡。该反应的文字表达式为
(2)FeC13溶液(一种黄色液体)作催化剂:向5mL5%的H2O2溶液中加入2滴一定浓度的 FeC13溶液,立即产生大量气泡。
【已知】 FeCl3溶液中主要含有三种微粒:H2O、Fe3+、Cl—
【问题】哪种微粒对H2O2溶液的分解起催化作用?
【假设】假设一:可能是H2O 假设二:可能是Fe3+ 假设三:可能是Cl—
【分析】①小李认为假设一不可能成立,其理由是
【实验】
| 步骤 | 操作 | 现象 |
| 1 | 其他条件不变,向H2O2溶液中加入NaCl溶液(含有H2O、Na+、Cl—) | 无明显变化 |
| 2 | 其他条件不变,向H2O2溶液中加入Na2SO4溶液(含有H2O、Na+、SO42—) | 无明显变化 |
| 3 | 其他条件不变,向H2O2溶液中加入Fe2(SO4)3溶液(含有H2O、Fe3+、SO42—) | 产生大量气泡 |
【结论】②假设
(3)实验反思
①对于步骤3而言,步骤2主要是为了排除
②催化剂比较:从便于回收再利用的角度分析,
您最近一年使用:0次