一种新型环保材料被塑胶跑道工程广泛应用,合成这种新材料的原料是二甲苯烷二异氰酸酯(其分子式式C15H10N2O2)。请回答下列有关问题;
(1)二甲苯烷二异氰酸酯(C15H10N2O2)中氢、氧元素的质量比为______ (填最简整数比)。
(2)二甲苯烷二异氰酸酯(C15H10N2O2)的相对分子质量为_______ 。
(3)500g二甲苯烷二异氰酸酯中含氮元素的质量为____________ g.
(1)二甲苯烷二异氰酸酯(C15H10N2O2)中氢、氧元素的质量比为
(2)二甲苯烷二异氰酸酯(C15H10N2O2)的相对分子质量为
(3)500g二甲苯烷二异氰酸酯中含氮元素的质量为
2017·四川内江·中考真题 查看更多[24]
2024年四川省内江市第一中学中考一模化学考试卷四川省德阳市第二中学2022-2023学年九年级上学期第一次月考化学试题天津市红桥区2021-2022学年九年级下学期结课考化学试题四川省南充市蓬安中学校2021-2022学年九年级上学期期末化学试题黑龙江省双鸭山市集贤县2019-2020学年九年级上学期期末化学试题河南省商丘市睢县2020-2021学年九年级上学期期中化学试题陕西省咸阳市武功县2020-2021学年九年级上学期期中化学试题(已下线)【万唯原创】2018年河南省中考化学面对面卷九年级第四单元湖南湘西州古丈县2019-2020学年九年级上学期期末化学试题2019年6月四川省成都市成华区中考模拟化学试题四川省南充市南部县伏虎中学2017-2018学年九年级上学期期末化学试题四川省绵阳市中学英才学校2019年秋人教版九年级化学上册过关检测试卷(第四单元 课题4 化学式与化合价)【校级联考】山东省德州市齐河县2019届九年级上学期期末考试化学试题湖南省怀化市芷江县2019届九年级上学期期末考试化学试题【校级联考】甘肃省静宁县第二大片区2019届九年级上学期期末联考化学试题(已下线)学易密卷:段考模拟君之2018-2019学年九年级化学上学期期末原创卷B卷(广东)河南2019届九年级人教版化学上册:第四单元 自然界的水同步测试题广东省中山市卓雅外国语学校2018届九年级中考考前信息卷(中考模拟)化学试题【全国区级联考】广东省汕头市潮南区2018届九年级初中毕业生学业考试模拟化学试题(已下线)2年中考1年模拟 专题17 有关化学式的计算(已下线)2年中考1年模拟 专题07 物质组成的表示人教版2018届九年级上册化学同步练习:第四单元 自然界的水安徽省合肥市五十中学西校2018届九年级上学期期中考试化学试题四川省内江市2017年中考化学试题
更新时间:2017-09-14 11:20:24
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】物质之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法。请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序。
| 规律 | 排序 |
| 示例:标准状况下,密度由大到小 | CO2、C2H4、C2H2、CH4 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下面是五种物质的化学式:
①N2②NH3③N2O4④N2O⑤HNO3
(1)五种物质中氮元素的化合价由高到低的顺序是___________ (填字母序号)
(2)分子中含有原子个数由多到少的顺序是____________ (填字母序号)
(3)相对分子质量由大到小的顺序是___________ (填字母序号)
A.③⑤④①② B.⑤③④①② C.③⑤②④①
①N2②NH3③N2O4④N2O⑤HNO3
(1)五种物质中氮元素的化合价由高到低的顺序是
(2)分子中含有原子个数由多到少的顺序是
(3)相对分子质量由大到小的顺序是
A.③⑤④①② B.⑤③④①② C.③⑤②④①
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】某科研小组设计利用稀H2SO4浸取某废弃的氧化铜锌矿(主要成分为CuO和ZnO,其余成分既不与酸反应,也不溶解于水)的方案。部分实验流程如下:

已知:①H2O2、KMnO4是常见的氧化剂
②各离子开始沉淀及完全沉淀时的pH如下表所示。
请根据上述实验流程回答下列问题:
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是_________ ,写出硫酸溶解氧化锌的化学方程式为_________________ 。
(2)“操作1”所需要的主要玻璃仪器有______________________ ,固体1的成分是___________ 。
(3)“氧化”的目的是将Fe2+反应生成Fe3+,以便在后续的操作中将溶液中铁元素除去从产品纯度的角度分析,氧化剂最好选用_________________ (填“H2O2"或“KMnO4”)。
(4)“除铁”过程中加入氨水的目的是通过调节溶液的pH,使Fe3+沉淀而Zn2+不沉淀,pH应控制在_______ 范围之间。
(5)某温度下,Fe(OH)3分解得到一种铁、氧质量比为21:8的氧化物,该氧化物的化式__________________ 。

已知:①H2O2、KMnO4是常见的氧化剂
②各离子开始沉淀及完全沉淀时的pH如下表所示。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是
(2)“操作1”所需要的主要玻璃仪器有
(3)“氧化”的目的是将Fe2+反应生成Fe3+,以便在后续的操作中将溶液中铁元素除去从产品纯度的角度分析,氧化剂最好选用
(4)“除铁”过程中加入氨水的目的是通过调节溶液的pH,使Fe3+沉淀而Zn2+不沉淀,pH应控制在
(5)某温度下,Fe(OH)3分解得到一种铁、氧质量比为21:8的氧化物,该氧化物的化式
您最近一年使用:0次
【推荐2】阅读下列关于味精的科普小文章回答问题。
味精,是国内外广泛使用的增鲜调味品之一,为白色柱状结晶体,其主要成分为谷氨酸钠(C5H8NO4Na)和食盐。味精被摄入人体中,谷氨酸钠与胃酸作用生成谷氨酸和氯化钠,很快被消化吸收为蛋白质,并参与人体中的多种新陈代谢。
经实验测定发现,当味精加热至100℃以上时,会失去鲜味,且有轻微毒性;当pH值在5.5~8.0时,鲜味最强;当pH值小于4.0时鲜味较弱;当pH值大于8.0时由于形成二钠盐而鲜味消失;味精对婴幼儿,特别是几周以内的婴儿生长发育有严重影响,它会造成婴儿体内缺锌,影响宝宝生长发育,并产生智力减退和厌食等不良后果。

(1)味精的物理性质有______ 。
(2)谷氨酸钠进入人体后会转化为______ 。
(3)谷氨酸钠中碳、氢元素的质量比为______ 。
(4)下列关于味精的说法中,合理的是______ 。
A.炒菜时加入味精后产生鲜味只与加热时间有关
B.烹饪时加入味精的最佳时间是大火翻炒时
C.婴幼儿的食品中不应该加入味精
D.味精应避免在酸性或碱性较强的条件下使用
味精,是国内外广泛使用的增鲜调味品之一,为白色柱状结晶体,其主要成分为谷氨酸钠(C5H8NO4Na)和食盐。味精被摄入人体中,谷氨酸钠与胃酸作用生成谷氨酸和氯化钠,很快被消化吸收为蛋白质,并参与人体中的多种新陈代谢。
经实验测定发现,当味精加热至100℃以上时,会失去鲜味,且有轻微毒性;当pH值在5.5~8.0时,鲜味最强;当pH值小于4.0时鲜味较弱;当pH值大于8.0时由于形成二钠盐而鲜味消失;味精对婴幼儿,特别是几周以内的婴儿生长发育有严重影响,它会造成婴儿体内缺锌,影响宝宝生长发育,并产生智力减退和厌食等不良后果。

(1)味精的物理性质有
(2)谷氨酸钠进入人体后会转化为
(3)谷氨酸钠中碳、氢元素的质量比为
(4)下列关于味精的说法中,合理的是
A.炒菜时加入味精后产生鲜味只与加热时间有关
B.烹饪时加入味精的最佳时间是大火翻炒时
C.婴幼儿的食品中不应该加入味精
D.味精应避免在酸性或碱性较强的条件下使用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】汽车的生产和使用与化学密切相关:
(1)车载安全气囊使用了叠氮化钠(NaN3)。在一定条件下NaN3迅速发生分解反应,生成两种单质,该反应的化学方程式为______ 。
(2)汽车防冻液的主要成分是乙二醇(C2H6O2)。乙二醇中碳、氢、氧三种元素的质量比为______ 。
(3)汽油不完全燃烧会产生CO和碳氢化合物,为减少汽车尾气排放,我国将在全国范围内推广车用乙醇汽油,乙醇(C2H5OH)的燃烧比汽油更充分,乙醇完全燃烧的化学方程式为______ 。
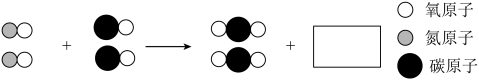
(4)汽车尾气中含有CO、NO等污染物,使用三元催化剂可以将它们转化成CO2和N2,其微观示意图如下图所示,请在方框中补全相应微粒的图示。
(1)车载安全气囊使用了叠氮化钠(NaN3)。在一定条件下NaN3迅速发生分解反应,生成两种单质,该反应的化学方程式为
(2)汽车防冻液的主要成分是乙二醇(C2H6O2)。乙二醇中碳、氢、氧三种元素的质量比为
(3)汽油不完全燃烧会产生CO和碳氢化合物,为减少汽车尾气排放,我国将在全国范围内推广车用乙醇汽油,乙醇(C2H5OH)的燃烧比汽油更充分,乙醇完全燃烧的化学方程式为
(4)汽车尾气中含有CO、NO等污染物,使用三元催化剂可以将它们转化成CO2和N2,其微观示意图如下图所示,请在方框中补全相应微粒的图示。

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】某补钙剂说明书的部分内容如图所示。

(1)碳酸钙的相对分子质量为____________ 。
(2)该钙片中碳酸钙的质量分数为____________ 。
(3)服用2片这种钙片,可摄入_______ 克钙元素?(写出计算过程)

(1)碳酸钙的相对分子质量为
(2)该钙片中碳酸钙的质量分数为
(3)服用2片这种钙片,可摄入
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】合成氨是人类科学技术上一项重大突破,对社会发展与科技进步做出了巨大贡献。合成氨工艺的主要流程如图:

(1)合成塔中反应必须在高温、高压、催化剂条件下进行,该反应属于________ 反应(填基本反应类型)。
(2)生产过程中可重复循环使用的物质是________ 。
(3)根据表中的数据回答问题。
在1.01×105Pa时,欲将NH3与N2、H2分离,最好将温度控制在以下哪个温度________ 。
a.-260℃ b.-200℃ c.-35℃ d.0℃
(4)获得的氨气还可以在一定条件下和二氧化碳反应,合成尿素【化学式为CO(NH2)2】,同时生成水,请写出该反应的文字或符号表达式________ 。若用3.4吨氨气和足量二氧化碳发生反应合成尿素(氮元素全部进入尿素中),理论上能生产尿素的质量为________ 吨。

(1)合成塔中反应必须在高温、高压、催化剂条件下进行,该反应属于
(2)生产过程中可重复循环使用的物质是
(3)根据表中的数据回答问题。
| 物质 | H2 | N2 | NH3 |
| 沸点/℃(1.01×105Pa) | -252 | -195.8 | -33.35 |
a.-260℃ b.-200℃ c.-35℃ d.0℃
(4)获得的氨气还可以在一定条件下和二氧化碳反应,合成尿素【化学式为CO(NH2)2】,同时生成水,请写出该反应的文字或符号表达式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】葡萄糖酸钙锌口服溶液,适用于治疗因缺钙、锌引起的疾病,包括骨质疏松、手足抽搐症、佝偻病等。下图是葡萄糖酸钙锌口服液的说明书摘要,请根据图中信息完成下列问题。

(1)“葡萄糖酸钙锌口服液”中的“钙”和“锌”指的是_______ (填“分子”“原子”“离子”“元素”);它与“补钙剂”相比,优点是_______ 。
(2)碳酸钙中钙元素的质量分数为_______ ;该补钙剂中每片至少含钙元素的质量为_______ 。
(3)成年人按照说明书服用葡萄糖酸钙锌口服液,每天可以补充钙元素的质量至少为_______ mg。
(4)青少年是生长的旺盛时期,研究表明,青少年对钙的需要量远远超过成人。若青少年每天钙的摄入推荐量是1000mg,其中食物中能够提供约50%,若用补钙剂代替葡萄糖酸钙锌口服液,则青少年每天需要服用该补钙剂约_______ 片。

(1)“葡萄糖酸钙锌口服液”中的“钙”和“锌”指的是
(2)碳酸钙中钙元素的质量分数为
(3)成年人按照说明书服用葡萄糖酸钙锌口服液,每天可以补充钙元素的质量至少为
(4)青少年是生长的旺盛时期,研究表明,青少年对钙的需要量远远超过成人。若青少年每天钙的摄入推荐量是1000mg,其中食物中能够提供约50%,若用补钙剂代替葡萄糖酸钙锌口服液,则青少年每天需要服用该补钙剂约
您最近一年使用:0次



