已知硝酸是一种强氧化性酸,能把SO32-氧化成为SO42-,则下列实验方案能够确定某未知试液中存在SO42-的是( )
| A.取少量试液,滴加BaCl2溶液,生成白色沉淀,再加入足量稀盐酸,沉淀不溶解 |
| B.取少量试液,加入足量稀硫酸,没有明显现象,再滴加BaCl2溶液,生成白色沉淀 |
| C.取少量试液,加入足量稀盐酸,没有明显现象,再滴加BaCl2溶液,生成白色沉淀 |
| D.取少量试液,加入足量稀硝酸,没有明显现象,再滴加Ba(NO3)2溶液,生成白色沉淀 |
更新时间:2018-03-20 09:47:19
|
相似题推荐
选择题-单选题
|
适中
(0.65)
解题方法
【推荐1】现有一包白色粉末,可能含有NaC1、Na2SO4、Na2CO3、CuCl2、CaCl2中的一种或几种物质。取少量该白色粉末,加水溶解后得到无色溶液,向所得溶液中加入足量的硝酸钡溶液后,产生白色沉淀,加入足量稀盐酸,溶液沉淀全部溶解。根据上述操作及现象,下面说法中一定正确的是
| A.原粉末中一定有Na2SO4、Na2CO3 |
| B.原粉末中可能有CaCl2、NaCl |
| C.原粉末中一定没有CuCl2、Na2SO4、CaCl2 |
| D.原粉末中只有Na2CO3 |
您最近一年使用:0次
选择题-单选题
|
适中
(0.65)
【推荐2】某河道两旁有甲乙两厂.它们排放的污水各含有下列离子H+、Cu2+、K+、NO3﹣、OH﹣中的三种离子(两厂只含有一种相同的离子).若将两厂的污水按一定比例混合,沉淀后污水会变成无色澄清的中性溶液.下列关于污水的分析,不正确的是( )
| A.Cu2+和OH﹣不可能来自同一工厂 |
| B.Cu2+和 K+可能来自同一工厂 |
| C.H+和OH﹣不可能来自同一工厂 |
| D.NO3﹣和OH﹣ 可能来自同一工厂 |
您最近一年使用:0次
选择题-单选题
|
适中
(0.65)
【推荐1】有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种,取样溶于水,有白色沉淀产生:过滤后向沉淀中滴加盐酸,沉淀完全溶解并有气体产生,由此推断白色固体中
| A.可能存在NaOH | B.可能存在Na2SO4 |
| C.肯定不存在BaCl2 | D.肯定只存在Na2CO3 |
您最近一年使用:0次
选择题-单选题
|
适中
(0.65)
解题方法
【推荐2】如图装置内盛放的物质不同则产生的现象不同,对以下实验现象叙述不正确的是( )
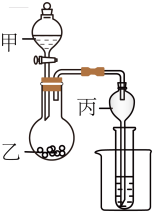

| A.若甲为稀盐酸,乙为贝壳,丙中盛Ca(OH)2溶液,则丙中溶液变浑浊 |
| B.若甲为H2O,乙为CaO固体,丙中盛水,则丙中导管口冒气泡 |
| C.若甲为H2O,乙为NH4NO3固体,丙中盛水,则丙中水会沿导管上升 |
| D.若甲为浓NaOH溶液,乙为NH4NO3固体,丙中盛酚酞溶液,则丙中溶液不变色 |
您最近一年使用:0次




