客家围屋如同城堡,可以抵御外敌入侵。现有A、B、C、D、E 5种物质作为围屋的守护“卫士”,它们分别由氢、碳、氧、钠、钙中的两种或三种元素组成。五种物质间建立起如下图1所示的关系才能组成守护的防线(→表示转化关系),其中物质A和B是氧化物,常用作灭火剂,C、D类别相同。
(1)物质E的俗名______________ 。
(2)生成物质D的化学方程式为____________ ,属于___________ (填基本反应类型)。
(3)现有下列物质作为“外敌”分别对围屋发起进攻,若该物质只要与两位相邻的守护“卫士”都能发生反应就能攻破防线,那么能攻入围屋的物质是__________ 。
①铁 ②稀盐酸 ③氧化铁 ④硫酸铜
(4)室温下,将稀盐酸慢慢滴入装有D溶液的烧杯中,利用温度传感器测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如下图2所示。
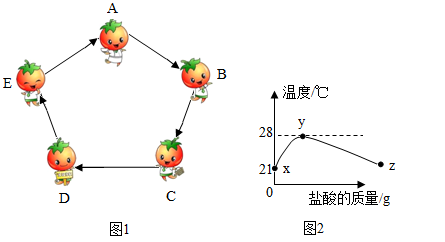
①请解释xy段温度变化的原因____________ 。
②在z处溶液中的溶质是_____________ (填化学式)。
(1)物质E的俗名
(2)生成物质D的化学方程式为
(3)现有下列物质作为“外敌”分别对围屋发起进攻,若该物质只要与两位相邻的守护“卫士”都能发生反应就能攻破防线,那么能攻入围屋的物质是
①铁 ②稀盐酸 ③氧化铁 ④硫酸铜
(4)室温下,将稀盐酸慢慢滴入装有D溶液的烧杯中,利用温度传感器测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如下图2所示。

①请解释xy段温度变化的原因
②在z处溶液中的溶质是
更新时间:2018-05-03 14:59:38
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
【推荐1】下图是一座化学城堡,可以抵御外敌入侵。现有A、B、C、D、E 5种物质作为城堡的守护“卫士”,它们分别由氢、碳、氧、钠、钙中的两种或三种元素组成。五种物质间建立起如图所示的关系才能组成守护的防线,其中物质A和B是常用的灭火剂。

(1)物质A的化学式为_________ .
(2)写出反应C→D的化学方程式__________________ .
(3)现有下列物质作为“外敌”分别对城堡发起进攻,若该物质只要与两位相邻的守护“卫士”都能发生反应就能攻破防线,那么能攻入城堡的物质是_________ .
①铁 ②稀盐酸 ③氧化铁 ④稀硫酸
(4)室温下,将稀盐酸慢慢滴入装有D溶液的烧杯中,利用温度传感器测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如下图所示。

请解释xy段温度变化的原因_______________ 。

(1)物质A的化学式为
(2)写出反应C→D的化学方程式
(3)现有下列物质作为“外敌”分别对城堡发起进攻,若该物质只要与两位相邻的守护“卫士”都能发生反应就能攻破防线,那么能攻入城堡的物质是
①铁 ②稀盐酸 ③氧化铁 ④稀硫酸
(4)室温下,将稀盐酸慢慢滴入装有D溶液的烧杯中,利用温度传感器测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如下图所示。

请解释xy段温度变化的原因
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】甲、乙、丙均为初中化学常见物质,有如图所示的转化关系(“→”表示转化关系,其他物质和反应条件已略去)。其中甲是固态非金属元素组成的单质;丙在空气中按体积分数计算约占0.03%,是植物光合作用的原料之一。

(1)写出物质的化学式:甲______ ;乙______ 。
(2)写出“甲→乙”的反应化学方程式为______ 。
(3)将丙通入澄清石灰水中,石灰水变浑浊,反应的化学方程式为______ 。

(1)写出物质的化学式:甲
(2)写出“甲→乙”的反应化学方程式为
(3)将丙通入澄清石灰水中,石灰水变浑浊,反应的化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐3】如图所示的是物质A~G相互间的关系(“→”表示物质间存在的转化关系,“﹣”表示两端的物质能发生化学反应)A、F都是单质;F是使用最多的金属材料;B是导致温室效应的主要气体;在工业上,C广泛用于玻璃、造纸、纺织和洗涤剂的生产等;D可用于改良酸性土壤;E是一种蓝色溶液。请回答:
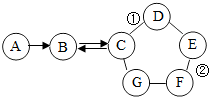
(1)C的化学式_____ ,G可能是_____ (填化学式)。
(2)写出标号①、②的化学反应方程式:①_____ ;②_____ 。
(3)分类观是化学的核心观念之一。以上7种物质中属于氧化物的是_____ (填化学式),属于盐类的是_____ (填化学式)。

(1)C的化学式
(2)写出标号①、②的化学反应方程式:①
(3)分类观是化学的核心观念之一。以上7种物质中属于氧化物的是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】甲、乙、丙、丁是初中化学常见的四种物质,它们之间存在如图所示的变化关系,其中“→”表示转化关系,“﹣”表示相互之间能反应(部分反应物、生成物以及反应条件省略).
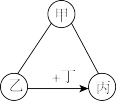
(1)若甲、乙、丙的颜色、状态(常温时)和物质类别如下 :
则丁物质可能是_________ (填化学式)。
(2)若甲、乙、丙、丁属于不同类别的物质。甲是目前世界上年产量最高的金属,乙的溶液中阳离子只有氢离子,丙属于硫酸盐且其溶液为蓝色。
①写出甲与丙反应的化学方程式_______ ,该反应的基本类型是_________ 。
②丁物质_________ (填“一定”或“可能”)属于氧化物。

(1)若甲、乙、丙的颜色、状态(常温时)和物质类别如下 :
| 颜色 | 状态 | 物质类别 | |
| 甲 | 红色 | 固体 | 氧化物 |
| 乙 | 黑 | 固体 | 单质 |
| 丙 | 无色 | 气体 | 氧化物 |
(2)若甲、乙、丙、丁属于不同类别的物质。甲是目前世界上年产量最高的金属,乙的溶液中阳离子只有氢离子,丙属于硫酸盐且其溶液为蓝色。
①写出甲与丙反应的化学方程式
②丁物质
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】请回答下列问题。
I.中国芯彰显中国“智”造,芯片的基材主要是高纯硅。下图是一种制备高纯硅的工艺流程图:

(1)反应I的化学方程式为: ,该反应属于
,该反应属于________ 反应(填“基本反应类型”)。
(2)反应Ⅱ的化学反应方程式为:________ ,该反应要在无氧气环境中进行,原因是________ (答出一种即可)。
(3)所得粗硅应充分洗涤,以除去表面可能含有的盐酸、________ (填“化学式”)。
(4)为了检验得到的粗硅是否洗涤干净,可以向最后一次洗涤液中加入的试剂是________ (填“字母标号”)。
a.铜粉 b.紫色石蕊试液 c.硫酸钠溶液
(5)上述已知生产流程中,可以循环利用的物质是________ (填“化学式”)。
Ⅱ.2060年前我国将实现“碳中和”,可以堪称全球应对环境变化进程的里程碑。“碳中和”的基本途径是“减排”(减少二氧化碳的排放)和“增汇”(增加对二氧化碳的吸收和转化)。
(6)常用的“减排”措施有:植树造林、__________ 等(填一种即可)。
(7)将二氧化碳转化为甲醇(CH3OH),可有效实现“增汇”,甲醇的产率与CuO的质量分数有关,根据下图1,说明在生产中为了提高甲醇的产率,常采用CuO的质量分数是______ %。

(8)CO2与H2在一定条件下转化为CH4(反应过程如上图2所示,虚线处部分中间产物略去),可实现CO2的再利用。
①该反应中,除H2O外另一种生成物为__________ (填“名称”)。
②理论上该反应过程中氧化镁__________ 不断补充(填“需要”或“不需要”)。
I.中国芯彰显中国“智”造,芯片的基材主要是高纯硅。下图是一种制备高纯硅的工艺流程图:

(1)反应I的化学方程式为:
 ,该反应属于
,该反应属于(2)反应Ⅱ的化学反应方程式为:
(3)所得粗硅应充分洗涤,以除去表面可能含有的盐酸、
(4)为了检验得到的粗硅是否洗涤干净,可以向最后一次洗涤液中加入的试剂是
a.铜粉 b.紫色石蕊试液 c.硫酸钠溶液
(5)上述已知生产流程中,可以循环利用的物质是
Ⅱ.2060年前我国将实现“碳中和”,可以堪称全球应对环境变化进程的里程碑。“碳中和”的基本途径是“减排”(减少二氧化碳的排放)和“增汇”(增加对二氧化碳的吸收和转化)。
(6)常用的“减排”措施有:植树造林、
(7)将二氧化碳转化为甲醇(CH3OH),可有效实现“增汇”,甲醇的产率与CuO的质量分数有关,根据下图1,说明在生产中为了提高甲醇的产率,常采用CuO的质量分数是

(8)CO2与H2在一定条件下转化为CH4(反应过程如上图2所示,虚线处部分中间产物略去),可实现CO2的再利用。
①该反应中,除H2O外另一种生成物为
②理论上该反应过程中氧化镁
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
【推荐3】MgSO4•7H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3,还含有少量FeCO3,其它成分忽略)为原料制备MgSO4•7H2O的主要流程如图:
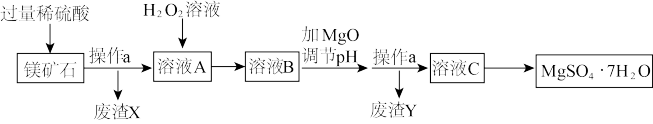
查阅资料:①SiO2既不溶于水也不溶于稀硫酸。
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)MgCO3溶于稀硫酸的化学方程式为_____ 。
(2)为了让镁矿石与稀硫酸充分反应,提高原料利用率,可采取的措施为_____ (填字母)。
A 将镁矿石粉碎 B 降低反应温度 C 用稀硫酸多次浸泡
(3)“溶液A”中加入H2O2溶液会生成Fe2(SO4)3,该反应的化学方程式为_____ 。
(4)选用MgO调节pH使Fe3+转化为沉淀,而不选用NaOH的原因是_____ 。
(5)加氧化镁调节后溶液的pH范围是_____ (用不等式表示)。
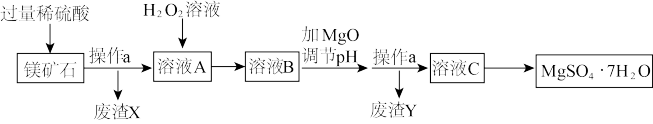
查阅资料:①SiO2既不溶于水也不溶于稀硫酸。
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Mg2+ | Fe2+ | Fe3+ |
| 开始沉淀时的pH | 9.1 | 7.6 | 1.9 |
| 沉淀完全时的pH | 11.1 | 9.7 | 3.2 |
(1)MgCO3溶于稀硫酸的化学方程式为
(2)为了让镁矿石与稀硫酸充分反应,提高原料利用率,可采取的措施为
A 将镁矿石粉碎 B 降低反应温度 C 用稀硫酸多次浸泡
(3)“溶液A”中加入H2O2溶液会生成Fe2(SO4)3,该反应的化学方程式为
(4)选用MgO调节pH使Fe3+转化为沉淀,而不选用NaOH的原因是
(5)加氧化镁调节后溶液的pH范围是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】中和反应是一类重要的化学反应。某同学利用图1实验研究稀盐酸与氢氧化钠液反应的过程,并测量反应过程中溶液的pH和温度的变化情况,得到图2和图3

(1)烧杯中发生反应的化学方程式为_____ ;
(2)滴管A中溶液的溶质是_____ (填化学式);
(3)结合图2中有关信息可知图3中V的数值最接近_____ (填“6”、“12”或“16”);
(4)下列说法正确的是_____ 。
A 图2中b点所示溶液中的溶质是NaCl和HCl
B 取图2中d点所示溶液加热蒸干所得固体为纯净物
C 图2中c→d所示溶液中NaCl的质量不断增加
D 图3中e→f变化趋势可说明该反应是放热反应

(1)烧杯中发生反应的化学方程式为
(2)滴管A中溶液的溶质是
(3)结合图2中有关信息可知图3中V的数值最接近
(4)下列说法正确的是
A 图2中b点所示溶液中的溶质是NaCl和HCl
B 取图2中d点所示溶液加热蒸干所得固体为纯净物
C 图2中c→d所示溶液中NaCl的质量不断增加
D 图3中e→f变化趋势可说明该反应是放热反应
您最近一年使用:0次
【推荐2】为探究稀盐酸的化学性质,兴趣学习小组的同学进行如图所示实验,请根据实验回答下列问题:

(1)实验中无明现象的是______ (填试管编号),下列实验不能证明两者发生了反应的是______ 。
a.测定加入另一反应物前后温度的变化:温度升高
b.测定加入另一反应物前后溶液pH的变化:pH变大
c.先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红
d.取该试管实验后的剩余溶液滴加碳酸钠,无气泡
(2)试管Ⅳ中发生反应的化学方程式是______ 。
(3)为了验证盐酸具有酸的通性,还需添加的实验是:向稀盐酸中加入______ 。

(1)实验中无明现象的是
a.测定加入另一反应物前后温度的变化:温度升高
b.测定加入另一反应物前后溶液pH的变化:pH变大
c.先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红
d.取该试管实验后的剩余溶液滴加碳酸钠,无气泡
(2)试管Ⅳ中发生反应的化学方程式是
(3)为了验证盐酸具有酸的通性,还需添加的实验是:向稀盐酸中加入
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】某兴趣小组在相同条件下,将10.00g下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中所有物质的质量随时间变化如下表,回答下列问题。
(1)图中能反映水在空气中放置时,发生变化的微观示意图是____ (填标号)。
A B
B  C
C  D
D 
(2)为研制一种安全、环保的除湿剂,可选择上表中的____ (填溶质的化学式)。
(3)为确认放置2天的盐酸浓度的变化,作如下的探究:取放置前后的盐酸分别滴入____ 溶液,再滴加_____ 相同的NaOH溶液,边滴加边振荡,当溶液颜色恰好由无色变为红色时,对比试管中溶液体积(如图所示),说明放置后盐酸溶质质量分数变____ (填“大”或“小”)。

(4)氯化钠溶液放置2天后析出0.60g固体,则原氯化钠溶液是____ (填“饱和溶液”或“不饱和溶液”)。(已知该温度下氯化钠的溶解度为36.0g)
| 时间 | 质量/g | |||||
| 水 | 氯化钠溶液 | 盐酸 | 浓硫酸 | 氢氧化钠浓溶液 | 氯化钙溶液 | |
| 1天 | 8.16 | 8.62 | 8.64 | 11.18 | 9.38 | 10.25 |
| 2天 | 5.76 | 6.40 | 6.69 | 12.55 | 8.47 | 10.33 |
A
 B
B  C
C  D
D 
(2)为研制一种安全、环保的除湿剂,可选择上表中的
(3)为确认放置2天的盐酸浓度的变化,作如下的探究:取放置前后的盐酸分别滴入

(4)氯化钠溶液放置2天后析出0.60g固体,则原氯化钠溶液是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】一包固体可能含有镁粉、碳粉、氧化铜、氢氧化钠、氯化钠中的一种或几种。为探究固体的组成,某化学兴趣小组进行了如图所示实验:
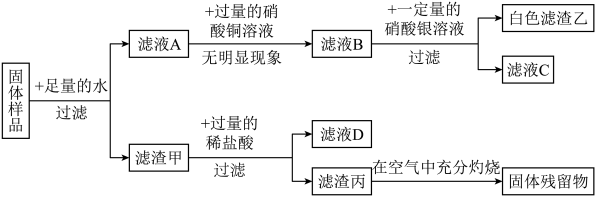
(1)该实验中生成白色沉淀滤渣乙的化学方程式为______ 。
(2)原固体中一定不含有的物质是______ (写化学式,下同),证据是______ 。
(3)原固体中一定含有的物质是______ 。
(4)实验结束后,该兴趣小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,上层清液E为蓝色,经检验,E中不含氯离子,则E中一定含有的溶质是_____ 。

(1)该实验中生成白色沉淀滤渣乙的化学方程式为
(2)原固体中一定不含有的物质是
(3)原固体中一定含有的物质是
(4)实验结束后,该兴趣小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,上层清液E为蓝色,经检验,E中不含氯离子,则E中一定含有的溶质是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】A-E是初中化学常见的物质。A是难溶性盐,B是胃酸的主要成分之一,D在农业上用于中和酸性土壤。它们之间的转化关系如下。(“一”表示相连物质间能反应,“→”表示物质间能转化。部分反应物、生成物及反应条件略)。请回答:
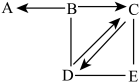
(1)D的化学式_________ 。
(2)B→A的的化学方程式_________ 。
(3)B-D基本反应类型_________ 。
(4)C物质的用途_________ 。

(1)D的化学式
(2)B→A的的化学方程式
(3)B-D基本反应类型
(4)C物质的用途
您最近一年使用:0次



