如图是包含物质A、B、C、D和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生反应。
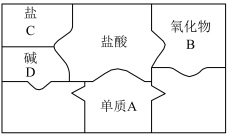
⑴A不可能是______ (填标号)。
a.Mg b.Fe c.Ag d.Zn
⑵若B为铁锈的主要成分Fe2O3,B与盐酸反应的化学方程式为______________ 。
⑶若C为碳酸钠。
①C与D的反应属于______ (填基本反应类型)。
②将二氧化碳通入C溶液,可化合生成碳酸氢钠( NaHCO3),该反应的反应物有______ 种。
⑷D与盐酸反应的化学方程式为_____________________ (写一个)。

⑴A不可能是
a.Mg b.Fe c.Ag d.Zn
⑵若B为铁锈的主要成分Fe2O3,B与盐酸反应的化学方程式为
⑶若C为碳酸钠。
①C与D的反应属于
②将二氧化碳通入C溶液,可化合生成碳酸氢钠( NaHCO3),该反应的反应物有
⑷D与盐酸反应的化学方程式为
更新时间:2018-05-31 19:35:36
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电动独轮车是新一代的节能、环保、便携的代步工具。它体形小巧、携带方便,最轻的一款只有10kg,可以直接放进汽车后备箱,提到家里或是办公室。
(1)制造电动独轮车所用的主要材料最好是___________ ;(在A、B、C中选填)
A.韧性好、硬度大的锰钢 B.强度好、密度小的铝合金 C.美观的黄金
(2)电动独轮车充电2个小时,可以行驶25Km,短途代步非常方便,可以代替公交和地铁。电动独轮车在行走时是由___________ 能转化为机械能;
(3)电动独轮车中许多电线为铜制的,铜能和浓硝酸(HNO3)反应,生成硝酸铜、二氧化氮和水,且二氧化氮与水的分子个数比为1:1,其反应方程式为___________ ,反应前氮元素的化合价为___________ ;
(4)在环境污染日益严重的背景下,电动车的大力普及,可缓解资源的消耗并减少含铅化合物、氮的氧化物、未燃烧的碳氢化合物以及___________ 和___________ 等汽车尾气的排放。
(1)制造电动独轮车所用的主要材料最好是
A.韧性好、硬度大的锰钢 B.强度好、密度小的铝合金 C.美观的黄金
(2)电动独轮车充电2个小时,可以行驶25Km,短途代步非常方便,可以代替公交和地铁。电动独轮车在行走时是由
(3)电动独轮车中许多电线为铜制的,铜能和浓硝酸(HNO3)反应,生成硝酸铜、二氧化氮和水,且二氧化氮与水的分子个数比为1:1,其反应方程式为
(4)在环境污染日益严重的背景下,电动车的大力普及,可缓解资源的消耗并减少含铅化合物、氮的氧化物、未燃烧的碳氢化合物以及
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】工业上利用海水提取粗盐的过程如图所示,回答有关问题:

(1)一定质量的海水,通过贮水池引入到蒸发池中,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量会______ (填“增大”、“不变”或“减小”)。在蒸发池中,经过风吹日晒使水部分蒸发,该变化是______ (填“物理变化”或“化学变化”)。
(2)结晶池里得到的母液中氯化钠溶液是______ (填“饱和”或“不饱和”)溶液。在粗盐精制成精盐的过程中,一般采用______ 的方法除去不溶性杂质。
(3)工业上常用电解饱和的食盐水制取氢氧化钠,同时得到氢气和氯气,反应时的化学方程式为______ 。

(1)一定质量的海水,通过贮水池引入到蒸发池中,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量会
(2)结晶池里得到的母液中氯化钠溶液是
(3)工业上常用电解饱和的食盐水制取氢氧化钠,同时得到氢气和氯气,反应时的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】为保护绿水青山,可将工业含铜废酸液(主要成分为CuSO4和H2SO4)进行无害化处理,制取硫酸钡(BaSO4)和硫化铜(CuS)主要流程如下:

资料:BaSO4、CuS难溶于水且不与稀硫酸反应:Cu(OH)2难溶于水,可与稀硫酸反应。
(1)从过滤器中分离出滤渣的成分为_____ 。
(2)反应釜3中发生复分解反应的化学方程式为___ 。

资料:BaSO4、CuS难溶于水且不与稀硫酸反应:Cu(OH)2难溶于水,可与稀硫酸反应。
(1)从过滤器中分离出滤渣的成分为
(2)反应釜3中发生复分解反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
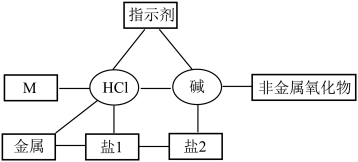
【推荐2】某同学归纳出酸碱盐的化学性质之间的关系如图所示(图中“—”表示相连的两种物质能反应)。___________ 。
(2)若图中的碱为Ba(OH)2,向稀盐酸中滴入一定量Ba(OH)2溶液,发生反应的化学方程式为___________ ,向反应后的溶液中滴加几滴无色酚酞试液,溶液变红,则混合液中含有的阴离子是 ___________ 。
(3)若图中的碱为NaOH,则金属、盐1和盐2满足以上关系的是 ___________(填字母)。
(2)若图中的碱为Ba(OH)2,向稀盐酸中滴入一定量Ba(OH)2溶液,发生反应的化学方程式为
(3)若图中的碱为NaOH,则金属、盐1和盐2满足以上关系的是 ___________(填字母)。
| A.Mg、KCl、CuSO4 |
| B.Fe、AgNO3、FeCl3 |
| C.Cu、Na2CO3、CaCl2 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】以固体废弃物粉煤灰(主要为SiO2、A12O3、FeO、Fe2O3、CaO等)为原料制备Al2O3的流程如下:

Ⅰ.粉煤灰中的Al2O3、FeO、Fe2O3不溶于稀盐酸;SiO2不与盐酸、硫酸反应。
Ⅱ.此流程中SO2可将Fe3+还原为Fe2+氢氧化物沉淀的pH:Fe(OH)3沉淀区间为1.94~3.20;Fe(OH)2沉淀区间为7.06~8.95;Al(OH)3沉淀区间为3.69~4.89。
(1)第一次酸浸时发生反应的化学方程式:__ 。采用两次酸浸而不直接用浓硫酸浸取的目的是__ 。提高热浸时反应速率可以采取的措施为_____ 。
(2)滤渣的主要成分为_______ (填化学式)。
(3)①氨水的浓度不同,铁、铝的沉淀率如图所示,当pH大于5.0时,产生的沉淀最终显浅黄色,其原因是_______ 。

②该流程中通过在Fe2+和A13+体系中分离铝铁,而没有在Fe3+和A13+体系中分离,其原因是_ 。

Ⅰ.粉煤灰中的Al2O3、FeO、Fe2O3不溶于稀盐酸;SiO2不与盐酸、硫酸反应。
Ⅱ.此流程中SO2可将Fe3+还原为Fe2+氢氧化物沉淀的pH:Fe(OH)3沉淀区间为1.94~3.20;Fe(OH)2沉淀区间为7.06~8.95;Al(OH)3沉淀区间为3.69~4.89。
(1)第一次酸浸时发生反应的化学方程式:
(2)滤渣的主要成分为
(3)①氨水的浓度不同,铁、铝的沉淀率如图所示,当pH大于5.0时,产生的沉淀最终显浅黄色,其原因是

②该流程中通过在Fe2+和A13+体系中分离铝铁,而没有在Fe3+和A13+体系中分离,其原因是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】以粗盐为原料生产ClO2(可用于自来水消毒)的工艺主要包括:①粗盐精制;②电解微酸性NaCl溶液;③ClO2的制取。工艺流程如下图,其中反应Ⅲ制取ClO2的化学方程式为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。

(1)试剂X是_____ (填化学式);操作A的名称是_____ 。
(2)加入适量HCl除为了满足电解时的微酸性外,还能除去溶液中的杂质离子,其中所发生的中和反应的化学方程式:_____ 。
(3)为提高经济效益,生产过程中除将H2和Cl2制成HCl充分利用外,还可循环使用的物质Y是_____ 。

(1)试剂X是
(2)加入适量HCl除为了满足电解时的微酸性外,还能除去溶液中的杂质离子,其中所发生的中和反应的化学方程式:
(3)为提高经济效益,生产过程中除将H2和Cl2制成HCl充分利用外,还可循环使用的物质Y是
您最近一年使用:0次
【推荐2】海洋是地球上最大的储水库,浩瀚的海洋蕴藏着丰富的化学资源.
(1)目前世界上60%的镁是从海水中提取的.其主要步骤如下:

①提取Mg的过程中,试剂A可以选用__________________ ,试剂B选用_______________ ,由无水MgCl2制取Mg的基本反应类型为________________________ 。
②分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、Na2CO3溶液,过滤,再向滤液中加入适量盐酸.实验中加入过量BaCl2溶液是为了除去________ ;加入过量Na2CO3溶液的目的是_______________________________ 。
(2)从海水中制得的氯化钠除可以食用外,还常用作工业原料生产相应的化工产品,如工业上利用氯化钠和水在通电条件下生成烧碱、氢气和氯气,试写出上述化学方程式:__________________________ 。
(1)目前世界上60%的镁是从海水中提取的.其主要步骤如下:

①提取Mg的过程中,试剂A可以选用
②分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、Na2CO3溶液,过滤,再向滤液中加入适量盐酸.实验中加入过量BaCl2溶液是为了除去
(2)从海水中制得的氯化钠除可以食用外,还常用作工业原料生产相应的化工产品,如工业上利用氯化钠和水在通电条件下生成烧碱、氢气和氯气,试写出上述化学方程式:
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐3】如图所示,部分反应物、生成物均已略去;所涉及的物质和反应在初中化学中较常见,且A-E为五种不同类别的物质,B是目前年产量最高的金属,C和F可用于配制农药波尔多液。请回答:

(1)E的化学式为_____________________ 。
(2)写出F的另一种用途______________________ 。
(3)F→D的化学方程式为___________________________ 。

(1)E的化学式为
(2)写出F的另一种用途
(3)F→D的化学方程式为
您最近一年使用:0次



