如图是实验室的部分实验装置图,回答有关问题:
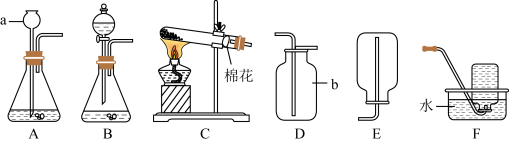
(1)写出仪器名称:a是_______________________ 。
(2)用A装置制取二氧化碳时长颈漏斗插入液面以下的目的是__________________ ,A中发生反应的化学方程式为 _____________________________________ ;收集二氧化碳应选用的装置是 ________ (填序号)。
(3)制取二氧化碳实验结束时,小丽同学将A装置锥形瓶中的溶液(底部没有固体)倒入烧杯中,对溶液中的溶质进行了探究。
【问题】溶液中溶质的成分有哪些?
【猜想】小刚的猜想:溶液中的溶质是氯化钙
小华的猜想:溶液中的溶质是____________________ 。
【实验证明】小方用试管取少量溶液,分别向溶液中加入下列试剂中的______ (填序号),如果没有明显现象就证明小刚的猜想正确。
①氢氧化钙溶液 ②石蕊试液 ③酚酞溶液 ④大理石

(1)写出仪器名称:a是
(2)用A装置制取二氧化碳时长颈漏斗插入液面以下的目的是
(3)制取二氧化碳实验结束时,小丽同学将A装置锥形瓶中的溶液(底部没有固体)倒入烧杯中,对溶液中的溶质进行了探究。
【问题】溶液中溶质的成分有哪些?
【猜想】小刚的猜想:溶液中的溶质是氯化钙
小华的猜想:溶液中的溶质是
【实验证明】小方用试管取少量溶液,分别向溶液中加入下列试剂中的
①氢氧化钙溶液 ②石蕊试液 ③酚酞溶液 ④大理石
更新时间:2018-06-02 09:31:19
|
相似题推荐
科学探究题
|
较难
(0.4)
解题方法
【推荐1】运用化学知识,开展科学探究。
【探究一】海洋封存是实现“碳中和”的途径之一,其原理是利用 在水等溶剂中的溶解性来吸收
在水等溶剂中的溶解性来吸收 ,某小组开展如下探究。
,某小组开展如下探究。
(1)活动一: 在水和食盐水(模拟海水)中的溶解情况
在水和食盐水(模拟海水)中的溶解情况 (如图1),待收集
(如图1),待收集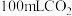 后,移出导管,每隔一段时间观察并记录量筒内
后,移出导管,每隔一段时间观察并记录量筒内 体积。重复实验,所测数据平均值如下表:
体积。重复实验,所测数据平均值如下表:
①图1发生装置中反应的化学方程式为________ 。
②由上表数据分析:
a.能用排水法收集 的理由是
的理由是________ 。
b.相同条件下,等体积水和食盐水吸收 更多的是
更多的是________ (填“水”或“食盐水”)。
(2)活动二:探究植物油隔离对 在水中溶解情况的影响
在水中溶解情况的影响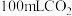 倒置于水槽中,向其中一个量筒内注入少量植物油,使
倒置于水槽中,向其中一个量筒内注入少量植物油,使 与水被植物油隔开(
与水被植物油隔开( 与植物油不反应),测得量筒内
与植物油不反应),测得量筒内 体积随时间变化曲线如图2。分析该图可得出的结论是
体积随时间变化曲线如图2。分析该图可得出的结论是________ 。
(3)活动三:深度探究“活动二”中 的溶解情况
的溶解情况 分子的微观示意图。请参照图3的表示方式,在图4方框中画出有植物油隔离时,量筒内植物油和水中存在的分子的微观示意图
分子的微观示意图。请参照图3的表示方式,在图4方框中画出有植物油隔离时,量筒内植物油和水中存在的分子的微观示意图_______ (植物油分子用 表示)。
表示)。
②为检验有植物油隔离时 是否会进入水中,请设计实验方案:
是否会进入水中,请设计实验方案:________ 。
【探究二】化学兴趣小组的同学们在进行“碱与酸碱指示剂反应”的实验时,将酚酞溶液滴入 溶液中,溶液变成了红色,但过一会儿红色却消失了。于是,兴趣小组的同学们对这一异常现象进行了探究。
溶液中,溶液变成了红色,但过一会儿红色却消失了。于是,兴趣小组的同学们对这一异常现象进行了探究。
【提出问题】滴有酚酞的 溶液由红色褪为无色的原因是什么?
溶液由红色褪为无色的原因是什么?
【猜想与假设】甲同学:酚酞与 发生了反应;乙同学:
发生了反应;乙同学: 溶液与空气中的
溶液与空气中的 发生了反应;丙同学:与
发生了反应;丙同学:与 溶液浓度大小有关。
溶液浓度大小有关。
【设计与实验】甲、乙、丙三位同学为了验证各自的猜想,设计并进行了如下实验,请你与他们一起探究。
③甲同学设计并完成如下实验:
④乙同学设计图所示的装置进行实验,一段时间后,试管中溶液的红色褪去,他认为自己的猜想正确,试管中反应的化学方程式为________ 。丁同学认为乙同学的猜想不正确,理由是________ 。丁同学为了进一步探究试管中溶液红色褪去的原因,用 试纸测试管中的溶液,结果
试纸测试管中的溶液,结果 ,说明溶液显酸性,造成试管中溶液红色褪去的原因可能是
,说明溶液显酸性,造成试管中溶液红色褪去的原因可能是________ 。 溶液,然后各滴加2滴酚酞溶液,同时放入色度传感器进行测量.测出溶液颜色的变化曲线如图所示,由此判断自己的猜想正确。你能从变化曲线中总结出的规律有
溶液,然后各滴加2滴酚酞溶液,同时放入色度传感器进行测量.测出溶液颜色的变化曲线如图所示,由此判断自己的猜想正确。你能从变化曲线中总结出的规律有________ (写一条)。 溶液由红色褪为无色与
溶液由红色褪为无色与 溶液的浓度有关。
溶液的浓度有关。
【探究一】海洋封存是实现“碳中和”的途径之一,其原理是利用
 在水等溶剂中的溶解性来吸收
在水等溶剂中的溶解性来吸收 ,某小组开展如下探究。
,某小组开展如下探究。(1)活动一:
 在水和食盐水(模拟海水)中的溶解情况
在水和食盐水(模拟海水)中的溶解情况
 (如图1),待收集
(如图1),待收集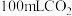 后,移出导管,每隔一段时间观察并记录量筒内
后,移出导管,每隔一段时间观察并记录量筒内 体积。重复实验,所测数据平均值如下表:
体积。重复实验,所测数据平均值如下表:| 时间/h | 0 | 0.5 | 6 | 12 | 24 | 48 |
排水法时 体积/ 体积/ | 100 | 98.5 | 85.5 | 77 | 66 | 59 |
排食盐水时 体积/ 体积/ | 100 | 99 | 93 | 90.5 | 89 | 88 |
②由上表数据分析:
a.能用排水法收集
 的理由是
的理由是b.相同条件下,等体积水和食盐水吸收
 更多的是
更多的是(2)活动二:探究植物油隔离对
 在水中溶解情况的影响
在水中溶解情况的影响
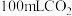 倒置于水槽中,向其中一个量筒内注入少量植物油,使
倒置于水槽中,向其中一个量筒内注入少量植物油,使 与水被植物油隔开(
与水被植物油隔开( 与植物油不反应),测得量筒内
与植物油不反应),测得量筒内 体积随时间变化曲线如图2。分析该图可得出的结论是
体积随时间变化曲线如图2。分析该图可得出的结论是(3)活动三:深度探究“活动二”中
 的溶解情况
的溶解情况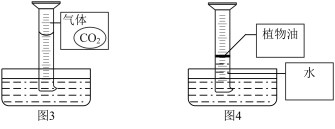
 分子的微观示意图。请参照图3的表示方式,在图4方框中画出有植物油隔离时,量筒内植物油和水中存在的分子的微观示意图
分子的微观示意图。请参照图3的表示方式,在图4方框中画出有植物油隔离时,量筒内植物油和水中存在的分子的微观示意图 表示)。
表示)。②为检验有植物油隔离时
 是否会进入水中,请设计实验方案:
是否会进入水中,请设计实验方案:【探究二】化学兴趣小组的同学们在进行“碱与酸碱指示剂反应”的实验时,将酚酞溶液滴入
 溶液中,溶液变成了红色,但过一会儿红色却消失了。于是,兴趣小组的同学们对这一异常现象进行了探究。
溶液中,溶液变成了红色,但过一会儿红色却消失了。于是,兴趣小组的同学们对这一异常现象进行了探究。【提出问题】滴有酚酞的
 溶液由红色褪为无色的原因是什么?
溶液由红色褪为无色的原因是什么?【猜想与假设】甲同学:酚酞与
 发生了反应;乙同学:
发生了反应;乙同学: 溶液与空气中的
溶液与空气中的 发生了反应;丙同学:与
发生了反应;丙同学:与 溶液浓度大小有关。
溶液浓度大小有关。【设计与实验】甲、乙、丙三位同学为了验证各自的猜想,设计并进行了如下实验,请你与他们一起探究。
③甲同学设计并完成如下实验:
| 实验步骤 | 实验目的 | 实验现象 | 实验结论 |
取少量实验中的 溶液于试管中,加热煮沸 溶液于试管中,加热煮沸 | 溶液变红,过一会儿红色消失 | 甲同学的猜想 | |
| 将①中的溶液冷却后滴入酚酞溶液,并滴一些植物油在其上方 | 隔绝氧气 |
 试纸测试管中的溶液,结果
试纸测试管中的溶液,结果 ,说明溶液显酸性,造成试管中溶液红色褪去的原因可能是
,说明溶液显酸性,造成试管中溶液红色褪去的原因可能是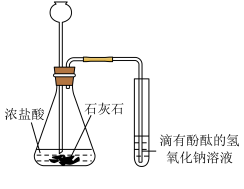
 溶液,然后各滴加2滴酚酞溶液,同时放入色度传感器进行测量.测出溶液颜色的变化曲线如图所示,由此判断自己的猜想正确。你能从变化曲线中总结出的规律有
溶液,然后各滴加2滴酚酞溶液,同时放入色度传感器进行测量.测出溶液颜色的变化曲线如图所示,由此判断自己的猜想正确。你能从变化曲线中总结出的规律有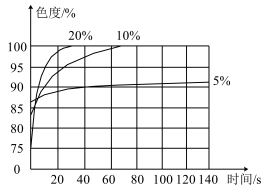
 溶液由红色褪为无色与
溶液由红色褪为无色与 溶液的浓度有关。
溶液的浓度有关。
您最近半年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】某实验小组对“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”感到非常好奇,于是设计实验进行探究.

【提出问题】过氧化钠是否为一种制氧剂?能与人呼出的哪种气体发生反应?
【查阅资料】①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等.
②CO2+2NaOH=Na2CO3+H2O.氢氧化钠溶液对二氧化碳的吸收能力较强.
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
【进行实验】
(1)实验Ⅰ:验证过氧化钠与氮气反应并生成氧气(实验操作如图甲所示).
实验现象及结论:观察到_____ 现象,判断过氧化钠与氮气没有发生反应.
(2)实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气.(实验操作如图乙所示)其中A装置的作用是_____ ,发生的变化是_____ .(填“物理变化”或“化学变化”)
实验现象及结论:用带火星的木条检验C中气体成分,结果带火星的木条复燃;证明过氧化钠与水蒸气发生反应并生成氧气.实验中这种验证氧气的方法是利用了氧气的_____ 的性质.请补充完整该反应的化学方程式:2H2O+2Na2O2=4_____ +O2。
(3)实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.(实验操作如图丙所示)
实验操作:①检查装置的气密性,向装置中加入药品.②打开分液漏斗活塞,向A装置中缓慢加入稀盐酸.③一段时间后用带火星的木条在D内进行检验.实验时观察到A装置中有气泡冒出,固体逐渐减少;D中带火星的木条复燃。则A中发生反应的化学方程式为_____ 。
实验结论:过氧化钠与二氧化碳发生反应并生成氧气.
【实验反思】①根据实验Ⅲ,过氧化钠和二氧化碳反应后,还会生成另一种物质,该物质属于_____ (填“单质”或“化合物”)
②某同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是_____

【提出问题】过氧化钠是否为一种制氧剂?能与人呼出的哪种气体发生反应?
【查阅资料】①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等.
②CO2+2NaOH=Na2CO3+H2O.氢氧化钠溶液对二氧化碳的吸收能力较强.
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
【进行实验】
(1)实验Ⅰ:验证过氧化钠与氮气反应并生成氧气(实验操作如图甲所示).
实验现象及结论:观察到
(2)实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气.(实验操作如图乙所示)其中A装置的作用是
实验现象及结论:用带火星的木条检验C中气体成分,结果带火星的木条复燃;证明过氧化钠与水蒸气发生反应并生成氧气.实验中这种验证氧气的方法是利用了氧气的
(3)实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.(实验操作如图丙所示)
实验操作:①检查装置的气密性,向装置中加入药品.②打开分液漏斗活塞,向A装置中缓慢加入稀盐酸.③一段时间后用带火星的木条在D内进行检验.实验时观察到A装置中有气泡冒出,固体逐渐减少;D中带火星的木条复燃。则A中发生反应的化学方程式为
实验结论:过氧化钠与二氧化碳发生反应并生成氧气.
【实验反思】①根据实验Ⅲ,过氧化钠和二氧化碳反应后,还会生成另一种物质,该物质属于
②某同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是
您最近半年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐3】化学兴趣小组同学在老师指导下进行了一系列有趣的实验探究:测定鸡蛋壳的主要成分碳酸钙的质量分数(假设杂质不溶于水,也不和盐酸反应)。实验方案如下:
【方案一】
将鸡蛋壳洗净、干燥并捣碎后,称取10.00g放在烧杯里,然后往烧杯中加入足量的稀盐酸,充分反应后,取反应剩余固体洗净干燥后称量为0.50g。
(1)将鸡蛋壳捣碎的目的是_______ ;
(2)稀盐酸发生的反应化学方程式为_______ ;
(3)该鸡蛋壳中碳酸钙的质量为_______ 。
【方案二】
将鸡蛋壳样品与足量稀盐酸反应,测定反应后生成CO2的体积,再将体积换算为质量,最后根据CO2的质量求出样品中碳酸钙的质量。图Ⅰ为鸡蛋壳样品与稀盐酸反应的装置,图Ⅱ为测量CO2体积的装置(省略相应固定装置)。
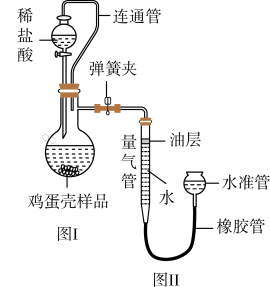

(4)图Ⅰ中连通管的作用_______ ;
(5)图Ⅱ中用油层的作用是_______ ;
(6)反应停止后,将水准管慢慢向下,可使反应前后油层上方气体压强和外界大气压相同,此时排出水的体积即为_______ 的体积。
【方案三】装置如图Ⅲ所示。
【查阅资料】1.浓硫酸可以吸收水蒸气;2.碱石灰可以吸收二氧化碳气体和水分。
【实验步骤】
①连接装置,检查装置气密性;
②称量ag鸡蛋壳样品装入A中;
③打开弹簧夹K,通入一段时间氮气;
④称量装置C的质量为bg;
⑤关闭弹簧夹K,滴加稀盐酸使其发生反应;
⑥打开弹簧夹K,通入一段时间氮气;
⑦再次称量C的质量为cg。
(7)D装置的作用是_________ 。
(8)B装置的作用_______ ,若没有B装置,则测定的碳酸钙的质量分数会______ (填“偏大”或“偏小”)。
(9)下列措施可以提高实验结果准确性的是______ 。
a.③⑥步骤中通入氮气时都要缓缓通入
b.⑤步骤中滴加稀盐酸时要快速滴入
c.⑤步骤中滴加稀盐酸时要至不产生气泡为止
d.通入的氮气换为空气成本更低效果更好
【数据处理】
(10)根据相关数据,列出该样品中碳酸钙质量分数的表达式为_______ 。
【方案一】
将鸡蛋壳洗净、干燥并捣碎后,称取10.00g放在烧杯里,然后往烧杯中加入足量的稀盐酸,充分反应后,取反应剩余固体洗净干燥后称量为0.50g。
(1)将鸡蛋壳捣碎的目的是
(2)稀盐酸发生的反应化学方程式为
(3)该鸡蛋壳中碳酸钙的质量为
【方案二】
将鸡蛋壳样品与足量稀盐酸反应,测定反应后生成CO2的体积,再将体积换算为质量,最后根据CO2的质量求出样品中碳酸钙的质量。图Ⅰ为鸡蛋壳样品与稀盐酸反应的装置,图Ⅱ为测量CO2体积的装置(省略相应固定装置)。


(4)图Ⅰ中连通管的作用
(5)图Ⅱ中用油层的作用是
(6)反应停止后,将水准管慢慢向下,可使反应前后油层上方气体压强和外界大气压相同,此时排出水的体积即为
【方案三】装置如图Ⅲ所示。
【查阅资料】1.浓硫酸可以吸收水蒸气;2.碱石灰可以吸收二氧化碳气体和水分。
【实验步骤】
①连接装置,检查装置气密性;
②称量ag鸡蛋壳样品装入A中;
③打开弹簧夹K,通入一段时间氮气;
④称量装置C的质量为bg;
⑤关闭弹簧夹K,滴加稀盐酸使其发生反应;
⑥打开弹簧夹K,通入一段时间氮气;
⑦再次称量C的质量为cg。
(7)D装置的作用是
(8)B装置的作用
(9)下列措施可以提高实验结果准确性的是
a.③⑥步骤中通入氮气时都要缓缓通入
b.⑤步骤中滴加稀盐酸时要快速滴入
c.⑤步骤中滴加稀盐酸时要至不产生气泡为止
d.通入的氮气换为空气成本更低效果更好
【数据处理】
(10)根据相关数据,列出该样品中碳酸钙质量分数的表达式为
您最近半年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】某化学兴趣小组的同学利用下图装置制取并收集一瓶二氧化碳气体,请和他们一起完成以下实验探究。
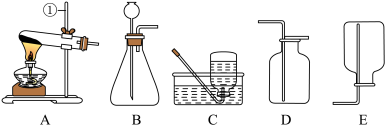
(1)写出标号①的仪器名称________ 。
(2)实验室制取一瓶二氧化碳气体,应选用的收集装置为________ (填序号),反应的化学方程式为____________________ 。
(3)化学兴趣小组的同学对反应后废液中溶质的成分进行进一步探究。
【提出问题】废液中的溶质有哪些物质?
【查阅资料】氯化钙溶液呈中性。
【猜想与假设】猜想①:废液中的溶质只有氯化钙;
猜想②:废液中的溶质是氯化钙和________ (填化学式)。
【设计并进行实验】Ⅰ. 为验证上面两种猜想哪种正确,甲小组的同学从下面A~E五种药品中选择合适的一种进行实验,证明了猜想②是正确的。他们选择的药品不可能是________ 。
A. 紫色石蕊试液 B. 无色酚酞试液 C. 锌粒 D. 氧化铁粉末 E. 氢氧化钠溶液
Ⅱ. 乙小组选用一种钠盐溶液进行实验,也证明了猜想②是正确的,请完成下面的实验报告。
【探究反思】:实验产生的污染深受人们重视,我们要利用恰当的方法对废液进行处理,实行无害化排放,从源头上消除对环境的污染。
(4)使用纯碱中常含有少量的氯化钠,现取某使用纯碱样品2.5g,加水溶解,配成溶液,向其中加入一定量CaCl2溶液恰好完全反应,同时产生了2g沉淀。试计算该食用纯碱中Na2CO3的质量分数_____________ (写出计算过程)。

(1)写出标号①的仪器名称
(2)实验室制取一瓶二氧化碳气体,应选用的收集装置为
(3)化学兴趣小组的同学对反应后废液中溶质的成分进行进一步探究。
【提出问题】废液中的溶质有哪些物质?
【查阅资料】氯化钙溶液呈中性。
【猜想与假设】猜想①:废液中的溶质只有氯化钙;
猜想②:废液中的溶质是氯化钙和
【设计并进行实验】Ⅰ. 为验证上面两种猜想哪种正确,甲小组的同学从下面A~E五种药品中选择合适的一种进行实验,证明了猜想②是正确的。他们选择的药品不可能是
A. 紫色石蕊试液 B. 无色酚酞试液 C. 锌粒 D. 氧化铁粉末 E. 氢氧化钠溶液
Ⅱ. 乙小组选用一种钠盐溶液进行实验,也证明了猜想②是正确的,请完成下面的实验报告。
| 实验操作 | 实验现象 | 实验结论 |
| 取少量反应后的废液于试管中,加入足量 | 猜想②正确 |
(4)使用纯碱中常含有少量的氯化钠,现取某使用纯碱样品2.5g,加水溶解,配成溶液,向其中加入一定量CaCl2溶液恰好完全反应,同时产生了2g沉淀。试计算该食用纯碱中Na2CO3的质量分数
您最近半年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】探究是学习化学的重要方法
Ι.探究水、石灰水、NaOH溶液对CO2的吸收。实验步骤如下:

步骤1:如图所示装置的气密性良好(图中a处连接气体压力传感器),甲、乙、丙三个烧瓶的容积均为250mL,分别收集满CO2,三个注射器内各装有85mL液体。
步骤2:三位同学同时迅速将注射器内液体全部注入各自烧瓶中,关闭活塞;一段时间后,同时振荡烧瓶。
步骤3:利用“数字化实验”测定烧瓶内的气压变化,得到如下图所示的烧瓶内压强与时间的关系曲线图,曲线1、2、3分别表示甲、乙、丙三个烧瓶内的气压变化。
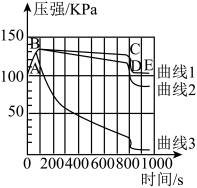
(1)实验过程中,观察到烧瓶乙中有白色沉淀生成。写出该反应的化学方程式:_____ 。
(2)导致AB段气压增大的主要原因是_____ 。
(3)曲线1中BC段气压逐渐变小的原因是_____ ,导致CD段气压快速变小的操作是_____ 。
(4)对比曲线1、2、3,能得出的结论是_____ (填序号)。
a.CO2能溶于水
b.CO2能与水发生反应
c.40%的NaOH溶液比饱和石灰水更适合吸收CO2
Ⅱ.探究能否用排水法收集CO2
(1)可行性分析:CO2气体生成和从水面逸出的速率_____ (填“大于”或“小于”、“等于”)其溶解和水反应的速率。可用排水法收集CO2。
(2)实验:用体积相同的2个集气瓶分别用排水法和排空气法各收集一瓶CO2,分别测定这两瓶CO2气体中氧气的体积分数,从而得到二氧化碳的体积分数。下图是用氧气测量仪分别测定的这两瓶CO2中O2的体积分数随时间的变化关系曲线(起始时氧气的体积分数都以21%计)。
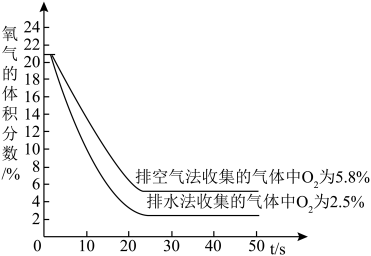
(3)结论:①两种方法收集的气体中二氧化碳体积分数较大的是_____ (填“排空气”或“排水”)法。
②排空气法收集的气体中二氧化碳体积分数是_____ 。
Ι.探究水、石灰水、NaOH溶液对CO2的吸收。实验步骤如下:

步骤1:如图所示装置的气密性良好(图中a处连接气体压力传感器),甲、乙、丙三个烧瓶的容积均为250mL,分别收集满CO2,三个注射器内各装有85mL液体。
步骤2:三位同学同时迅速将注射器内液体全部注入各自烧瓶中,关闭活塞;一段时间后,同时振荡烧瓶。
步骤3:利用“数字化实验”测定烧瓶内的气压变化,得到如下图所示的烧瓶内压强与时间的关系曲线图,曲线1、2、3分别表示甲、乙、丙三个烧瓶内的气压变化。

(1)实验过程中,观察到烧瓶乙中有白色沉淀生成。写出该反应的化学方程式:
(2)导致AB段气压增大的主要原因是
(3)曲线1中BC段气压逐渐变小的原因是
(4)对比曲线1、2、3,能得出的结论是
a.CO2能溶于水
b.CO2能与水发生反应
c.40%的NaOH溶液比饱和石灰水更适合吸收CO2
Ⅱ.探究能否用排水法收集CO2
(1)可行性分析:CO2气体生成和从水面逸出的速率
(2)实验:用体积相同的2个集气瓶分别用排水法和排空气法各收集一瓶CO2,分别测定这两瓶CO2气体中氧气的体积分数,从而得到二氧化碳的体积分数。下图是用氧气测量仪分别测定的这两瓶CO2中O2的体积分数随时间的变化关系曲线(起始时氧气的体积分数都以21%计)。

(3)结论:①两种方法收集的气体中二氧化碳体积分数较大的是
②排空气法收集的气体中二氧化碳体积分数是
您最近半年使用:0次
科学探究题
|
较难
(0.4)
真题
解题方法
【推荐3】某课外活动小组利用下列装置制取二氧化碳,并探究钠在二氧化碳中的燃烧产物。已知:Na2O和CaO相似,能与水反应。请回答下列问题:

(1)按图连接装置后,首先进行的操作是__________________ 。
(2)A装置用于制取CO2,用到的玻璃仪器有长颈漏斗、导管和_______ 。
(3)实验中下列操作的先后顺序是__________ 。
a.点燃酒精灯,加热硬质玻璃管中的钠
b.等燃烧终止并冷却后,停止通CO2
c.打开A装置中活塞,通入CO2
(4)D装置中观察到的现象有:钠在二氧化碳中燃烧,产生大量白烟和黑色物质。待钠充分燃烧,冷却,将管内生成的固态物质移出,加水溶解,过滤得黑色固体和澄清滤液。实验证明:D中排出的尾气能被NaOH溶液完全吸收。
①黑色固体在O2中灼烧,全部转化为气体,则黑色固体是______ 。
②对白色固体有以下猜想:
a.只有Na2O b.只有Na2CO3c.Na2O和Na2CO3的混合物
若猜想a成立,则Na与CO2反应的化学方程式是__________________ 。
若猜想c成立,请设计实验验证产物中存在Na2O:取滤液少许,________________________ 。
(5)反思拓展:你对二氧化碳灭火的范围有什么新的认识?_______________ 。

(1)按图连接装置后,首先进行的操作是
(2)A装置用于制取CO2,用到的玻璃仪器有长颈漏斗、导管和
(3)实验中下列操作的先后顺序是
a.点燃酒精灯,加热硬质玻璃管中的钠
b.等燃烧终止并冷却后,停止通CO2
c.打开A装置中活塞,通入CO2
(4)D装置中观察到的现象有:钠在二氧化碳中燃烧,产生大量白烟和黑色物质。待钠充分燃烧,冷却,将管内生成的固态物质移出,加水溶解,过滤得黑色固体和澄清滤液。实验证明:D中排出的尾气能被NaOH溶液完全吸收。
①黑色固体在O2中灼烧,全部转化为气体,则黑色固体是
②对白色固体有以下猜想:
a.只有Na2O b.只有Na2CO3c.Na2O和Na2CO3的混合物
若猜想a成立,则Na与CO2反应的化学方程式是
若猜想c成立,请设计实验验证产物中存在Na2O:取滤液少许,
(5)反思拓展:你对二氧化碳灭火的范围有什么新的认识?
您最近半年使用:0次
【推荐1】某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖。对于该溶液是否变质,同学们开始实验探究。
【猜想假设】
猜想(1):该溶液没有变质,为NaOH溶液。
猜想(2):该溶液全部变质,为Na2CO3溶液。
猜想(3):该溶液部分变质,为NaOH和Na2CO3的混合溶液。
【查阅资料】Na2CO3溶液呈碱性
【设计方案】请你完善下表几组同学探讨的设计方案
【探究实验】综合各小组的方案后,动手实验。
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存。
【拓展延伸】同学们设计了下列两套装置进行实验:
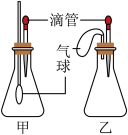
用胶头滴管吸取某种液体,锥形瓶中充入一种气体或放入一种固体物质,挤压胶头滴管。一段时间后,两装置中气球明显胀大。
(1)甲装置中可能发生反应的方程式是______________ 。
(2)若乙装置中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是______________ 。
【猜想假设】
猜想(1):该溶液没有变质,为NaOH溶液。
猜想(2):该溶液全部变质,为Na2CO3溶液。
猜想(3):该溶液部分变质,为NaOH和Na2CO3的混合溶液。
【查阅资料】Na2CO3溶液呈碱性
【设计方案】请你完善下表几组同学探讨的设计方案
| 实验操作 | 可能出现的现象与结论 | 同学评价 | |
| 第1组 |  | 若溶液变红,则猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是: |
| 第2组 | 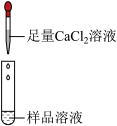 | 若产生白色沉淀,反应方程式是: | 第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立。 |
| 第3组 | 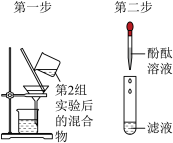 | 若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立。 | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是: |
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存。
【拓展延伸】同学们设计了下列两套装置进行实验:

用胶头滴管吸取某种液体,锥形瓶中充入一种气体或放入一种固体物质,挤压胶头滴管。一段时间后,两装置中气球明显胀大。
(1)甲装置中可能发生反应的方程式是
(2)若乙装置中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是
您最近半年使用:0次
【推荐2】化学兴趣小组的同学在探究氢氧化钙的化学性质时进行了如图实验:
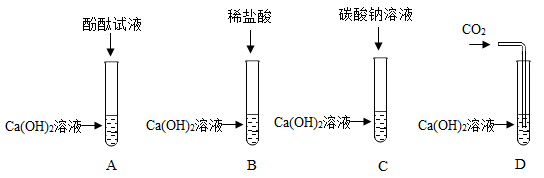
请回答下列问题:
(1)试管A中的现象是______ 。
(2)B试管没有明显的现象,可以加入______ 试液使得反应出现明显现象。
(3)实验D中发生反应的化学方程式为______ ,该反应______ (填“是”或“不是”)复分解反应。
(4)实验结束后,小组同学做了两个探究实验:
实验一:充分反应后,小组同学对C试管中上层清液的溶质成分产生疑问,作出猜想:
猜想一:只含有NaOH
猜想二:含有 NaOH、Na2CO3
猜想三:含有NaOH、Ca(OH)2
同学们取少量C试管的清液分别置于甲、乙两个试管中,进行探究:
实验二:小组同学将A、B、C、D四个试管中的物质倒入一个洁净的大烧杯中,充分反应后静置,发现烧杯中只得到无色澄清溶液,则烧杯中废液的溶质(指示剂除外)一定有______ (写出化学式)。

请回答下列问题:
(1)试管A中的现象是
(2)B试管没有明显的现象,可以加入
(3)实验D中发生反应的化学方程式为
(4)实验结束后,小组同学做了两个探究实验:
实验一:充分反应后,小组同学对C试管中上层清液的溶质成分产生疑问,作出猜想:
猜想一:只含有NaOH
猜想二:含有 NaOH、Na2CO3
猜想三:含有NaOH、Ca(OH)2
同学们取少量C试管的清液分别置于甲、乙两个试管中,进行探究:
| 实验操作 | 实验现象 | 结论 |
| 在试管甲中滴加碳酸钠溶液 | 不产生白色沉淀 | 猜想 |
| 在试管乙中滴加足量稀盐酸 | 开始无明显现象,一段时间后 | 猜想二正确 |
您最近半年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】某白色固体可能由氯化钡、氢氧化钠、碳酸钠、硫酸钠、四氧化三铁中的一种或几种物质组成。同学们为了确定该白色固体的成分,进行了如下实验探究:
【资料卡片】BaCl2溶液显中性。
【初步结论】
甲同学根据固体的描述确定样品中肯定没有______________
(填化学式)。
【初步探究】
同学们设计的实验过程及现象如图所示。

【交流讨论】
同学们认为:无色溶液 M 中一定含有________ (填化学式),无色溶液 M 加入酚酞试液后变红色,说明溶液 M 显碱性,需对溶液 M 继续探究。
【提出问题】
使溶液 M 显碱性的物质是什么?
【猜想与假设】
猜想一:是氢氧化钠;猜想二:是碳酸钠;猜想三:是氢氧化钠和碳酸钠。
【探究与结论】
(1)乙同学取无色溶液 M 于试管中,加入过量的氯化钡溶液,振荡,静置,观察到____________ ,证明无色溶液 M 中含有碳酸钠。
(2)丙同学为进一步证明无色溶液 M 中的成分,进行的实验是:取乙同学实验所得上层清液少许于试管中,____________ (请你将丙同学的实验及实验现象补充完整),证明猜想三成立。
综合分析,乙同学加入过量氯化钡溶液的作用:____________ 。
【实验结论】
原白色固体中一定有的物质是____________ (填化学式)。
【资料卡片】BaCl2溶液显中性。
【初步结论】
甲同学根据固体的描述确定样品中肯定没有
(填化学式)。
【初步探究】
同学们设计的实验过程及现象如图所示。

【交流讨论】
同学们认为:无色溶液 M 中一定含有
【提出问题】
使溶液 M 显碱性的物质是什么?
【猜想与假设】
猜想一:是氢氧化钠;猜想二:是碳酸钠;猜想三:是氢氧化钠和碳酸钠。
【探究与结论】
(1)乙同学取无色溶液 M 于试管中,加入过量的氯化钡溶液,振荡,静置,观察到
(2)丙同学为进一步证明无色溶液 M 中的成分,进行的实验是:取乙同学实验所得上层清液少许于试管中,
综合分析,乙同学加入过量氯化钡溶液的作用:
【实验结论】
原白色固体中一定有的物质是
您最近半年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐1】将打磨光亮的镁条与一定量稀盐酸反应时发现“意外”:产生大量气泡后还出现白色固体。
【提出问题】白色固体是什么?
【查阅资料】在MgCl2溶液中,常温下反应: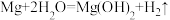
【猜想假设】
猜想①:反应后有镁剩余
猜想②:生成的MgCl2过多而析出
猜想③:生成Mg(OH)2沉淀
【实验探究】将上述试管中反应后的物质过滤、洗涤、烘干,得到0.459g白色固体,进行如下实验:
【实验分析】
(1)生成白色沉淀A得化学方程式为_______ 。
(2)结合XRD图谱分析得知,白色固体的化学式可用MgX(OH)Y△Z表示,其中“△”表示的元素符号是___ 。
(3)经计算分析X:Y:Z=_______ 。
(4)请写出得到白色固体和H2的化学方程式(已知两者化学计量数之比为1:2):_____ 。
【提出问题】白色固体是什么?
【查阅资料】在MgCl2溶液中,常温下反应:
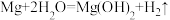
【猜想假设】
猜想①:反应后有镁剩余
猜想②:生成的MgCl2过多而析出
猜想③:生成Mg(OH)2沉淀
【实验探究】将上述试管中反应后的物质过滤、洗涤、烘干,得到0.459g白色固体,进行如下实验:
| 猜想 | 操作 | 现象 | 结论 |
| ① | 取0.153g固体,滴加足量稀盐酸 | 不成立 | |
| ② | 另取0.153g固体,加入适量 | 固体仍为0.153g | 不成立 |
| ③ | 再取0.153g固体,先滴入足量稀硝酸使固体完全溶解后,再滴加足量NaOH溶液,过滤、洗涤、烘干后称重 | 得到0.116g白色沉淀A | 不成立 |
| 继续向滤液中滴加足量硝酸银溶液,过滤、洗涤、烘干后称重 | 得到0.287g白色沉淀B |
(1)生成白色沉淀A得化学方程式为
(2)结合XRD图谱分析得知,白色固体的化学式可用MgX(OH)Y△Z表示,其中“△”表示的元素符号是
(3)经计算分析X:Y:Z=
(4)请写出得到白色固体和H2的化学方程式(已知两者化学计量数之比为1:2):
您最近半年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】小华到厨房帮妈妈拿小苏打和面烙火烧,打开调料盒一看,咦,三种白色粉末,哪种是呢?妈妈告诉他,三种白色粉末分别是小苏打、苏打、食盐。于是小华利用化学知识、求助同学、上网查阅资料等方法成功找出小苏打。
【查阅资料】获得如下信息:
(1)氯化钡溶液呈中性,与碳酸氢钠溶液不发生反应
(2)小苏打受热易分解,生成苏打、水和一种无色气体
(3)碳酸氢钠溶液呈碱性,与澄清石灰水反应生成白色沉淀
(4)碳酸钠受热不分解,与少量稀盐酸反应的化学方程式为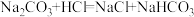 ;与过量稀盐酸反应的方程式为
;与过量稀盐酸反应的方程式为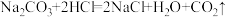 。
。
【实验探究】
(1)小华设计实验如下:
(2)小童告诉小华可以利用如图装置,将A、B、C样品分别加热进行实验,也能找出小苏打。当看到澄清石灰水变浑浊,说明样品是碳酸氢钠;试管中的实验原理是______ (用化学方程式表示)。
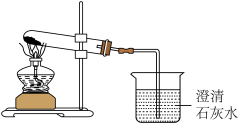
(3)小辰认为只用一种试剂不需加热也能找出小苏打,该试剂是______ ,请写出小辰的实验方法(实验步骤、现象与结论)______ 。
【实验反思】类比资料信息,碳酸氢钠与氢氧化钠反应生成另外两种化合物,反应的化学方程式为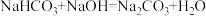 。
。
【查阅资料】获得如下信息:
(1)氯化钡溶液呈中性,与碳酸氢钠溶液不发生反应
(2)小苏打受热易分解,生成苏打、水和一种无色气体
(3)碳酸氢钠溶液呈碱性,与澄清石灰水反应生成白色沉淀
(4)碳酸钠受热不分解,与少量稀盐酸反应的化学方程式为
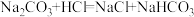 ;与过量稀盐酸反应的方程式为
;与过量稀盐酸反应的方程式为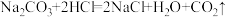 。
。 【实验探究】
(1)小华设计实验如下:
| 实验步骤 | 实验现象 | 实验结论 |
| 1.将样品编号A、B、C,分别取少量样品于烧杯,加适量水充分溶解,向烧杯中各滴加2-3滴酚酞溶液。 | C样品是氯化钠 | |
| 2.另取A、B样品少量于烧杯,加适量水充分溶解,滴入适量 | A中无现象,B中产生白色沉淀 | A样品是 |

(3)小辰认为只用一种试剂不需加热也能找出小苏打,该试剂是
【实验反思】类比资料信息,碳酸氢钠与氢氧化钠反应生成另外两种化合物,反应的化学方程式为
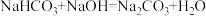 。
。
您最近半年使用:0次
科学探究题
|
较难
(0.4)
【推荐3】在高温下,铁与水蒸气能发生反应生成一种常见的铁的氧化物和一种气体。某兴趣小组请你参与研究:铁与水蒸气反应一段时间后剩余固体物质的成分、性质及再利用。
实验装置如图所示(夹持仪器略)
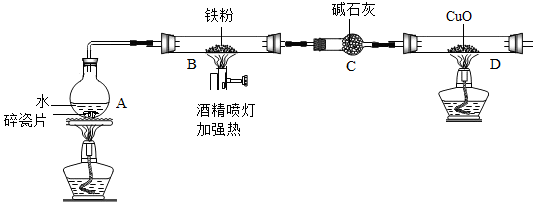
(1)【推断】观察到D中黑色固体变红,则B中生成的气体是_____________ 。
(2)探究B装置中剩余固体成分是什么?
【查阅资料】
(1).碎瓷片能防爆沸;碱石灰是氧化钙和氢氧化钠的混合物
(2).铁的氧化物中,只有Fe2O3是红棕色,其余均为黑色,只有Fe3O4能被磁铁吸引。
【初步探究】
B装置中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】
猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是_____________ 。
【实验探究】
【实验结论】铁与水蒸气反应的化学方程式为_____________ 。
(3)【成分再利用】若将B装置中剩余的黑色固体a g,经过一系列转化,全部变为红棕色固体Fe2O3(假设转化过程中铁元素无损耗),增加的质量为x,则x的取值范围为_____________ 。
实验装置如图所示(夹持仪器略)

(1)【推断】观察到D中黑色固体变红,则B中生成的气体是
(2)探究B装置中剩余固体成分是什么?
【查阅资料】
(1).碎瓷片能防爆沸;碱石灰是氧化钙和氢氧化钠的混合物
(2).铁的氧化物中,只有Fe2O3是红棕色,其余均为黑色,只有Fe3O4能被磁铁吸引。
【初步探究】
B装置中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】
猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是
【实验探究】
| 实验操作 | 实验现象及结论 |
| 取少量黑色固体于试管中,加入足量的稀盐酸(或稀硫酸) | 若固体全部溶解,没有气泡冒出,剩余固体是Fe3O4,若固体全部溶解,有气泡冒出,剩余固体是Fe和Fe3O4(与实验操作一致) |
【实验结论】铁与水蒸气反应的化学方程式为
(3)【成分再利用】若将B装置中剩余的黑色固体a g,经过一系列转化,全部变为红棕色固体Fe2O3(假设转化过程中铁元素无损耗),增加的质量为x,则x的取值范围为
您最近半年使用:0次



