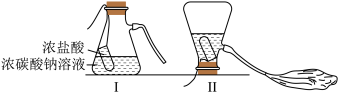
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究。
【猜想与假设】
猜想1:废液中的溶质可能是NaCl、Na2CO3和HCl。
猜想2:废液中的溶质只有NaCl。
猜想3:废液中的溶质是NaCl和HCl。
猜想4:废液中的溶质是__________________ 。
【讨论与交流】
小明认为猜想1无需验证就知道是错误的。他的理由是_____________________________ 。
【实验与结论】
(1)为验证猜想2,小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解。于是小强认为猜想2正确。小强的实验______ (填“能”或“不能”)验证猜想2的正确性,原因是_____________________ 。
(2)小丽为验证猜想3,选锌粒做试剂。若猜想3是正确的,验证时反应的化学方程式为_____________________________________________ 。
(3)若验证猜想4是否正确,下列试剂中可选用的有____________ (填序号)。
①氢氧化钠溶液 ②氯化钙溶液 ③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行_______________ 操作即可从废液中得到NaCl固体。此方法的缺点是_______________________________________________ 。
【猜想与假设】
猜想1:废液中的溶质可能是NaCl、Na2CO3和HCl。
猜想2:废液中的溶质只有NaCl。
猜想3:废液中的溶质是NaCl和HCl。
猜想4:废液中的溶质是
【讨论与交流】
小明认为猜想1无需验证就知道是错误的。他的理由是
【实验与结论】
(1)为验证猜想2,小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解。于是小强认为猜想2正确。小强的实验
(2)小丽为验证猜想3,选锌粒做试剂。若猜想3是正确的,验证时反应的化学方程式为
(3)若验证猜想4是否正确,下列试剂中可选用的有
①氢氧化钠溶液 ②氯化钙溶液 ③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行
2012·黑龙江哈尔滨·中考模拟 查看更多[2]
更新时间:2018-06-06 11:38:17
|
相似题推荐
科学探究题
|
较难
(0.4)
【推荐1】铁是日常生活中最常见的金属,据资料介绍:氧化铁在隔绝空气的条件下高温加热能生成黑色固体和一种气体。小明在实验室进行了下列实验:
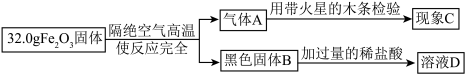
根据以上图示回答问题:
(1)气体A的化学式为_____ ,现象C是_____ 。
(2)对黑色固体B的探究:
【实验现象】在向黑色固体B中加过量稀盐酸的实验过程中,没有观察到有气泡产生。由此可知黑色固体B中没有铁,判断依据是_____ (用化学方程式表示)
【查阅资料】①氧化亚铁和四氧化三铁都是黑色固体②它们都可以和稀盐酸或稀硫酸反应,其中四氧化三铁与盐酸反应的化学方程式为:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O。
【猜想】黑色固体B是Ⅰ、FeO Ⅱ、Fe3O4 Ⅲ、_____ 。
【实验分析】
①小亮认为,如果猜想Ⅱ 成立,则溶液D中的溶质为_____ ;
②小意认为,要确定黑色固体B的组成,还应该继续称量B的质量。若实验称得黑色固体B的质量为30.4g,则B中铁、氧元素的质量比为_____ ,猜想_____ 成立。则氧化铁分解的化学方程式为_____

根据以上图示回答问题:
(1)气体A的化学式为
(2)对黑色固体B的探究:
【实验现象】在向黑色固体B中加过量稀盐酸的实验过程中,没有观察到有气泡产生。由此可知黑色固体B中没有铁,判断依据是
【查阅资料】①氧化亚铁和四氧化三铁都是黑色固体②它们都可以和稀盐酸或稀硫酸反应,其中四氧化三铁与盐酸反应的化学方程式为:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O。
【猜想】黑色固体B是Ⅰ、FeO Ⅱ、Fe3O4 Ⅲ、
【实验分析】
①小亮认为,如果猜想Ⅱ 成立,则溶液D中的溶质为
②小意认为,要确定黑色固体B的组成,还应该继续称量B的质量。若实验称得黑色固体B的质量为30.4g,则B中铁、氧元素的质量比为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】甲、乙两位同学分别用氢氧化钠溶液和稀硫酸做了中和反应实验。
甲同学设计的实验方案:向装有氢氧化钠溶液的试管内滴入2滴的酚酞试液,再逐滴滴加稀硫酸,边滴边振荡。
上述方案实施时,能说明两者恰好完成反应的现象是___________ 。涉及的化学反应方程式为___________ 。
乙同学在做“硫酸中和氢氧化钠溶液”的实验时,滴加稀硫酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。对反应后溶液中溶质成分进行了探究。
【提出问题】溶液中的溶质是什么物质?
【作出猜想】猜想一:只有Na2SO4猜想二:Na2SO4和___________ 猜想三:Na2SO4和NaOH
【查阅资料】
①Na2SO4溶液显中性
②A1与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气。
【实验验证】
结论资料和信息,你___________ (填“同意”、“不同意”)乙同学的结论。理由是___________ 。
如果乙同学的猜想二是正确的。请你再设计实验加以证明。
【实验反思】为了验证猜想二成立,下列试剂还可以选择的是___________ 。
A 紫色石蕊 B Cu C Cu (OH)2 D Ba(NO3)2溶液 E Na2CO3溶液
甲同学设计的实验方案:向装有氢氧化钠溶液的试管内滴入2滴的酚酞试液,再逐滴滴加稀硫酸,边滴边振荡。
上述方案实施时,能说明两者恰好完成反应的现象是
乙同学在做“硫酸中和氢氧化钠溶液”的实验时,滴加稀硫酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。对反应后溶液中溶质成分进行了探究。
【提出问题】溶液中的溶质是什么物质?
【作出猜想】猜想一:只有Na2SO4猜想二:Na2SO4和
【查阅资料】
①Na2SO4溶液显中性
②A1与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气。
【实验验证】
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,将打磨的铝片浸入溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色。 | 猜想二成立 |
如果乙同学的猜想二是正确的。请你再设计实验加以证明。
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入少量CuO | 猜想二成立 |
A 紫色石蕊 B Cu C Cu (OH)2 D Ba(NO3)2溶液 E Na2CO3溶液
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】一种自加热食品包装中加热包的成分有:生石灰、活性炭、铝粉、碳酸钠、氯化钙、硫酸镁。使用时需向加热包加水,课堂上老师取适量加热包中的固体样品进行如图实验:
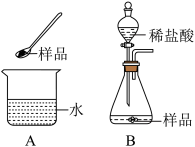
(1)实验A中,将样品加入水里,触摸烧杯外壁发烫,其原因是___________ 。(用化学方程式表示)
(2)实验B中,将一定量稀盐酸加入锥形瓶中,剧烈反应,生成大量气体,可能产生气体反应的化学方程式为___________ 、_________ 。学习小组同学对气体成分和锥形瓶内溶液进行探究。
Ⅰ.对气体成分进行探究。
【作出假设】
假设一:只有H2,假设二:只有CO2,假设三:H2和CO2。
【实验验证】小明同学设计如图实验,对气体成分进行探究。

①当气体通过甲时,现象___________ ,证明假设一不成立。
②丁装置中出现___________ 的现象时,证明假设三成立,丁中发生反应的化学方程式为___________ ,在反应中,发生氧化反应的是___________ 。
③乙装置的作用是___________ 。
Ⅱ、对锥形瓶内的溶液进行探究。
实验后,小萍同学取少量锥形瓶内的溶液于试管中,向其中滴加NaOH溶液,开始一段时间无沉淀生成,其原因是锥形瓶内的溶液中存在___________ ,生成沉淀的化学方程式为___________ 。
【总结反思】
通过以上探究,小林同学做了如下的反思归纳,你认为其中不正确的是___________ 。(填字母)
A加热包应密封防潮保存
B向用过的加热包内的固体中,加入过量稀盐酸后过滤,可以回收活性炭
C能与水混合放出热量的物质均可用作加热包中的发热材料

(1)实验A中,将样品加入水里,触摸烧杯外壁发烫,其原因是
(2)实验B中,将一定量稀盐酸加入锥形瓶中,剧烈反应,生成大量气体,可能产生气体反应的化学方程式为
Ⅰ.对气体成分进行探究。
【作出假设】
假设一:只有H2,假设二:只有CO2,假设三:H2和CO2。
【实验验证】小明同学设计如图实验,对气体成分进行探究。

①当气体通过甲时,现象
②丁装置中出现
③乙装置的作用是
Ⅱ、对锥形瓶内的溶液进行探究。
实验后,小萍同学取少量锥形瓶内的溶液于试管中,向其中滴加NaOH溶液,开始一段时间无沉淀生成,其原因是锥形瓶内的溶液中存在
【总结反思】
通过以上探究,小林同学做了如下的反思归纳,你认为其中不正确的是
A加热包应密封防潮保存
B向用过的加热包内的固体中,加入过量稀盐酸后过滤,可以回收活性炭
C能与水混合放出热量的物质均可用作加热包中的发热材料
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐1】实验室有一瓶失去标签的溶液,知道只含有一种阳离子钾离子,为了弄清其到底含有几种溶质(都是初中常见的物质),四九芳华小组做了如下实验:(不考虑微溶和碳酸氢根)

根据上述实验过程:小四同学根据滤渣处产生的_____________ 现象,从而确定了一定含有的两种溶质为___________ ,写出此过程反应的化学方程式:________ 。
还有那些溶质呢?小九同学继续探究如下图:

得出结论:该溶液一定含有氢氧化钾,请你对其结论进行评价_________ ;四九芳华小组经过讨论,觉得上述过程所加的试剂有一处不够明确和准确,从而对后续其他溶质的确定带来了影响,决定对一种试剂稍作调整,其他不变,调整为__________________ ,然后重新取滤液加入________ ,立即向所得溶液中加入__________ ,从而可推出瓶中溶液的溶质最多有__________ 种。

根据上述实验过程:小四同学根据滤渣处产生的
还有那些溶质呢?小九同学继续探究如下图:

得出结论:该溶液一定含有氢氧化钾,请你对其结论进行评价
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】请你根据如图回答有关问题:

(1)实验室欲制备并收集二氧化碳,需在图一中选用A、B与___________ (填序号)组合,该反应的化学方程式为_________________ 。
(2)图二是两套干燥气体装置,可用于干燥二氧化碳的是_______________ (填“甲”或“乙”),为探究CO2与NaOH溶液发生的反应,某兴趣小组尝试用不同的方式进行实验。
[查阅资料]
I.20°C时,几种物质在水中的溶解度见下表:
II.本实验条件下,Na2CO3溶液和NaHCO3溶液的pH分别约为11.0和8.5。
[实验探究]
(3)实验一:小雨取一充满CO2 的矿泉水瓶,加入一定量的水,立即拧紧瓶盖,振荡,发现瓶子变瘪,小雨另取一相同的充满 CO2的矿泉水瓶,向其中加入与水等体积的NaOH溶液,立即拧紧瓶盖,振荡,得到溶液X,此时观察到的现象是_________________ 。
(4)实验二:为检验CO2与NaOH溶液反应的产物,小亮取实验一所得溶液 X少许,向其中滴加BaCl2溶液,有白色沉淀产生,该反应的化学方程式为_________________ 。实验中不宜将BaCl2溶液换成CaCl2溶液的原因是________________ 。
(5)实验三:小华取实验一所得溶液X少许,向其中加入过量的BaCl2溶液,振荡,静置,取上层清液,滴入1滴酚酞试液,发现溶液呈_______________ 色,证明溶液X中有NaOH剩余。实验中,小华没有直接向少量溶液X中滴入酚酞试液,理由是_________________ 。
(6)实验四:兴趣小组将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测定反应过程中溶液的pH和温度变化,结果如图1、图2所示。

图2中,DE段温度变化的原因是________________ 。
[反思感悟]
(7)实验从CO2减少、NaOH减少,Na2CO3生成等物质的变化,以及______________ 转化等视角多维度探究CO2与NaOH发生了反应,对于现象不明显的化学反应,可以通过现代技术手段进行数据测定,实现反应过程的“可视化”。

(1)实验室欲制备并收集二氧化碳,需在图一中选用A、B与
(2)图二是两套干燥气体装置,可用于干燥二氧化碳的是
[查阅资料]
I.20°C时,几种物质在水中的溶解度见下表:
| 物质 | Na2CO3 | NaHCO3 | Ca(OH)2 | Ba(OH)2 |
| 溶解度/g | 21.5 | 9.6 | 0.165 | 3.89 |
[实验探究]
(3)实验一:小雨取一充满CO2 的矿泉水瓶,加入一定量的水,立即拧紧瓶盖,振荡,发现瓶子变瘪,小雨另取一相同的充满 CO2的矿泉水瓶,向其中加入与水等体积的NaOH溶液,立即拧紧瓶盖,振荡,得到溶液X,此时观察到的现象是
(4)实验二:为检验CO2与NaOH溶液反应的产物,小亮取实验一所得溶液 X少许,向其中滴加BaCl2溶液,有白色沉淀产生,该反应的化学方程式为
(5)实验三:小华取实验一所得溶液X少许,向其中加入过量的BaCl2溶液,振荡,静置,取上层清液,滴入1滴酚酞试液,发现溶液呈
(6)实验四:兴趣小组将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测定反应过程中溶液的pH和温度变化,结果如图1、图2所示。

图2中,DE段温度变化的原因是
[反思感悟]
(7)实验从CO2减少、NaOH减少,Na2CO3生成等物质的变化,以及
您最近一年使用:0次
科学探究题
|
较难
(0.4)
真题
解题方法
【推荐3】某化学活动小组在一次实验中进行了如图所示实验:
此时观察到的实验现象是__________ 。
实验后,小组同学充分振荡U形玻璃管,将U形玻璃管内的物质过滤后,对滤液成分产生了浓厚的兴趣,进行了进一步的探究活动。

【提出问题】滤液中除Na+外,还含有什么离子?
【猜想与假设】A同学:含有OH-、Cl-、
B同学:含有OH-、Cl-、Ba2+
C同学:含有________ (填离子符号)
【实验探究】B同学为了验证自己的猜想,取滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象。由此B同学得出结论:自己的猜想不成立,A同学的猜想成立。
【评价与交流】请你评价B同学的结论:__________ 。同学们经过讨论后一致认为:B同学在验证自己的猜想时,若将所加试剂调换成足量的另一种试剂________ (填化学式),既能验证自己的猜想.也能确定滤液中的离子成分。
C同学取该试剂进行实验,最终确定了滤渡中的离子成分。
【归纳与总结】通过上述实验我们能够总结出:在确定化学反应后所得溶液中的离子成分时,一般应加入__________ ,验证_________ 就可以确定溶液中的离子成分。
此时观察到的实验现象是
实验后,小组同学充分振荡U形玻璃管,将U形玻璃管内的物质过滤后,对滤液成分产生了浓厚的兴趣,进行了进一步的探究活动。

【提出问题】滤液中除Na+外,还含有什么离子?
【猜想与假设】A同学:含有OH-、Cl-、

B同学:含有OH-、Cl-、Ba2+
C同学:含有
【实验探究】B同学为了验证自己的猜想,取滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象。由此B同学得出结论:自己的猜想不成立,A同学的猜想成立。
【评价与交流】请你评价B同学的结论:
C同学取该试剂进行实验,最终确定了滤渡中的离子成分。
【归纳与总结】通过上述实验我们能够总结出:在确定化学反应后所得溶液中的离子成分时,一般应加入
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】在探究酸、碱、盐性质活动中,小揭同学向NaHCO3溶液中加入NaOH溶液,未观察到明显现象,即认为两者没有发生化学反应,化学学霸小阳同学却不同意此观点。
【提出问题】在溶液中,NaHCO3和NaOH不发生反应是真的吗?
【猜想假设】小阳的猜想:NaHCO3和NaOH在溶液中会发生反应;小空的猜想:NaHCO3和NaOH在溶液中不会发生反应。
(1)小港认同小空的猜想,也同意小揭的观点,他们共同的依据是NaHCO3和NaOH都含有相同阳离子,无法交换成分,不满足______ 进行的条件。
(下面是小阳同学带领其他同学通过查阅资料,设计实验来验证自己的猜想的过程)
【查阅资料】
可溶于水的酸、碱、盐在水中能解离出对应的阳离子和阴离子;
部分碱、盐的溶解性表(室温)
【进行实验】
【解释与结论】
(2)实验②中实验现象“?”是______ ,因为Na+、 、Ca2+、Cl-四种离子能共存于溶液中。
、Ca2+、Cl-四种离子能共存于溶液中。
(3)分析实验结果,获得以下结论:
a、实验③中生成的沉淀为______ (填化学式);
b、小阳的猜想成立,反应方程式为:______ 。
【总结拓展】
(4)两种溶液混合,未能观察到明显现象______ 发生化学反应(填“一定没有”或“不一定没有”)。
(5)很多不能共存离子对都是阴阳离子不共存,如:H++OH-→______ (请补填符号,下同),Ag++Cl-→AgCl↓,而该实验却出现一个“怪胎”,即阴阴不共存: +OH﹣→
+OH﹣→______ ,让人大开眼界。
【提出问题】在溶液中,NaHCO3和NaOH不发生反应是真的吗?
【猜想假设】小阳的猜想:NaHCO3和NaOH在溶液中会发生反应;小空的猜想:NaHCO3和NaOH在溶液中不会发生反应。
(1)小港认同小空的猜想,也同意小揭的观点,他们共同的依据是NaHCO3和NaOH都含有相同阳离子,无法交换成分,不满足
(下面是小阳同学带领其他同学通过查阅资料,设计实验来验证自己的猜想的过程)
【查阅资料】
可溶于水的酸、碱、盐在水中能解离出对应的阳离子和阴离子;
部分碱、盐的溶解性表(室温)
| OH- | Cl﹣ |  |  | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 溶 | 溶 | 不 | 溶 |
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少许NaHCO3溶液于试管中,滴入NaOH溶液 | 无明显现象 |
| ② | 取少许NaHCO3溶液于试管中,滴入CaCl2溶液 | ? |
| ③ | 将实验①、②两支试管中的溶液混合在一起 | 产生白色沉淀 |
【解释与结论】
(2)实验②中实验现象“?”是
 、Ca2+、Cl-四种离子能共存于溶液中。
、Ca2+、Cl-四种离子能共存于溶液中。(3)分析实验结果,获得以下结论:
a、实验③中生成的沉淀为
b、小阳的猜想成立,反应方程式为:
【总结拓展】
(4)两种溶液混合,未能观察到明显现象
(5)很多不能共存离子对都是阴阳离子不共存,如:H++OH-→
 +OH﹣→
+OH﹣→
您最近一年使用:0次
【推荐2】化学兴趣小组的同学为了探究酸碱盐的性质,做了如下图所示的实验。

(1)实验一中观察到的现象为____ ,该反应的化学方程式为____ 。
(2)实验二中没有观察到明显现象,据此____ (填“能”或“不能”)证明硫酸和氢氧化钠发生了化学反应。
实验结束后,小组同学对实验二溶液成分展开了探究。
【提出问题】实验二溶液中溶质的成分是什么?
【猜想假设】
(3)猜想一:CuSO4、Na2SO4、H2SO4
猜想二:CuSO4、Na2SO4、NaOH
猜想三:____ 。
以上猜想中,直接可以排除的是____ ,理由是____ 。
【实验设计】
(4)若要证明猜想一成立,下列试剂中不能达到实验目的的是 。

(1)实验一中观察到的现象为
(2)实验二中没有观察到明显现象,据此
实验结束后,小组同学对实验二溶液成分展开了探究。
【提出问题】实验二溶液中溶质的成分是什么?
【猜想假设】
(3)猜想一:CuSO4、Na2SO4、H2SO4
猜想二:CuSO4、Na2SO4、NaOH
猜想三:
以上猜想中,直接可以排除的是
【实验设计】
(4)若要证明猜想一成立,下列试剂中不能达到实验目的的是 。
| A.锌粒 | B.氯化钡溶液 | C.酚酞溶液 | D.氢氧化镁 |
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐3】有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成。为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性。他们经过思考设计并进行了以下实验:

请分析实验过程,回答下列问题:
(1)白色粉末中一定不含____________ ,可能含有 ____________ 。
(2)生成白色沉淀的化学方程式为________________________________________________ 。
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
[提出问题]无色滤液中呈碱性的物质是什么?
[做出猜想]猜想Ⅰ:Na2CO3;猜想Ⅱ:①____________ ;猜想Ⅲ:Na2CO3和NaOH。
[进行实验]
[得出结论]白色粉末的成分是⑥ ____________ 。

请分析实验过程,回答下列问题:
(1)白色粉末中一定不含
(2)生成白色沉淀的化学方程式为
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
[提出问题]无色滤液中呈碱性的物质是什么?
[做出猜想]猜想Ⅰ:Na2CO3;猜想Ⅱ:①
[进行实验]
| 实验步骤 | 实验现象 | 结论 |
| 1.取少许该溶液于试管中,滴入② | ③ | 猜想三正确 |
| 2.静置上述溶液,取上层清液少许于另一支试管中,滴入几滴④ | ⑤ |
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究。

【提出问题】
废液中所含溶质是什么物质?
【猜想与假设】
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl。
猜想(二):废液中的溶质只有NaCl。
猜想(三):废液中的溶质是NaCl和HCl。
猜想(四):废液中的溶质是_________ 。
【讨论与交流】
小明认为猜想(一)无需验证就知道是错误的。他的理由是_________ 。
【实验与结论】
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解。于是小强认为猜想(二)正确。小强的实验________ (填“能”或“不能”)验证猜想(二)的正确性,原因是 _______ 。
(2)小丽为验证猜想(三),选用大理石做试剂。若猜想(三)是正确的,验证时反应的化学方程式为________ 。
(3)若验证猜想(四)是否正确,下列试剂中可选用的有_______ (填序号)。
①氢氧化钠溶液 ②氯化钙溶液 ③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行_________ 操作即可从废液中得到NaCl固体。此方法的缺点是 ________ 。

【提出问题】
废液中所含溶质是什么物质?
【猜想与假设】
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl。
猜想(二):废液中的溶质只有NaCl。
猜想(三):废液中的溶质是NaCl和HCl。
猜想(四):废液中的溶质是
【讨论与交流】
小明认为猜想(一)无需验证就知道是错误的。他的理由是
【实验与结论】
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解。于是小强认为猜想(二)正确。小强的实验
(2)小丽为验证猜想(三),选用大理石做试剂。若猜想(三)是正确的,验证时反应的化学方程式为
(3)若验证猜想(四)是否正确,下列试剂中可选用的有
①氢氧化钠溶液 ②氯化钙溶液 ③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】某班同学用氢氧化钠溶液和稀盐酸进行中和反应实验:
(1)甲同学在烧杯中加入约5 mL氢氧化钠溶液,滴入几滴无色_______ 溶液,此时溶液呈红色,接着用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液变为无色,于是他得出两者恰好中和的结论,反应的化学方程式为______________________________ 。
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究。
【实验探究】反应后溶液中的溶质是什么?
猜想一:只有NaCl 猜想二:_____________ 猜想三:NaCl和NaOH
以上猜想中,你觉得不合理的是________ 。
为了验证另外两种猜想,乙同学设计如下实验方案:
【反思交流】实验结束后,废液处理的方法是_____________ 。
(1)甲同学在烧杯中加入约5 mL氢氧化钠溶液,滴入几滴无色
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究。
【实验探究】反应后溶液中的溶质是什么?
猜想一:只有NaCl 猜想二:
以上猜想中,你觉得不合理的是
为了验证另外两种猜想,乙同学设计如下实验方案:
| 实验操作 | 实验现象 | 实验结论 |
| 取水量反应后的溶液于试管中,滴入Na2CO3溶液 | 猜想二成立 |
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】瑶瑶同学在实验室发现有一瓶没有标签的白色粉末,可能含有NaCl 、Na2CO3、CaCl2和无水CuSO4中的一种或几种,为确定白色粉末的成分,取该白色粉末进行以下实验:
【提出问题】这包白色粉末的成分是什么?
【实验探究1】瑶瑶同学取白色粉末少许于试管中,向其中加入足量的蒸馏水充分溶解后,得到无色透明溶液,瑶瑶同学所得能出的结论是__________ ;
【实验探究2】瑶瑶同学取上述所得无色透明溶液于另一试管中,向其中加入足量的稀盐酸,观察到__________ 的现象,得出结论,白色粉末中一定含有Na2CO3,推出一定不含CaCl2,请写出上述反应的化学方程式是__________ .
【实验探究3】为了验证氯化钠是否存在,瑶瑶同学做了如下实验:取原粉末少许于试管中,加足量的蒸馏水充分溶解后,再向其中滴加__________ 和__________ ,后当观察到__________ 现象后,确定白色粉末中还含有氯化钠.
【提出问题】这包白色粉末的成分是什么?
【实验探究1】瑶瑶同学取白色粉末少许于试管中,向其中加入足量的蒸馏水充分溶解后,得到无色透明溶液,瑶瑶同学所得能出的结论是
【实验探究2】瑶瑶同学取上述所得无色透明溶液于另一试管中,向其中加入足量的稀盐酸,观察到
【实验探究3】为了验证氯化钠是否存在,瑶瑶同学做了如下实验:取原粉末少许于试管中,加足量的蒸馏水充分溶解后,再向其中滴加
您最近一年使用:0次



