《四川盐法志》记载,“敞锅熬盐”主要步骤为:①将黄卤和黑卤按比例混合;②放入敞口锅中加热浓缩,析出粗盐;③用“花水”冲洗粗盐得精品盐。
(1)步骤①中,黄卤所含杂质BaCl2和黑卤所含杂质MgSO4反应生成白色沉淀。该反应的化学方程式为__________________ 。
(2)步骤②中,析出粗盐的过程称为___________________ 。
(3)步骤③用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl。则“花水”应当是____________ (填标号)。
A.蒸馏水B.饱和NaCl溶液C.饱和NaOH溶液D.饱和BaCl2溶液
(4)将60kg含10%NaCl的黄卤和40kg含15%NaCl的黑卤混合,经“敞锅熬盐”制得的粗盐中NaCl的质量最多为__________________ kg。
(1)步骤①中,黄卤所含杂质BaCl2和黑卤所含杂质MgSO4反应生成白色沉淀。该反应的化学方程式为
(2)步骤②中,析出粗盐的过程称为
(3)步骤③用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl。则“花水”应当是
A.蒸馏水B.饱和NaCl溶液C.饱和NaOH溶液D.饱和BaCl2溶液
(4)将60kg含10%NaCl的黄卤和40kg含15%NaCl的黑卤混合,经“敞锅熬盐”制得的粗盐中NaCl的质量最多为
2018·福建·中考真题 查看更多[8]
福建省2018年中考化学试题(已下线)【万唯原创】2019年河南省中考化学试题研究卷九年级第十一单元(已下线)【万唯原创】2019年安徽省中考化学试题研究卷讲解册模块一第7-9讲(已下线)【万唯原创】2019年陕西省中考化学试题研究卷讲解册模块一-专题6-8(已下线)题型 创新题推荐·课后练习2(已下线)主题 盐 化肥·满分特训2福建省莆田市城厢区莆田第二中学2020-2021学年九年级上学期期末化学试题(已下线)专题10 流程题-5年(2018-2022)中考1年模拟化学分项汇编(福建专用)
更新时间:2018-06-25 10:21:01
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】能源既是国家经济发展的命脉,也是国家发展战略的重要支柱。
(1)目前,人类使用的燃料大多来自化石燃料,如______ 、石油、天然气等,它们是______ (填“可再生”或“不可再生”)能源。当家用燃气灶火焰呈黄色,锅底出现黑色固体时,应______ (填“调大”或“调小”)灶具的进风口,使燃料充分燃烧。
(2)在相同的温度和压强下,相同体积的气体具有相同的分子数。在20℃、101kPa下,将1m3一氧化碳和1m3甲烷分别在氧气中充分燃烧,反应完全后,消耗氧气的体积比为______ 。
(3)氢气作为能源,越来越受到人们的关注。
①氢气是一种理想清洁、高能燃料,但目前未大量使用的原因为______ (填序号)。
A.制取成本高 B.本身无毒,燃烧产物无污染
C.贮存困难 D.完全燃烧时产生热量约为同质量甲烷的二倍
②实验室用锌与稀硫酸反应制得0.4g氢气,至少需要含锌80%的锌粒(杂质不与稀硫酸反应)的质量是多少?(写出计算过程)______ 。
(1)目前,人类使用的燃料大多来自化石燃料,如
(2)在相同的温度和压强下,相同体积的气体具有相同的分子数。在20℃、101kPa下,将1m3一氧化碳和1m3甲烷分别在氧气中充分燃烧,反应完全后,消耗氧气的体积比为
(3)氢气作为能源,越来越受到人们的关注。
①氢气是一种理想清洁、高能燃料,但目前未大量使用的原因为
A.制取成本高 B.本身无毒,燃烧产物无污染
C.贮存困难 D.完全燃烧时产生热量约为同质量甲烷的二倍
②实验室用锌与稀硫酸反应制得0.4g氢气,至少需要含锌80%的锌粒(杂质不与稀硫酸反应)的质量是多少?(写出计算过程)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属材料与人类的生产和生活密切相关。请回答:
(1)家庭常见的锅有陶瓷锅、铁锅、铜锅等。
①铜锅与陶瓷锅相比,加热速度更快,利用的金属性质是______ 。
②铁锅清洗后如未擦干,容易产生红色铁锈,这是因为铁与______ 等发生化学反应。
(2)为了验证铝、铜、银三种金属的活动性顺序,设计了下列三种方案,其中可行的是:______ (填序号)。
①将铝、银分别浸入到硫酸铜溶液中
②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中
(3)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液,①滤液中一定含有的溶质是______ (填化学式);②向滤渣中滴加稀盐酸,没有气泡产生,则滤渣中一定含有的物质是______ (填化学式)。
(4)1000g含有氧化铁80%的赤铁矿石,理论上可以炼出含铁97%的生铁的质量约是______ g。(计算结果保留到小数点后一位)
(1)家庭常见的锅有陶瓷锅、铁锅、铜锅等。
①铜锅与陶瓷锅相比,加热速度更快,利用的金属性质是
②铁锅清洗后如未擦干,容易产生红色铁锈,这是因为铁与
(2)为了验证铝、铜、银三种金属的活动性顺序,设计了下列三种方案,其中可行的是:
①将铝、银分别浸入到硫酸铜溶液中
②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中
(3)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液,①滤液中一定含有的溶质是
(4)1000g含有氧化铁80%的赤铁矿石,理论上可以炼出含铁97%的生铁的质量约是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】为确定某品牌钙片(主要成分是碳酸钙,其他成分不含钙和碳酸根、不能与稀盐酸发生反应,假设其他成分难溶于水)的标签信息是否属实,进行如下实验活动。

(1)上述实验中发生反应的化学方程式为______ 。
(2)根据已知条件列出求解钙片中参加反应的物质质量(x)的比例式为______ 。
(3)每片该钙片中钙元素的质量分数为______ ,标签信息______ (填“属实”或“不属实”)。
(4)配制150g实验中所用的稀盐酸,需要36.5%的浓盐酸的质量为______ g。
(5)将滤液蒸发31.6g水,最终所得溶液的溶质的质量分数为______ 。

(1)上述实验中发生反应的化学方程式为
(2)根据已知条件列出求解钙片中参加反应的物质质量(x)的比例式为
(3)每片该钙片中钙元素的质量分数为
(4)配制150g实验中所用的稀盐酸,需要36.5%的浓盐酸的质量为
(5)将滤液蒸发31.6g水,最终所得溶液的溶质的质量分数为
您最近一年使用:0次
【推荐1】回答下列问题。
(1)用化学符号填空。
①能改良酸性土壤常见的碱是__________ ;
②标出氧化铁中铁元素的化合价_____________ 。
(2)食醋中含有醋酸,生活中人们常用食醋去除水壶里的水垢,反应的化学方程式为______ 。
(3)根据图示回答下列问题。

①下列关于图甲的说法中正确的是___ (填序号)。
A.a的溶解度大于b的溶解度
B.将t1℃时a、b、c的饱和溶液分别升温至t2℃,所得溶液中溶质质量分数b>c>a
C.将t3℃时a、b饱和溶液分别降温至t1℃,a析出的晶体一定比b多
②图乙所示的试管中盛有a、b、c三种物质中某一种物质的饱和溶液,且试管底部仍有未溶解的该物质,向烧杯中加入硝酸铵晶体,试管中固体逐渐减少,该物质是_____ (填序号)。
(1)用化学符号填空。
①能改良酸性土壤常见的碱是
②标出氧化铁中铁元素的化合价
(2)食醋中含有醋酸,生活中人们常用食醋去除水壶里的水垢,反应的化学方程式为
(3)根据图示回答下列问题。

①下列关于图甲的说法中正确的是
A.a的溶解度大于b的溶解度
B.将t1℃时a、b、c的饱和溶液分别升温至t2℃,所得溶液中溶质质量分数b>c>a
C.将t3℃时a、b饱和溶液分别降温至t1℃,a析出的晶体一定比b多
②图乙所示的试管中盛有a、b、c三种物质中某一种物质的饱和溶液,且试管底部仍有未溶解的该物质,向烧杯中加入硝酸铵晶体,试管中固体逐渐减少,该物质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
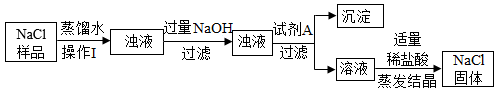
【推荐2】有一包固体粉末可能含有NaOH、NaNO3、CuCl2、CaCO3、BaCl2、Na2SO4中的一种或多种,为探究其成分,某同学取样进行了如图所示实验:

(1)操作Ⅰ和操作Ⅱ相同,其名称是___________ 。
(2)蓝色溶液溶质一定含有的成分___________ 。(填化学式)
(3)反应生成白色沉淀Ⅱ的化学方程式为___________ 。
(4)若加足量稀盐酸后,实验现象为沉淀部分溶解,产生无色气体,溶液呈蓝色,原固体粉末中一定含有的物质是___________ 。(填化学式)

(1)操作Ⅰ和操作Ⅱ相同,其名称是
(2)蓝色溶液溶质一定含有的成分
(3)反应生成白色沉淀Ⅱ的化学方程式为
(4)若加足量稀盐酸后,实验现象为沉淀部分溶解,产生无色气体,溶液呈蓝色,原固体粉末中一定含有的物质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】某工厂废液中含有氯化钠、氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如下图所示: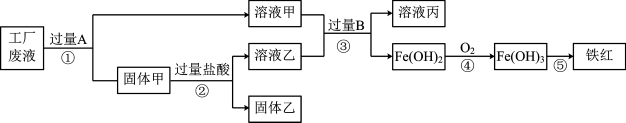
请回答下列问题:
(1)工厂废液中加入过量A反应的化学方程式为________ 。
(2)过量盐酸的作用是________ 。
(3)溶液甲中的溶质是________ (用化学式表示)。
(4)完成步骤④的化学方程式:4Fe(OH)2+O2+2____ =4Fe(OH)3
(5)能证明金属活动性Fe>Cu的过程是________ (填①-⑤)。
(6)溶液丙能否直接排放?请说明理由________

请回答下列问题:
(1)工厂废液中加入过量A反应的化学方程式为
(2)过量盐酸的作用是
(3)溶液甲中的溶质是
(4)完成步骤④的化学方程式:4Fe(OH)2+O2+2
(5)能证明金属活动性Fe>Cu的过程是
(6)溶液丙能否直接排放?请说明理由
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】溶液在生产、生活中起着十分重要的作用,请回答下列问题:
(1)下列溶液中,溶剂不是水的是______(填序号)。
(2)下表是氯化钾、硝酸钾在不同温度时的溶解度;图1为这两种物质的溶解度曲线。
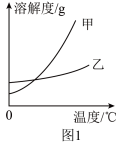
①图1中乙表示的物质是________ (填化学式);
②60 ℃时,相同质量的KCl和KNO3饱和溶液降温至20 ℃时,所得溶液中溶质质量KCl_______ (填“>”“<”或“=”)KNO3。
(3)图2是配制50 g溶质质量分数为 6%的氯化钠溶液的操作示意图。
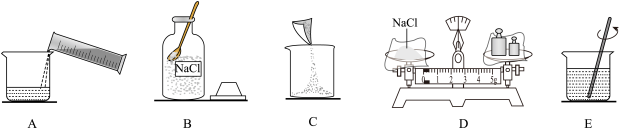
①用氯化钠固体配制氯化钠溶液,正确的操作顺序为______ (填序号);
②D中称量氯化钠的质量是______ g。
(4)在除去粗盐中不溶性杂质的实验中。
①若最初称取粗盐的质量为5.5 g,实验后得到精盐的质量是4.95 g,则该粗盐的产盐率为________ ;
②下列操作可能造成产率偏低的是________ (填序号)。
A.转移到蒸发皿中时,有液体洒出
B.过滤时液面高于滤纸边缘
C.蒸发后的精盐留有水分
(1)下列溶液中,溶剂不是水的是______(填序号)。
| A.医用酒精 | B.生理盐水 | C.碘酒 | D.硝酸钾溶液 |
(2)下表是氯化钾、硝酸钾在不同温度时的溶解度;图1为这两种物质的溶解度曲线。
| 温度/℃ | 0 | 20 | 40 | 60 |
| 溶解度/g | ||||
| 氯化钾 | 27.6 | 34.0 | 40.0 | 45.5 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110.0 |

①图1中乙表示的物质是
②60 ℃时,相同质量的KCl和KNO3饱和溶液降温至20 ℃时,所得溶液中溶质质量KCl
(3)图2是配制50 g溶质质量分数为 6%的氯化钠溶液的操作示意图。

①用氯化钠固体配制氯化钠溶液,正确的操作顺序为
②D中称量氯化钠的质量是
(4)在除去粗盐中不溶性杂质的实验中。
①若最初称取粗盐的质量为5.5 g,实验后得到精盐的质量是4.95 g,则该粗盐的产盐率为
②下列操作可能造成产率偏低的是
A.转移到蒸发皿中时,有液体洒出
B.过滤时液面高于滤纸边缘
C.蒸发后的精盐留有水分
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海洋中蕴含着丰富的化学资源,开发前景十分远大。
(1)目前海水淡化的方法主要是膜法和热法,热法中普遍采取的方法是________ 。
(2)海水晒盐能够得到粗盐,某兴趣小组同学选取一些粗盐样品,想制得较纯净的精盐,进行如下实验探究。
(3)步骤一:除去泥沙等难溶性杂质。操作的主要步骤为溶解、过滤、蒸发,在最后一步中玻璃棒的作用为________ ,以防止因局部温度过高,造成液滴进溅。
(4)步骤二:除去步骤一所得粗盐中的可溶性杂质氯化镁、氯化钙、硫酸钠,采用如图所示流程:
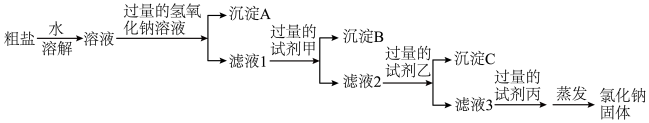
写出试剂甲溶液的溶质是________ ,试剂丙溶液的溶质是 ________ 。(均填化学式)
(1)目前海水淡化的方法主要是膜法和热法,热法中普遍采取的方法是
(2)海水晒盐能够得到粗盐,某兴趣小组同学选取一些粗盐样品,想制得较纯净的精盐,进行如下实验探究。
(3)步骤一:除去泥沙等难溶性杂质。操作的主要步骤为溶解、过滤、蒸发,在最后一步中玻璃棒的作用为
(4)步骤二:除去步骤一所得粗盐中的可溶性杂质氯化镁、氯化钙、硫酸钠,采用如图所示流程:

写出试剂甲溶液的溶质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】海洋是巨大的资源宝库,人类应合理开发利用。请回答下列问题。
(1)海水淡化:蒸馏法淡化海水是利用海水中各成分______ 不同进行分离的。
(2)海水晒盐:海水晒盐后得到的卤水是氯化钠的______ (填“饱和”或“不饱和”)溶液。
(3)海水制“碱”,在用粗盐(含 、
、 杂质)制纯碱过程中,除杂时,先后加入过量的
杂质)制纯碱过程中,除杂时,先后加入过量的 溶液和
溶液和 溶液产生的沉淀是
溶液产生的沉淀是______ ,由氯化钠制取纯碱,从元素守恒的角度看,还需要含有______ 元素的物质参加反应。
(1)海水淡化:蒸馏法淡化海水是利用海水中各成分
(2)海水晒盐:海水晒盐后得到的卤水是氯化钠的
(3)海水制“碱”,在用粗盐(含
 、
、 杂质)制纯碱过程中,除杂时,先后加入过量的
杂质)制纯碱过程中,除杂时,先后加入过量的 溶液和
溶液和 溶液产生的沉淀是
溶液产生的沉淀是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某工厂生产留下的废液中含有 、NaCl、
、NaCl、 和
和 四种物质,可按照下图的流程回收
四种物质,可按照下图的流程回收 晶体。请回答:
晶体。请回答:

(1)步骤①的目的是除去 ,则X的名称为
,则X的名称为_______ 。
(2)步骤②发生反应的化学方程式为_______ 。
(3)步骤③加入过量 溶液的目的是
溶液的目的是________ 。
(4)滤液B中所含有的金属阳离子为______ (填符号)。
(5)步骤⑤具体操作是加热浓缩、降温结晶、过滤,为提高步骤⑤后晶体的纯度和产量最好用 (填序号)进行洗涤后,再烘干。
 、NaCl、
、NaCl、 和
和 四种物质,可按照下图的流程回收
四种物质,可按照下图的流程回收 晶体。请回答:
晶体。请回答:
(1)步骤①的目的是除去
 ,则X的名称为
,则X的名称为(2)步骤②发生反应的化学方程式为
(3)步骤③加入过量
 溶液的目的是
溶液的目的是(4)滤液B中所含有的金属阳离子为
(5)步骤⑤具体操作是加热浓缩、降温结晶、过滤,为提高步骤⑤后晶体的纯度和产量最好用 (填序号)进行洗涤后,再烘干。
| A.NaCl饱和溶液 | B. 饱和溶液 饱和溶液 | C.蒸馏水 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】海洋是一个巨大的资源宝库。海水资源综合利用的部分途径如下图。 和
和  杂质,加入下列3种过量试剂的顺序依次可以是 (填字母序号之一)。
杂质,加入下列3种过量试剂的顺序依次可以是 (填字母序号之一)。
(2)按加入试剂的正确顺序,过滤后的滤渣有______ 种。
(3)在上述制取单质镁的三个反应中属于中和反应的是______ (选填“反应①”“反应②”“反应③”之一)
(4)若向分离出 晶体后的母液B(含有
晶体后的母液B(含有 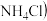 中加入过量
中加入过量 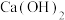 ,加热则可获得一种可以循环使用的物质,其化学式是
,加热则可获得一种可以循环使用的物质,其化学式是_______ 。
(5)海水制备氯化镁的过程中,选择石灰乳(主要成分是氢氧化钙)而不选用氢氧化钠的原因________ 。

 和
和  杂质,加入下列3种过量试剂的顺序依次可以是 (填字母序号之一)。
杂质,加入下列3种过量试剂的顺序依次可以是 (填字母序号之一)。A.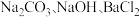 | B.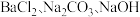 |
| C.NaOH、Na2CO3、BaCl2 | D.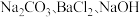 |
(2)按加入试剂的正确顺序,过滤后的滤渣有
(3)在上述制取单质镁的三个反应中属于中和反应的是
(4)若向分离出
 晶体后的母液B(含有
晶体后的母液B(含有 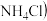 中加入过量
中加入过量 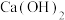 ,加热则可获得一种可以循环使用的物质,其化学式是
,加热则可获得一种可以循环使用的物质,其化学式是(5)海水制备氯化镁的过程中,选择石灰乳(主要成分是氢氧化钙)而不选用氢氧化钠的原因
您最近一年使用:0次