思维导图是激发大脑潜能,练就科学思维的有效方法。A-D是初中化学常见的四种物质,A可用于金属除锈,B难溶于水。它们相互之间的关系如图所示,“—”表示两种物质之间可以相互反应,“→”表示一种物质可生成另一种物质。分析推理,回答问题:
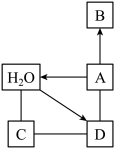
(1)A的化学式为_______________ 。A 与D反应的实质为______________________ 。
(2)A生成B的化学方程式_______________________________ 。
(3)C与D反应的化学方程式__________________________ 。

(1)A的化学式为
(2)A生成B的化学方程式
(3)C与D反应的化学方程式
2018·山西·中考真题 查看更多[17]
山西省2018年中考化学试题(已下线)2018年中考试题分项版解析汇编【第一期】专题8—1 金属材料、金属资源的利用、保护(已下线)2019年6月13日《每日一题》—— 押题10 物质的推断云南省2019届九年级中考模拟化学试题2020年广东省惠州市中考模拟化学试题(已下线)专题 物质的转化与推断·课后特训32020年重庆市部分名校中考模拟化学试题(十三)(已下线)题型 物质推断·课后训练1(已下线)题型 物质推断·课后练习2(已下线)题型 物质的推断·课后训练3(已下线)题型 物质推断·课后训练4(已下线)主题 盐 化肥?满分特训12019年山东省滨州市滨城区中考二模化学试题(B卷)2023年山东省淄博市张店区中考一模化学试题2023年山东省淄博市第十一中学中考一模化学试题山东省淄博市张店区2023-2024学年九年级上学期1月期末化学试题山东省淄博市高新片区2023-2024学年九年级上学期期末化学试题
更新时间:2018-06-23 10:30:27
|
相似题推荐
填空与简答-流程题
|
困难
(0.15)
名校
解题方法
【推荐1】稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属镧的氧化物([La2O3)广泛应用于军事、民用、医疗等领域,其颗粒大小决定了产品的质量。利用独居石(含La2O3等金属氧化物及P2O5、SiO2等非金属氧化物)生产超细La2O3颗粒的一种工艺如下:
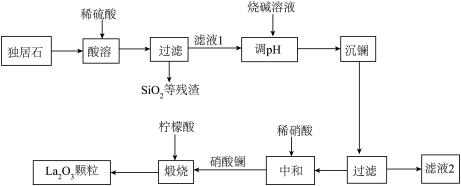
(1)“酸溶”过程中,La2O3与稀硫酸反应的化学方程式是_____ ;
(2)通过调节滤液1的pH,可将镧的盐溶液转化为镧的氢氧化物并以沉淀的形式析出,该反应的化学方程式是_____ ;
(3)“调 pH”时加入烧碱溶液使溶液的 pH_____ (填“增大”、“减小”或“不变”);
(4)将镧的氢氧化物固体溶于稀硝酸,可得到硝酸镧溶液,该反应的化学方程式是______ 。
(5)实验室使用加柠檬酸作燃料的方法,在马福炉中进行硝酸镧的煅烧,马福炉的温度设置只能为100℃的整数倍。为获得适当大小的氧化镧颗粒,某小组研究了条件对产品粒径的影响,相关数据如下:
①实验1、5、6研究的结论是:其它实验条件相同时,______ ;
②分析以上数据可知,若将实验条件变更为以下条件:硝酸镧浓度165g/L,煅烧温度700℃,煅烧1.5h,则氧化镧粒径最有可能的数值为_____ (填序号);
A 30nm B 50nm C. 80nm D 110nm
③要获得更小粒径的高纯氧化镧,在上述最佳条件的基础上,研究方向可以是____ 。
A 增加硝酸镧浓度 B 降低硝酸镧浓度 C 升高煅烧温度 D 降低煅烧温度 E 增加煅烧时间 F 减少煅烧时间

(1)“酸溶”过程中,La2O3与稀硫酸反应的化学方程式是
(2)通过调节滤液1的pH,可将镧的盐溶液转化为镧的氢氧化物并以沉淀的形式析出,该反应的化学方程式是
(3)“调 pH”时加入烧碱溶液使溶液的 pH
(4)将镧的氢氧化物固体溶于稀硝酸,可得到硝酸镧溶液,该反应的化学方程式是
(5)实验室使用加柠檬酸作燃料的方法,在马福炉中进行硝酸镧的煅烧,马福炉的温度设置只能为100℃的整数倍。为获得适当大小的氧化镧颗粒,某小组研究了条件对产品粒径的影响,相关数据如下:
| 实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 硝酸镧浓度(g/L) | 165 | 330 | 495 | 165 | 165 | 165 | 165 | 165 | 165 |
| 煅烧温度/℃ | 700 | 700 | 700 | 600 | 800 | 900 | 700 | 700 | 700 |
| 煅烧时间/h | 1 | 1 | 1 | 1 | 1 | 1 | 0.5 | 2 | 3 |
| 氧化镧粒径/nm | 42 | 63 | 75 | 不纯 | 65 | 80 | 38 | 75 | 133 |
①实验1、5、6研究的结论是:其它实验条件相同时,
②分析以上数据可知,若将实验条件变更为以下条件:硝酸镧浓度165g/L,煅烧温度700℃,煅烧1.5h,则氧化镧粒径最有可能的数值为
A 30nm B 50nm C. 80nm D 110nm
③要获得更小粒径的高纯氧化镧,在上述最佳条件的基础上,研究方向可以是
A 增加硝酸镧浓度 B 降低硝酸镧浓度 C 升高煅烧温度 D 降低煅烧温度 E 增加煅烧时间 F 减少煅烧时间
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
【推荐2】有一包固体粉末,可能含有镁粉、碳粉、氧化铜、硫酸钾、氢氧化钠中的一种或几种。
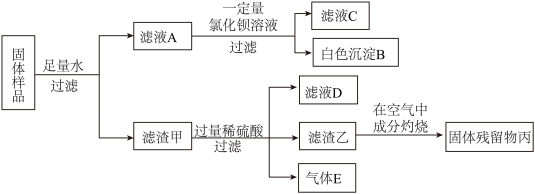
(1)实验中生成白色沉淀B的化学方程式是_______ 。
(2)实验结束后,该小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,则滤液C中一定含有的阳离子有______ (填离子符号)。
(3)测得滤渣乙的质量等于固体残留物丙的质量,由此同学推测出滤渣乙在空气中灼烧时还生成了另外一种物质,通过计算可知该物质与固体残留物丙的质量比为______ 。
(4)综合以上分析可知,原固体混合物中一定含有的物质为_______ 。

(1)实验中生成白色沉淀B的化学方程式是
(2)实验结束后,该小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,则滤液C中一定含有的阳离子有
(3)测得滤渣乙的质量等于固体残留物丙的质量,由此同学推测出滤渣乙在空气中灼烧时还生成了另外一种物质,通过计算可知该物质与固体残留物丙的质量比为
(4)综合以上分析可知,原固体混合物中一定含有的物质为
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
【推荐3】下表是从物质分类的角度认识部分酸碱盐的反应规律。
①请完成下表
②表中属于复分解反应的有__ 个;“锌和硫酸铜溶液”反应中现象是_____ 。
③可见,生成盐的途径有多种。当生成物中有硫酸钠时,可以是硫酸和氢氧化钠的反应,也可以是______ 和_____ (写出具体物质的名称或化学式,酸和碱反应除外)。
④除了表中所列,盐还能与______ (填物质类别名称)反应。
①请完成下表
| 序 列 | 物质分类的角度 | 实例 | 化学方程式 | |
| 反应物 | 生成物 | |||
1 | 盐和碱 | 盐和碱 | 碳酸钠和氢氧化钡 | Na2CO3+Ba(OH)2→BaCO3↓+2NaOH |
2 | 酸和金属 | 盐和氢气 | 铁和稀硫酸 | |
3 | 盐和盐 | 盐和盐 | 硝酸银和 | |
4 | 盐和金属 | 盐和金属 | 锌和硫酸铜溶液 | |
③可见,生成盐的途径有多种。当生成物中有硫酸钠时,可以是硫酸和氢氧化钠的反应,也可以是
④除了表中所列,盐还能与
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
名校
【推荐1】硼(B)及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和难溶性SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:

已知:①Mg2B2O5·H2O+2H2SO4 2MgSO4+2H3BO3②CaSO4微溶于水
2MgSO4+2H3BO3②CaSO4微溶于水
③H2O2溶液可将Fe2+氧化为Fe3+④Fe3+、Fe2+、Al3+以氢氧化物形式开始沉淀和完全沉淀时的pH如下表:
请回答下列问题:
(1)利用______ (填物质名称)的磁性,可将该物质直接从“铁硼矿粉”中分离。
(2)酸浸时,矿粉中的金属氧化物会和酸反应,试写出Fe2O3酸浸时的化学反应方程式__________ 。
(3)为了提高浸出速率(即加快反应速率),除适当增加硫酸浓度外,还可采取的措施有______ (写出一条)。
(4)操作a为______ ,“浸渣”中含有CaSO4和______ (填物质化学式)。
(5)“净化除杂”需先加H2O2溶液,然后再调节溶液的pH约为5,目的是_____ 。
(6)制得的粗硼酸中的主要杂质为________________ (填物质化学式)。

已知:①Mg2B2O5·H2O+2H2SO4
 2MgSO4+2H3BO3②CaSO4微溶于水
2MgSO4+2H3BO3②CaSO4微溶于水③H2O2溶液可将Fe2+氧化为Fe3+④Fe3+、Fe2+、Al3+以氢氧化物形式开始沉淀和完全沉淀时的pH如下表:
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 1.14 | 3.0 |
| Fe2+ | 5.85 | 8.35 |
| Al3+ | 3.0 | 4.7 |
(1)利用
(2)酸浸时,矿粉中的金属氧化物会和酸反应,试写出Fe2O3酸浸时的化学反应方程式
(3)为了提高浸出速率(即加快反应速率),除适当增加硫酸浓度外,还可采取的措施有
(4)操作a为
(5)“净化除杂”需先加H2O2溶液,然后再调节溶液的pH约为5,目的是
(6)制得的粗硼酸中的主要杂质为
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
【推荐2】酸、碱、盐在生产和生活中有着广泛的应用。

(1)图1是氢氧化钠和硫酸反应的微观示意图,从图中可知,酸碱中和反应的实质是_______ 。
(2)图2是氢氧化钠和硫酸反应时的pH变化情况。从图中能看出,是把_____ 溶液加到另外一种溶液中。当加入该溶液的质量为bg时,溶液中的溶质是_____ 。
(3)以粗盐(主要成分是NaCl,含有不溶性泥砂、可溶性的MgCl2、CaCl2等杂质)为原料,电解食盐水生产氢氧化钠的简要流程如图3:
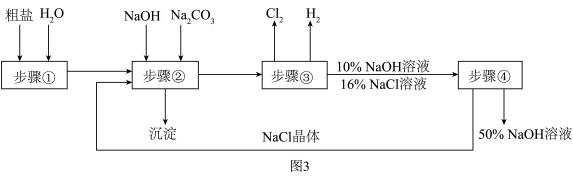
①步骤②除去可溶性杂质,写出其中一个化学方程式______ 。
②步骤③氯化钠饱和溶液在通电条件下发生反应的化学方程式是_____ 。
(4)某兴趣小组发现了一瓶敞口放置的氢氧化钠固体,经实验确定该固体已变质。为确定固体中碳酸钠的质量分数,小组同学利用如图4装置进行探究。
查阅资料:碱石灰是NaOH和CaO的固体混合物。
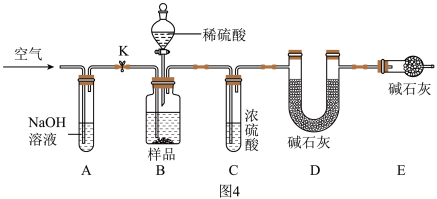
①A的作用是_____ 。
②通过称量D装置反应前后的质量变化,可以测定碳酸钠的质量分数。如果没有E 装置,则测得的碳酸钠的质量分数会______ (填“偏大”“偏小”或“无影响”)。
(5)取上述变质氢氧化钠样品10g进行实验,反应前称得D装置为50g,完全反应后称得D装置为52.2g。求该氢氧化钠样品中碳酸钠的质量分数_____ 。

(1)图1是氢氧化钠和硫酸反应的微观示意图,从图中可知,酸碱中和反应的实质是
(2)图2是氢氧化钠和硫酸反应时的pH变化情况。从图中能看出,是把
(3)以粗盐(主要成分是NaCl,含有不溶性泥砂、可溶性的MgCl2、CaCl2等杂质)为原料,电解食盐水生产氢氧化钠的简要流程如图3:

①步骤②除去可溶性杂质,写出其中一个化学方程式
②步骤③氯化钠饱和溶液在通电条件下发生反应的化学方程式是
(4)某兴趣小组发现了一瓶敞口放置的氢氧化钠固体,经实验确定该固体已变质。为确定固体中碳酸钠的质量分数,小组同学利用如图4装置进行探究。
查阅资料:碱石灰是NaOH和CaO的固体混合物。

①A的作用是
②通过称量D装置反应前后的质量变化,可以测定碳酸钠的质量分数。如果没有E 装置,则测得的碳酸钠的质量分数会
(5)取上述变质氢氧化钠样品10g进行实验,反应前称得D装置为50g,完全反应后称得D装置为52.2g。求该氢氧化钠样品中碳酸钠的质量分数
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
【推荐3】在如图所示的转盘中,A~F分别代表Na2CO3、NaNO3、NaOH、HNO3、Na2SO4、NaCl六种物质中的一种。已知:B的俗名为纯碱,A和E可发生中和反应,A、B、C、D、E都能转化成F,A、B、C、D能依次转化。请根据初中所学化学知识回答下列问题:

(1)F的化学式为_____ 。
(2)让指针逆时针从当前位置开始转动,若所指物质能转化为下一物质,指针可继续转动,否则停止。则使指针停止转动的物质D为___ (填物质名称)。
(3)让指针顺时针从当前位置开始转动,若所指物质不能转化为下一物质,指针可继续转动,否则停止。则指针将停止在____ (填字母编号)物质上。
(4)写出下列指定的化学方程式:
①E转化成F的中和反应____ 。
②C转化成D_____ 。

(1)F的化学式为
(2)让指针逆时针从当前位置开始转动,若所指物质能转化为下一物质,指针可继续转动,否则停止。则使指针停止转动的物质D为
(3)让指针顺时针从当前位置开始转动,若所指物质不能转化为下一物质,指针可继续转动,否则停止。则指针将停止在
(4)写出下列指定的化学方程式:
①E转化成F的中和反应
②C转化成D
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
【推荐1】现有一白色固体混合物,可能由BaCl2、KOH、KNO3、MgCl2、CuSO4中的几种混合而成。为证明其组成,做如下实验:
(1)取一定量该固体混合物加入足量的水,充分搅拌,得到白色沉淀和无色液体。过滤得白色沉淀①和无色滤液①。则原混合物一定含有_________ ,一定不含有_________ 。
(2)向无色滤液①中加入KOH溶液,无任何现象,再加入过量的某可溶性碳酸盐溶液,充分反应后过滤,得白色沉淀②,无色滤液②,则原混合物中一定还含有_________ 。
(3)向无色滤液②中加入过量的盐酸,然后将所得的液体蒸干,得到固体A。如果固体A中只含有2种元素,A为_________ ,则加入的碳酸盐溶液是_________ ,如果固体A中含有两种金属元素,则加入的碳酸盐溶液是_________ 。
(1)取一定量该固体混合物加入足量的水,充分搅拌,得到白色沉淀和无色液体。过滤得白色沉淀①和无色滤液①。则原混合物一定含有
(2)向无色滤液①中加入KOH溶液,无任何现象,再加入过量的某可溶性碳酸盐溶液,充分反应后过滤,得白色沉淀②,无色滤液②,则原混合物中一定还含有
(3)向无色滤液②中加入过量的盐酸,然后将所得的液体蒸干,得到固体A。如果固体A中只含有2种元素,A为
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
真题
【推荐2】A~G是初中化学中常见的七种物质,其中A、B、C、E、F、G含有同一种元素,A、B、C、E、G是五种不同类别的物质;D和F在通常情况下为气体,两者分别溶于水后溶液的酸碱性相反.它们相互间的关系如图所示.(图中“﹣”表示相连的物质之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去.)

(1)G的化学式是____________ .
(2)A与D反应符合绿色化学的原则,属于_______ 反应(填基本反应类型).
(3)C→D+E+F的化学方程式:____________________________ .
(4)从微观的角度分析A与B能发生反应的原因是______________________ .

(1)G的化学式是
(2)A与D反应符合绿色化学的原则,属于
(3)C→D+E+F的化学方程式:
(4)从微观的角度分析A与B能发生反应的原因是
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
名校
解题方法
【推荐3】某固体样品中含有的离子由Na+、Ca2+、Ba+、 、
、 、
、 、
、 中的若干种组成,取适量该固体进行如下实验:
中的若干种组成,取适量该固体进行如下实验:
【查阅资料】
标准状况下1mol气体的体积为22.4L。
回答下列问题:
(1)固体E中所含物质的化学式为____________ 。
(2)可用____________ 检验气体C,现象是____________ 。
(3)1.97gBaCO3在空气中高温充分灼烧得到1.69g固体,经检验没有产生有毒气体,写出高温灼烧时发生反应的化学方程式:_____________ 。
(4)100mL无色溶液A中c( )=
)=____________ mol/L,固体样品中n( )=
)=____________ mol。
(5)当m>___________ g时,100mL无色溶液A中会含有 ,此时c(
,此时c( )=
)=____________ mol/L(用含m的代数式表示)。
 、
、 、
、 、
、 中的若干种组成,取适量该固体进行如下实验:
中的若干种组成,取适量该固体进行如下实验: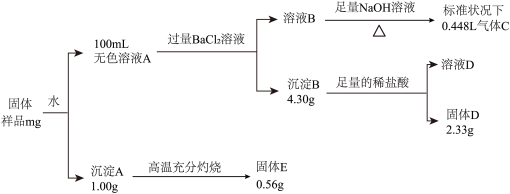
【查阅资料】
标准状况下1mol气体的体积为22.4L。
回答下列问题:
(1)固体E中所含物质的化学式为
(2)可用
(3)1.97gBaCO3在空气中高温充分灼烧得到1.69g固体,经检验没有产生有毒气体,写出高温灼烧时发生反应的化学方程式:
(4)100mL无色溶液A中c(
 )=
)= )=
)=(5)当m>
 ,此时c(
,此时c( )=
)=
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
【推荐1】下图中A、B、C、D、E、F是初中化学常见的六种物质。C是胃液中含有的酸,A、B是盐溶液,E、F是氧化物,D与F反应时现象明显。(图中用“—”或“⌒”表示两种物质能发生反应,用“ ”“
”“ ”或“
”或“ ”表示两种物质能单向或双向转化,用“
”表示两种物质能单向或双向转化,用“ ”表示两种物质既能单向转化又能反应。部分反应物、生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质。)
”表示两种物质既能单向转化又能反应。部分反应物、生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质。)

(1)写出D、F(或主要成分)的化学式: D_____ ; F_____ ;
(2)C A的实验现象是
A的实验现象是_____ ;
(3)A B的化学方程式是
B的化学方程式是_____ 。
 ”“
”“ ”或“
”或“ ”表示两种物质能单向或双向转化,用“
”表示两种物质能单向或双向转化,用“ ”表示两种物质既能单向转化又能反应。部分反应物、生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质。)
”表示两种物质既能单向转化又能反应。部分反应物、生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质。)
(1)写出D、F(或主要成分)的化学式: D
(2)C
 A的实验现象是
A的实验现象是(3)A
 B的化学方程式是
B的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
解题方法
【推荐2】以橄榄石尾矿(主要成分MgO、Fe2O3等)为原料,生产高纯Mg(OH)2的部分工艺流程如下(此流程不考虑其它微量杂质的反应):
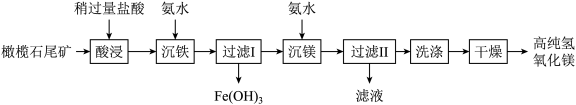
(1)“酸浸”后,溶液中含有的金属阳离子有___________ (写离子符号)。
(2)“酸浸”过程中加入“稍过量盐酸”。盐酸不能加得太多的原因是___________ 。
(3)由工艺流程中先“沉铁”后“沉镁”,可推断:氢氧化铁完全沉淀时的pH___________ (选填“高于”“低于”“等于”)氢氧化镁完全沉淀时的pH。
(4)“滤液”主要成分的化学式为___________ ,写出该物质的一种用途:_____ 。
(5)添加了氢氧化镁的沥青有阻燃作用,原理是氢氧化镁受热分解会吸收热量。取同质量的基质沥青和添加了一定量氢氧化镁的阻燃沥青进行加热,结果如图所示。表示阻燃沥青的是___________ (选填“虚线”“实线”)。


(1)“酸浸”后,溶液中含有的金属阳离子有
(2)“酸浸”过程中加入“稍过量盐酸”。盐酸不能加得太多的原因是
(3)由工艺流程中先“沉铁”后“沉镁”,可推断:氢氧化铁完全沉淀时的pH
(4)“滤液”主要成分的化学式为
(5)添加了氢氧化镁的沥青有阻燃作用,原理是氢氧化镁受热分解会吸收热量。取同质量的基质沥青和添加了一定量氢氧化镁的阻燃沥青进行加热,结果如图所示。表示阻燃沥青的是

您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
解题方法
【推荐3】元素X、Y,Z的相关信息如下表所示。
(1)若A、B、C分别是由X、Y,Z中的一种或两种元素组成的纯净物。它们之间的转化关系如下图所示。(“→”表示转化关系,部分反应物、生成物及反应条件已略去),A、B是组成元素相同的氧化物,请回答下列问题:
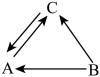
A的化学式为______ ;该物质由______ 构成(填“分子”、“原子”或“离子”)。B→C的反应类型是______ 。(填“化合反应”“分解反应”或者“无法确定”)
(2)若A为两种元素组成的气体10g,且两种元素质量比为3:22,C、D、E均为纯净物,每步都是恰好完全反应。
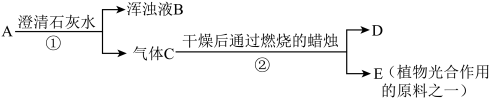
根据上述转化关系回答下列问题。
A从分类上看属于(填“化合物”,“混合物”或者“纯净物”)______ ;气体C的质量为______ ;若生成E的质量为4.4g,请推测蜡烛的元素组成______ 。
| 元素 | X | Y | Z |
| 相关信息 | 该元素原子的结构示意图为: | 该元素是地壳中含量最多的元素 | 位于第二周期,最外层有4个电子 |
(1)若A、B、C分别是由X、Y,Z中的一种或两种元素组成的纯净物。它们之间的转化关系如下图所示。(“→”表示转化关系,部分反应物、生成物及反应条件已略去),A、B是组成元素相同的氧化物,请回答下列问题:

A的化学式为
(2)若A为两种元素组成的气体10g,且两种元素质量比为3:22,C、D、E均为纯净物,每步都是恰好完全反应。

根据上述转化关系回答下列问题。
A从分类上看属于(填“化合物”,“混合物”或者“纯净物”)
您最近一年使用:0次



