利用某工业废弃固体(成分为Cu2S和FeS2)制备硫酸铜溶液和硫酸亚铁晶体,流程如图所示。
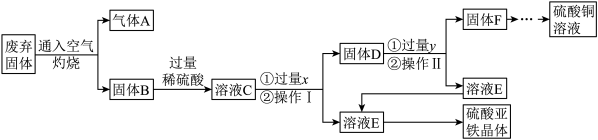
(已知:①固体B含有氧化铜、氧化铁②铁能与硫酸铁反应,生成硫酸亚铁)
(1)操作I是_____ 。为了提高废弃固体的反应速率,除将固体粉碎、提高温度外,还可以采取的具体措施有_____ (写一条)。
(2)写出FeS2在空气中灼烧的化学方程式_____ 。
(3)溶液C中的溶质有_____ (用化学式表示)。
(4)试剂y的作用是_____ 。

(已知:①固体B含有氧化铜、氧化铁②铁能与硫酸铁反应,生成硫酸亚铁)
(1)操作I是
(2)写出FeS2在空气中灼烧的化学方程式
(3)溶液C中的溶质有
(4)试剂y的作用是
2018·广西玉林·中考真题 查看更多[4]
广西玉林市2018年中考化学试题2020年广西崇左市江州区中考四模化学试题(已下线)第五单元 金属的冶炼与利用(能力提升)-2020-2021学年九年级化学上册单元测试定心卷(沪教版)广西北部湾经济区六市2019届九年级中考二模化学试题
更新时间:2018-07-31 23:37:49
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】化学就在我们身边,请用所学化学知识回答下列问题:
(1)利用空气制取氮肥的流程如下图所示。
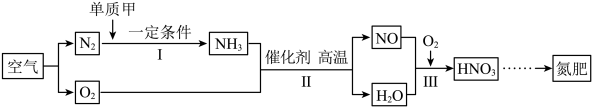
Ⅰ中参加反应的单质甲为___________ 。
Ⅱ中反应的化学方程式为___________ 。
(2)为防止钢铁锈蚀,常在铁制品表面刷含铝粉的防锈漆,这是因为铝在空气中能自我保护,表面形成一层致密的氧化膜。化学方程式是___________ 。
(3)向含有硫酸亚铁和硫酸铜的废液中加入某种金属,可回收硫酸亚铁和铜。该反应的化学方程式是___________ 。
(4)甲醇(CH3OH)可用作赛车燃料。若其燃烧产物与石蜡燃烧产物相同,则甲醇燃烧的化学方程式为___________ 。
(5)阻燃剂氢氧化铝受热分解时吸收热量,同时生成耐高温的氧化铝和水蒸气,起到防火作用。写出阻燃剂氢氧化铝受热分解的化学方程式为___________ 。
(1)利用空气制取氮肥的流程如下图所示。

Ⅰ中参加反应的单质甲为
Ⅱ中反应的化学方程式为
(2)为防止钢铁锈蚀,常在铁制品表面刷含铝粉的防锈漆,这是因为铝在空气中能自我保护,表面形成一层致密的氧化膜。化学方程式是
(3)向含有硫酸亚铁和硫酸铜的废液中加入某种金属,可回收硫酸亚铁和铜。该反应的化学方程式是
(4)甲醇(CH3OH)可用作赛车燃料。若其燃烧产物与石蜡燃烧产物相同,则甲醇燃烧的化学方程式为
(5)阻燃剂氢氧化铝受热分解时吸收热量,同时生成耐高温的氧化铝和水蒸气,起到防火作用。写出阻燃剂氢氧化铝受热分解的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
【推荐2】2015年4月25日14时11分,尼泊尔发生8.1级地震。在抗震救灾中,可使用“84”消毒液(NaClO溶液)的稀溶液进行消毒。制取NaClO的化学方程式为2NaOH+X=NaClO+NaCl+H2O。由于“84”消毒液有一定的腐蚀性,使用时应将其稀释成0.2%~0.5%的稀溶液。
(1)X的化学式为____ ,NaClO中氯元素化合价为____ 。
(2)配制120kg质量分数为0.5%的“84”消毒液,需使用12%的“84”消毒液_________ kg。
(3)地震后,水源受到严重污染。为了保证本地饮用水的安全,生活用水需多次消毒。
①如果使用二氧化氯消毒杀菌,该变化过程属于____ (填“物理变化”或“化学变化”);
②如果使用漂白粉作为水源消毒剂,漂白粉的有效成分为次氯酸钙,其化学式为Ca(ClO)2,次氯酸钙溶于水与空气中的CO2反应生成碳酸钙和次氯酸(HClO)。请写出该反应的化学方程式___________________ 。
(4)为防止疫病传染,需对河水处理后方可饮用,常用措施有:①加热煮沸 ②消毒 ③过滤 ④自然沉降,较合理的顺序为______ (填字母序号)。
(1)X的化学式为
(2)配制120kg质量分数为0.5%的“84”消毒液,需使用12%的“84”消毒液
(3)地震后,水源受到严重污染。为了保证本地饮用水的安全,生活用水需多次消毒。
①如果使用二氧化氯消毒杀菌,该变化过程属于
②如果使用漂白粉作为水源消毒剂,漂白粉的有效成分为次氯酸钙,其化学式为Ca(ClO)2,次氯酸钙溶于水与空气中的CO2反应生成碳酸钙和次氯酸(HClO)。请写出该反应的化学方程式
(4)为防止疫病传染,需对河水处理后方可饮用,常用措施有:①加热煮沸 ②消毒 ③过滤 ④自然沉降,较合理的顺序为
| A.③①②④ | B.④①③② |
| C.④③②① | D.③①④② |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】人类文明进步与金属材料的发展关系十分密切,金属在生活和生产中有着非常广泛的应用。请回答下列问题。
(1)我国是世界上已知矿物种类比较齐全的少数国家之一、在赤铁矿(主分成分是Fe2O3),菱铁矿(主分成分是FeCO3)、铝土矿(主分成分是A12O3)、辉铜矿(主分成分是Cu2S)中,其主要成分属于氧化物的是____________ (填矿石名称)。近代工业上采用电解熔融氧化铝(A12O3)的方法冶炼铝,A12O3分解后得到两种单质,该反应的化学方程式为___________ 。
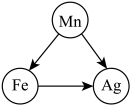
(2)已知Fe、Mn、Ag三种金属存在如图所示的转化关系,则三种金属的活动性由强到弱的顺序是____________ ,欲验证三种金凤的活动性顺序,可选用的一组药品为Mn、Ag和____________ 溶液。
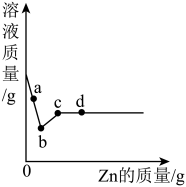
(3)向一定质量Cu(NO3)2、AgNO3混合溶液中加入Zn,溶液质量与加入Zn如的质量关系如图所示。下列说法正确的是____________(填字母序号)。
(1)我国是世界上已知矿物种类比较齐全的少数国家之一、在赤铁矿(主分成分是Fe2O3),菱铁矿(主分成分是FeCO3)、铝土矿(主分成分是A12O3)、辉铜矿(主分成分是Cu2S)中,其主要成分属于氧化物的是
(2)已知Fe、Mn、Ag三种金属存在如图所示的转化关系,则三种金属的活动性由强到弱的顺序是

(3)向一定质量Cu(NO3)2、AgNO3混合溶液中加入Zn,溶液质量与加入Zn如的质量关系如图所示。下列说法正确的是____________(填字母序号)。

| A.取a点溶液,滴加稀盐酸,有白色沉淀生成 |
| B.取b点溶液中一定含有Zn2+和Cu2+,可能含有Ag+ |
| C.取bc段固体,滴加稀盐酸,有气泡产生 |
| D.取d点固体有3种 |
您最近一年使用:0次
【推荐1】某化工厂排出的废水透明、澄清、略显蓝色。一同学取少量废水,加入过量的盐酸,有不溶于稀硝酸的白色沉淀生成。过滤,所得的滤液分成两份,一份滤液中加入稀硫酸,也有不溶于稀硝酸的白色沉淀生成;另一份滤液中加入氢氧化钠溶液,产生蓝色溶液。试回答:
(1)加入过量的盐酸,生成的白色沉淀是___________ ;加入NaOH溶液,生成的蓝色沉淀是___________ 。
(2)废水中一定含有的物质是_________(填编号)。
(3)该同学设计了一个从废水中除去重金属离子的实验方案如下【已知:白色的Fe(OH)2固体在潮湿的空气中可生成红褐色的Fe(OH)3】:
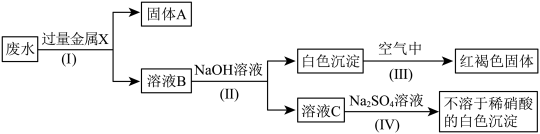
①金属X为___________ ,固体A中一定含有的物质为___________ (写化学式)。
②B溶液中的溶质一定含有___________ (填化学式)。
③第Ⅲ步反应的化学方程式为___________ 。
(1)加入过量的盐酸,生成的白色沉淀是
(2)废水中一定含有的物质是_________(填编号)。
| A.氯化物 | B.硫酸盐 | C.硝酸盐 | D.碳酸盐 |
(3)该同学设计了一个从废水中除去重金属离子的实验方案如下【已知:白色的Fe(OH)2固体在潮湿的空气中可生成红褐色的Fe(OH)3】:

①金属X为
②B溶液中的溶质一定含有
③第Ⅲ步反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下:
资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体。
资料2:+2价的铁元素容易被空气中的氧气氧化。
回答下列问题:

(1)发电厂是利用垃圾焚烧产生的热能转变为_______ 能。
(2)吸收步骤中,石灰浆的作用是_______ 。
(3)溶解步骤中,产生H2的化学方程式为_______ ,除此反应外,溶解步骤还能发生两个反应:①Fe2O3+3H2SO4═Fe2(SO4)3+3H2O ②Fe+Fe2(SO4)3═3FeSO4,其中反应前后铁元素的化合价不变的是反应______ (填“①”或“②”)。
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、_______ (填操作名称),得到硫酸亚铁晶体,其中氮气的作用是_______ 。
资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体。
资料2:+2价的铁元素容易被空气中的氧气氧化。
回答下列问题:

(1)发电厂是利用垃圾焚烧产生的热能转变为
(2)吸收步骤中,石灰浆的作用是
(3)溶解步骤中,产生H2的化学方程式为
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
真题
解题方法
【推荐3】已知A、B、C、D是初中化学常见的四种不同类别的物质,相邻两物质都可以发生化学反应,分别生成甲、乙、丙、丁四种物质(部分生成物已经略去),它们之间的关系如图所示。其中B为杀菌剂波尔多液的成分之一,其溶液呈蓝色;C为应用最广泛的金属;丙为氯化物。
(1)B的化学式是_____ ;A所属的物质类别是_____ 。
(2)B的溶液与C反应后,溶液的质量_____ (填“增大”“减小”或“不变”)。
(3)C与D反应的化学方程式是_____ ;A与B反应的基本类型属于_____ 。
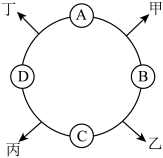
(1)B的化学式是
(2)B的溶液与C反应后,溶液的质量
(3)C与D反应的化学方程式是

您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】合金A由几种单质组成,取少量该合金做实验,见下图。已知:①合金A中不含K、Ca、Na;②气体B是自然界中最轻的气体;③气体G是导致温室效应的主要气体。
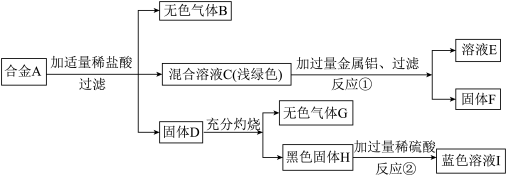
请回答:
(1)过滤时需用到的玻璃仪器有:玻璃棒、______ 、______ 。
(2)组成合金A的单质有(用化学式表示):______ 、______ 、______ 。
(3)反应①的化学方程式为______ ;反应②的化学方程式为______ 。
(4)已知Al(OH)3溶解于过量的NaOH溶液。如果要验证合金中还存在金属镁,应取少量溶液______ (选填:C、E、I)滴入过量的的NaOH溶液。

请回答:
(1)过滤时需用到的玻璃仪器有:玻璃棒、
(2)组成合金A的单质有(用化学式表示):
(3)反应①的化学方程式为
(4)已知Al(OH)3溶解于过量的NaOH溶液。如果要验证合金中还存在金属镁,应取少量溶液
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】某合金主要成分为Zn、Fe、Cu,还含有少量这三种金属的氧化物。利用该合金制成的机械零件废弃物制取高纯度ZnO,其部分工艺流程如下图所示。已知: Zn(OH) 2溶于NaOH等强碱形成可溶性盐。回答相关问题:
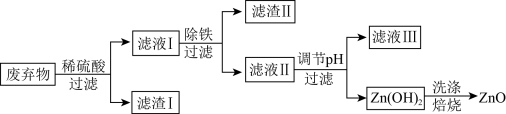
(1)滤渣I中一定有___________ 。
(2)加酸溶解废弃物时,需要通风并远离火源,其原因是__________ 。 此过程中Zn还能起到除去含铜化合物的作用.写出该反应的化学方程式:______________ 。
(3)调节溶液的pH可用NaOH,但不能过量,其原因是____________ 。
(4)焙烧Zn(OH) 2发生分解反应的化学方程式为___________ 。

(1)滤渣I中一定有
(2)加酸溶解废弃物时,需要通风并远离火源,其原因是
(3)调节溶液的pH可用NaOH,但不能过量,其原因是
(4)焙烧Zn(OH) 2发生分解反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】我国早在商代时期就开始使用铜器,到春秋战国时期,开始生产和使用铁器。
(1)铁锅用于烹饪食物主要是利用铁具有良好的______ 性。
(2)下列文物中不属于金属制品的是______(填字母序号)。
(3)《本草纲目拾遗》中记载:“舶上铁日久起销(锈)…刮下之销末,名铁线粉”。铁丝“日久起销”的原因是铁与空气中的______ (填化学式)同时接触而导致。
(4)我国古代曾用“湿法炼铜”和“火法炼铜”,其原理分别为:
①湿法炼铜:Fe+CuSO4=Cu+FeSO4
②火法炼铜:Cu2S+O2 2Cu+SO2
2Cu+SO2
上述两种方案中较优的是______ (填数字序号),理由是______ 。
(5)将一定量的铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液。下列判断正确的是______(填字母序号)。
(6)某金属粉末含有Mg、Al、Cu、Ag中的一种或几种,取24g该金属粉末与足量的稀盐酸反应产生2g氢气,则该金属粉末的组成情况有_______ 种。
(1)铁锅用于烹饪食物主要是利用铁具有良好的
(2)下列文物中不属于金属制品的是______(填字母序号)。
A.鎏金骑士铜贮贝器 | B.鸡形陶壶 |
C.牛虎铜案 | D.滇王金印 |
(3)《本草纲目拾遗》中记载:“舶上铁日久起销(锈)…刮下之销末,名铁线粉”。铁丝“日久起销”的原因是铁与空气中的
(4)我国古代曾用“湿法炼铜”和“火法炼铜”,其原理分别为:
①湿法炼铜:Fe+CuSO4=Cu+FeSO4
②火法炼铜:Cu2S+O2
 2Cu+SO2
2Cu+SO2上述两种方案中较优的是
(5)将一定量的铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液。下列判断正确的是______(填字母序号)。
| A.滤液中一定有Zn(NO3)2 |
| B.滤渣的质量一定大于所加入固体的质量 |
| C.向滤渣中加入稀硫酸,有气泡产生,则滤渣中一定有Zn,一定不含Ag |
| D.若滤液为蓝色、则滤液中一定含有硝酸锌和硝酸铜,一定役有硝酸银 |
(6)某金属粉末含有Mg、Al、Cu、Ag中的一种或几种,取24g该金属粉末与足量的稀盐酸反应产生2g氢气,则该金属粉末的组成情况有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】某电镀厂排放的污水中含有CuSO4、ZnSO4、FeSO4,为减少水污染及节约成本,回收重要物质硫酸锌及有关金属,设计如图所示流程。你做小小工程师,解释问题:
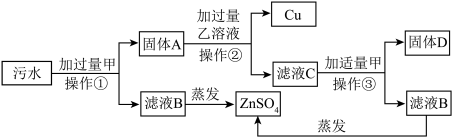
(1)操作①、②、③都是相同的操作,化学上叫___________ 。固体D是___________ (填物质)。
(2)污水中加入过量甲时,发生的反应有___________ (用化学方程式表示),观察到___________ 时停止加入甲。
(3)乙溶液中的溶质是___________ (填化学式)。固体A中加入乙必须过量的目的是___________ 。

(1)操作①、②、③都是相同的操作,化学上叫
(2)污水中加入过量甲时,发生的反应有
(3)乙溶液中的溶质是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】氯化钡是一种可溶性重金属盐,广泛应用于化工领域。用毒重石(主要成分为BaCO3)制备氯化钡晶体工艺流程如下:
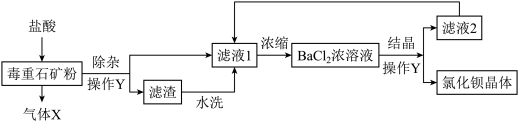
(1)毒重石要进行粉碎的目的是____ 。气体X的化学式为____ 。
(2)操作Y的名称是____ 。该操作中用到的玻璃仪器有烧杯,玻璃棒和____ ,其中玻璃棒作用____ 。滤液2中可循环利用的物质除水外还有____ 。洗涤氯化钡晶体最适宜的洗涤剂是____ (填字母)。
A.30℃水 B.30℃饱和氯化钠溶液 C.30℃饱和氯化钡溶液
(3)滤渣水洗的目的是_____________ 和 ______________ 。
(4)取一定量的产物配成100 g 质量分数为5.2%的溶液,需要溶质的质量为________ g,若量取水时俯视读数,则溶质质量分数将________ (填“偏大”、“偏小”“不变”)。

(1)毒重石要进行粉碎的目的是
(2)操作Y的名称是
A.30℃水 B.30℃饱和氯化钠溶液 C.30℃饱和氯化钡溶液
(3)滤渣水洗的目的是
(4)取一定量的产物配成100 g 质量分数为5.2%的溶液,需要溶质的质量为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】碳化硅(SiC)具有独特的光学、电学及力学等性能,在众多战略行业具有重要的应用价值和广阔的应用前景。一种以石英砂(含有SiO2、Fe2O3、Al2O3及杂质)和焦炭为主要原料制备碳化硅的生产工艺流程如图所示。(已知:①金属氧化物能与酸反应,二氧化硅不与酸反应;②其他杂质不溶于水或酸)

(1)粉碎机内将焦炭粉碎的目的是_______ ,酸洗池中除去的物质是_______ ,酸洗后为将固体和溶液分离可进行_______ 操作。
(2)电阻炉中是焦炭与二氧化硅的主要反应场所,在高温条件下产生碳化硅和一种具有可燃性的氧化物,该反应方程式是_______ ,其中C具有_______ 性(填“氧化”或“还原”)。
(3)关于电阻炉中反应的说法正确的是______。
(4)从环保角度考虑,上述生产流程需要注意的是______ (写一条)。

(1)粉碎机内将焦炭粉碎的目的是
(2)电阻炉中是焦炭与二氧化硅的主要反应场所,在高温条件下产生碳化硅和一种具有可燃性的氧化物,该反应方程式是
(3)关于电阻炉中反应的说法正确的是______。
| A.SiO2是由Si原子和O2分子构成 |
| B.反应后固体减少的质量等于生成气体的质量 |
| C.反应前后元素的化合价均未发生变化 |
| D.产物中的氧化物在工业上可用于冶炼金属 |
(4)从环保角度考虑,上述生产流程需要注意的是
您最近一年使用:0次



