现有一包黑色固体粉,可能含有炭粉、CuO、Fe3O4中的两种或者三种,某化学兴趣小组通过实验探究其成分。
(1)提出问题:该黑色固体粉末成分是什么?
(2)作出猜想:
猜想一:混合固体是炭粉、CuO
猜想二:混合固体是炭粉、Fe3O4
猜想三:混合固体是______ (两种物质写不全不给分)
猜想四:混合固体是炭粉、CuO、Fe3O4
(3)查阅资料:Fe3O4为黑色粉末,能与盐酸反应,含有Fe3+的盐溶液遇到KSCN(硫氰化钾)溶液时变成红色,Fe(OH)2是一种白色沉淀。
(4)实验探究:取一定量的固体于试管中,加足量的盐酸,充分反应后有部分固体溶解,过滤,得到滤液A,并对滤液A的成分进行如下探究:
(5)讨论交流:
①通过以上实验,猜想______ 成立。
②写出Fe3O4与盐酸反应的化学方程式_____ 。
③Fe3O4与盐酸反应时元素的化合价没有改变,请大家推断Fe3O4中铁元素的化合价为___ (写两种价态才得分)。
(6)拓展:请写出同种元素显不同化合价的一种盐_____ (其它合理答案也得分)(写化学式)。
(1)提出问题:该黑色固体粉末成分是什么?
(2)作出猜想:
猜想一:混合固体是炭粉、CuO
猜想二:混合固体是炭粉、Fe3O4
猜想三:混合固体是
猜想四:混合固体是炭粉、CuO、Fe3O4
(3)查阅资料:Fe3O4为黑色粉末,能与盐酸反应,含有Fe3+的盐溶液遇到KSCN(硫氰化钾)溶液时变成红色,Fe(OH)2是一种白色沉淀。
(4)实验探究:取一定量的固体于试管中,加足量的盐酸,充分反应后有部分固体溶解,过滤,得到滤液A,并对滤液A的成分进行如下探究:
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取一定量滤液A于试管中,加入足量的铁粉 | 无红色固体析出 | 该固体物质一定没有 |
| 步骤二:又取一定量的滤液A于试管中,加入少量的KSCN(硫氰化钾)溶液 | 溶液变成红色 | 滤液A中还一定含有的物质是 |
| 步骤三:再取一定量的滤液A于试管中,加入足量的NaOH溶液 | 有红褐色沉淀生成,同时还有少量的白色沉淀生成,白色沉淀迅速变成灰绿色,最后面变成红褐色 | 滤液A中还一定含有的物质是 |
(5)讨论交流:
①通过以上实验,猜想
②写出Fe3O4与盐酸反应的化学方程式
③Fe3O4与盐酸反应时元素的化合价没有改变,请大家推断Fe3O4中铁元素的化合价为
(6)拓展:请写出同种元素显不同化合价的一种盐
2018·广西贺州·中考真题 查看更多[3]
更新时间:2018-08-13 08:46:07
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】“打铁花”是一种民间传统焰火,属于国家级非物质文化遗产。化学兴趣小组的同学利用所学化学知识对“打铁花”进行了探究。
【查阅资料】铁水打花的主要原料为生铁、锯末等。打花者将生铁放到熔炉中加热至熔化,然后用坩埚舀出铁水轻轻抛起,再用木板奋力一击,铁水在空中霎时间分散开来,万千燃烧着的铁屑犹如银珠飞溅,金丝飞驰。
【联想思考】
(1)同学们想到铁丝在氧气中燃烧的实验(如下图),实验现象是剧烈燃烧,火星四射。实验中集气瓶底部预留少量水的原因是_____ 。
同学们产生了疑问:铁丝在空气中不能燃烧,为什么“打铁花”能使铁屑在空气中剧烈燃烧?请你分析原因:_____ 。

【提出问题】“打铁花”溅落下来的黑色物质是什么?
【实验1】
(2)小明和小红分别用两种不同的化学方法,选用不同类型的物质,验证了黑色物质中含有铁屑。
小明的实验方案是:取“打铁花”溅落下来的黑色物质于试管中,加入适量稀硫酸,观察到有气泡产生,该反应的化学方程式为_____ 。
小红的实验方案是:取“打铁花”溅落下来的黑色物质于试管中,_____ (填加入的试剂及实验现象)。
【实验2】
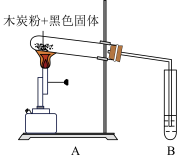
(3)小刚根据铁丝在氧气中燃烧的实验猜测黑色固体中还可能含有四氧化三铁(不考虑氧化亚铁的干扰),并设计图(上图)实验进行验证。B中的试剂是_____ ,该实验的现象是_____ ,证明黑色固体中含有四氧化三铁。木炭粉和四氧化三铁反应说明碳单质具有_____ 性。
【交流讨论】经过本次探究,同学们有了自己的收获,也体会到了中华民族深厚的文化传统。
【查阅资料】铁水打花的主要原料为生铁、锯末等。打花者将生铁放到熔炉中加热至熔化,然后用坩埚舀出铁水轻轻抛起,再用木板奋力一击,铁水在空中霎时间分散开来,万千燃烧着的铁屑犹如银珠飞溅,金丝飞驰。
【联想思考】
(1)同学们想到铁丝在氧气中燃烧的实验(如下图),实验现象是剧烈燃烧,火星四射。实验中集气瓶底部预留少量水的原因是
同学们产生了疑问:铁丝在空气中不能燃烧,为什么“打铁花”能使铁屑在空气中剧烈燃烧?请你分析原因:

【提出问题】“打铁花”溅落下来的黑色物质是什么?
【实验1】
(2)小明和小红分别用两种不同的化学方法,选用不同类型的物质,验证了黑色物质中含有铁屑。
小明的实验方案是:取“打铁花”溅落下来的黑色物质于试管中,加入适量稀硫酸,观察到有气泡产生,该反应的化学方程式为
小红的实验方案是:取“打铁花”溅落下来的黑色物质于试管中,
【实验2】

(3)小刚根据铁丝在氧气中燃烧的实验猜测黑色固体中还可能含有四氧化三铁(不考虑氧化亚铁的干扰),并设计图(上图)实验进行验证。B中的试剂是
【交流讨论】经过本次探究,同学们有了自己的收获,也体会到了中华民族深厚的文化传统。
您最近半年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】将炉甘石(ZnCO3)、赤铜矿(Cu2O)和过量的炭混合后,加热至800 ℃左右,即得金光闪闪的“假黄金”。有同学对“假黄金”的组成进行了以下探究。
[查阅资料]高温时炭可将金属活动顺序表中铝以后的金属氧化物还原成金属单质;ZnCO3高温可分解成金属氧化物。
[提出问题]“假黄金”的化学组成可能是什么?
[猜想]甲同学对该“假黄金”的组成做了以下三种猜想:
猜想①:可能的单质有:C、Zn、Cu
猜想②:可能的氧化物有:ZnO、CuO、Cu2O
猜想③:可能是单质和氧化物组成的混合物
[论证]乙同学经思考和推理后,首先排除了猜想________________ (选填①、②或③),理由是______________ 。进而再排除了猜想__________ (选填①、②或③);对余下的一种猜想,乙同学又排除了其中的一种物质,依据是______________ 。对余下的两种物质,甲和乙同学用实验鉴定该两种物质确实是“假黄金”的成分。
[查阅资料]高温时炭可将金属活动顺序表中铝以后的金属氧化物还原成金属单质;ZnCO3高温可分解成金属氧化物。
[提出问题]“假黄金”的化学组成可能是什么?
[猜想]甲同学对该“假黄金”的组成做了以下三种猜想:
猜想①:可能的单质有:C、Zn、Cu
猜想②:可能的氧化物有:ZnO、CuO、Cu2O
猜想③:可能是单质和氧化物组成的混合物
[论证]乙同学经思考和推理后,首先排除了猜想
您最近半年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】有一包黑色固体可能是炭粉、氧化铜、二氧化锰和铁粉中的两种,为鉴定其成分,某小组同学进行了如下实验:
【查阅资料】:
炭粉常温下与稀酸不反应,氧化铜常温下与稀硫酸反应生成硫酸铜和水,二氧化锰常温下与稀硫酸不反应。
【实验探究】:
(1)取少量固体于表面皿上用磁铁吸引,部分能够被吸,则固体中一定有_____ ;
(2)取少量样品隔绝空气充分加热,冷却后称量,固体质量不变,则该固体中一定没有_____ ;
(3)将样品放入足量稀硫酸中充分反应,有气泡产生并有固体残留,则该固体中可能含有_____ ,生成气体的反应化学方程式为_____ 。
【查阅资料】:
炭粉常温下与稀酸不反应,氧化铜常温下与稀硫酸反应生成硫酸铜和水,二氧化锰常温下与稀硫酸不反应。
【实验探究】:
(1)取少量固体于表面皿上用磁铁吸引,部分能够被吸,则固体中一定有
(2)取少量样品隔绝空气充分加热,冷却后称量,固体质量不变,则该固体中一定没有
(3)将样品放入足量稀硫酸中充分反应,有气泡产生并有固体残留,则该固体中可能含有
您最近半年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】进入冬季,雾霾天气频繁出现。雾是空气中水蒸气凝结的微小水滴大量悬浮在近地面空气中形成的;霾形成的主要原因是工业燃煤、车用燃料不充分燃烧产生的炭粒、碳氢化合物以及建筑尘埃等大量混入空气形成的。同学们收集了少量空气净化器滤芯上的黑色物质,对其成分进行了探究。
【查阅资料】A 碳氢化合物具有可燃性,燃烧生成水和二氧化碳。
B 无水硫酸铜为白色固体,遇水变蓝。
【提出问题】黑色物质中是否含有炭粒和水?
同学们在老师的指导下对其进行探究,下图为探究过程中的部分装置。
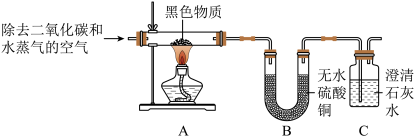
(1)加热前先向 A 中通入除去二氧化碳和水蒸气的空气,这样做的目的是_____ 。
【进行实验】
(2)C 中发生反应的化学方程式为 _____ 。
(3)连接装置的正确顺序如图所示。若先连接 C 再连接 B,会对实验结果产生的影响是_____ 。
【反思与评价】同学们得出黑色固体中含有炭粒的依据是_____ (用化学方程 式表示)。组内成员认为该结论不严谨,他的理由是 _____ 。
【总结提升】雾霾成分复杂,还需进一步学习和研究。请你对治理雾霾提出一点合理化的建议:_____ 。
【查阅资料】A 碳氢化合物具有可燃性,燃烧生成水和二氧化碳。
B 无水硫酸铜为白色固体,遇水变蓝。
【提出问题】黑色物质中是否含有炭粒和水?
同学们在老师的指导下对其进行探究,下图为探究过程中的部分装置。

(1)加热前先向 A 中通入除去二氧化碳和水蒸气的空气,这样做的目的是
【进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| 点燃酒精灯,充分反应 | 观察到的现象是 | 黑色物质中含有炭粒和水 |
(3)连接装置的正确顺序如图所示。若先连接 C 再连接 B,会对实验结果产生的影响是
【反思与评价】同学们得出黑色固体中含有炭粒的依据是
【总结提升】雾霾成分复杂,还需进一步学习和研究。请你对治理雾霾提出一点合理化的建议:
您最近半年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,这引起了同学们的兴趣。难道生成的硫酸铜粉末受热后还能分解?那分解的产物是什么呢?
通过查阅资料,同学们了解到:
1、硫酸铜受热分解生成氧化铜和气体。气体是由SO2、SO3、O2中的一种或几种。受热时温度不同,生成的气体成分也不同。
2、SO2、SO3都能被碱石灰吸收。
3、SO2、SO3都能被氢氧化钠溶液吸收。
【提出猜想】根据质量守恒定律猜测气体的成分:
I.只含_______ 一种;
II.含有SO2、O2二种;
III.含有SO2、SO3、O2三种。
【设计实验】利用下图装置加热硫酸铜粉末直至完全分解
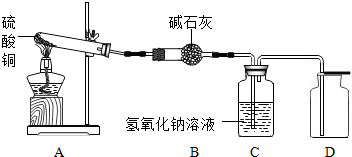
【获取事实】
(1)用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有_______ 。
(2)已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是哪一个?_______
A 3CuSO4 3CuO+SO3↑+2SO2↑+O2↑
3CuO+SO3↑+2SO2↑+O2↑
B 4CuSO4 4CuO+2SO3↑+2SO2↑+O2↑
4CuO+2SO3↑+2SO2↑+O2↑
C 5CuSO4 5CuO+SO3↑+4SO2↑+2O2↑
5CuO+SO3↑+4SO2↑+2O2↑
D 6CuSO4 6CuO+4SO3↑+2SO2↑+O2↑
6CuO+4SO3↑+2SO2↑+O2↑
通过查阅资料,同学们了解到:
1、硫酸铜受热分解生成氧化铜和气体。气体是由SO2、SO3、O2中的一种或几种。受热时温度不同,生成的气体成分也不同。
2、SO2、SO3都能被碱石灰吸收。
3、SO2、SO3都能被氢氧化钠溶液吸收。
【提出猜想】根据质量守恒定律猜测气体的成分:
I.只含
II.含有SO2、O2二种;
III.含有SO2、SO3、O2三种。
【设计实验】利用下图装置加热硫酸铜粉末直至完全分解

【获取事实】
(1)用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有
(2)已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0克 | 75.0克 | 140.0克 |
| 反应后 | 37.0克 | 79.5克 | 140.0克 |
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是哪一个?
A 3CuSO4
 3CuO+SO3↑+2SO2↑+O2↑
3CuO+SO3↑+2SO2↑+O2↑B 4CuSO4
 4CuO+2SO3↑+2SO2↑+O2↑
4CuO+2SO3↑+2SO2↑+O2↑C 5CuSO4
 5CuO+SO3↑+4SO2↑+2O2↑
5CuO+SO3↑+4SO2↑+2O2↑D 6CuSO4
 6CuO+4SO3↑+2SO2↑+O2↑
6CuO+4SO3↑+2SO2↑+O2↑
您最近半年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】如图是实验室制取气体的部分装置,请根据实验装置(部分固定装置已省略)回答问题:
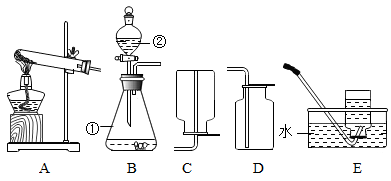
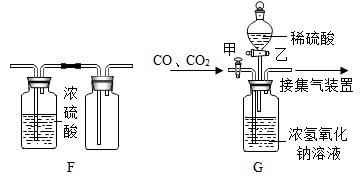
(1)仪器①②名称是:①_______ ,②_______ 。
(2)实验室既可以制取CO2,又可以制取O2的发生和收集装置组合为:____ (在A-E中选)。收集装置的选择是由气体的性质决定的。既能用排水法也能用排空气法收集的气体一定具有的性质有___ (填数字序号)。
①难溶于水 ②易溶于水 ③密度与空气不接近 ④不与水反应
(3)若用F装置收集一瓶干燥的某气体,则该气体可能是_____ (填字母代号)
A.NH3 B.H2 C.O2 D.CH4
(4)工业上常需分离CO2和CO的混合气体,某同学采用装置G也能达到分离该混合气体的目的,操作步骤如下:关闭活塞乙,打开活塞甲,通入混合气体,可收集到____ 气体(填名称),然后____ (填操作),又可收集到另一种气体。
(5)某研究小组对自动充气气球(如下图1所示)进行下列探究,
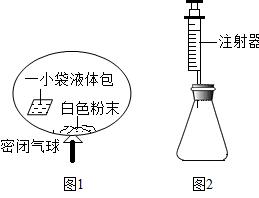
【查阅资料】该气球充气原理是通过挤破气球内液体包使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。为检验气体是二氧化碳,可选用____ (填试剂名称)。
探究一:液体包内溶液酸碱性的探究。
室温时,用pH试纸测得溶液pH=3,则该溶液呈酸性。
探究二:白色粉末成分的探究
【猜想与假设】甲同学认为是碳酸钙:乙同学认为是碳酸钠;丙同学认为是碳酸氢钠
【设计并进行实验】将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想____ (填“正确”或“不正确”)。然后在室温时分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%的盐酸(装置如上图2所示),记录如下:
实验①的化学方程式为_______ 表中X=_______ g;V1=_______ (填“>”“<”或“=”)V2。
【实验结论】根据表中CO2体积与锥形瓶内物质质量的关系,得出的结论及判断依据是____ 。


(1)仪器①②名称是:①
(2)实验室既可以制取CO2,又可以制取O2的发生和收集装置组合为:
①难溶于水 ②易溶于水 ③密度与空气不接近 ④不与水反应
(3)若用F装置收集一瓶干燥的某气体,则该气体可能是
A.NH3 B.H2 C.O2 D.CH4
(4)工业上常需分离CO2和CO的混合气体,某同学采用装置G也能达到分离该混合气体的目的,操作步骤如下:关闭活塞乙,打开活塞甲,通入混合气体,可收集到
(5)某研究小组对自动充气气球(如下图1所示)进行下列探究,

【查阅资料】该气球充气原理是通过挤破气球内液体包使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。为检验气体是二氧化碳,可选用
探究一:液体包内溶液酸碱性的探究。
室温时,用pH试纸测得溶液pH=3,则该溶液呈酸性。
探究二:白色粉末成分的探究
【猜想与假设】甲同学认为是碳酸钙:乙同学认为是碳酸钠;丙同学认为是碳酸氢钠
【设计并进行实验】将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想
| 实验编号 | 锥形瓶内物质 | 最终得到CO2的体积/mL | |
| 物质 | 质量/g | 0 | |
| ① | 碳酸氢钠 | 0.10 | V1 |
| ② | 碳酸钠 | 0.10 | V2 |
| ③ | 白色粉末 | X | V1 |
实验①的化学方程式为
【实验结论】根据表中CO2体积与锥形瓶内物质质量的关系,得出的结论及判断依据是
您最近半年使用:0次



