氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程:
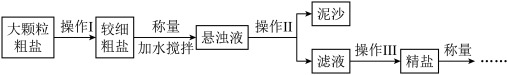
(1)操作Ⅰ是将粗盐研碎,这样做的目的是____________ 。
(2)实验过程中,多次用到玻璃棒。请你写出操作Ⅲ中玻璃棒的作用:___________ 。
(3)如果过滤后的滤液仍浑浊,其原因可能是________ (写出一条)。
(4)蒸发操作中除用到三脚架、酒精灯、玻璃棒、坩埚钳外,还需要用到_________ 等仪器。
(5)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是_________ (填序号)。
A.食盐没有全部溶解即过滤 B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿 D.器皿上沾有的精盐没全部转移到称量纸上

(1)操作Ⅰ是将粗盐研碎,这样做的目的是
(2)实验过程中,多次用到玻璃棒。请你写出操作Ⅲ中玻璃棒的作用:
(3)如果过滤后的滤液仍浑浊,其原因可能是
(4)蒸发操作中除用到三脚架、酒精灯、玻璃棒、坩埚钳外,还需要用到
(5)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是
A.食盐没有全部溶解即过滤 B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿 D.器皿上沾有的精盐没全部转移到称量纸上
更新时间:2019-03-23 19:38:40
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
【推荐1】为除去氯化钾固体中混有的少量氯化钙和硫酸钾杂质,现做如下实验。
步骤:①取固体于试管中,并加足量水溶解,得无色溶液;
②向上述溶液中加入过量a溶液,充分反应后,再加入过量b溶液,充分振荡
③过滤,向滤液中滴加适量c溶液,充分反应后,蒸发、结晶,即得纯净的氯化钾
请回答:加入过量b溶液的目的是_______________ ;c为___________ (填化学式)。
步骤:①取固体于试管中,并加足量水溶解,得无色溶液;
②向上述溶液中加入过量a溶液,充分反应后,再加入过量b溶液,充分振荡
③过滤,向滤液中滴加适量c溶液,充分反应后,蒸发、结晶,即得纯净的氯化钾
请回答:加入过量b溶液的目的是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】实验室的废水中含有氯化钠、氯化镁和氯化钙,为了处理废水并回收氯化钠固体,某同学设计了以下方案,请根据流程图回答问题。
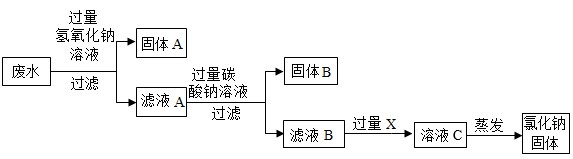
(1)写出在废水中加入过量氢氧化钠溶液时发生反应的化学方程式。__________
(2)写出滤液B中含有的溶质。__________
(3)请写出试剂X的名称__________ 。

(1)写出在废水中加入过量氢氧化钠溶液时发生反应的化学方程式。
(2)写出滤液B中含有的溶质。
(3)请写出试剂X的名称
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】2021年6月8日是第13个“世界海洋日”。烟台有漫长的海岸线,蕴藏着丰富的海洋资源。某兴趣小组设计的综合利用海水的部分流程图如图。据如图回答:

(1)海水制镁:步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式为___________ 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是___________ 。
(2)海水晒盐:
①利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是___________ (填字母序号)。
A.在蒸发池中水蒸发所需能量主要为太阳能和风能
B.在结晶池中主要通过降温结晶使氯化钠析出
C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液
②粗盐中常含有泥沙等难溶性杂质。在实验室中除去粗盐中的难溶性杂质,可依次通过___________ 、过滤、蒸发结晶等操作。蒸发结晶操作中要用到玻璃棒,其作用是___________ 。通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是___________ 。
(3)海水制碱:步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向NaCl饱和溶液中先后加入的两种物质分别是___________ (写化学式)。步骤⑨中发生反应的化学方程式是___________ 。
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是___________ 。
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是___________ 。

(1)海水制镁:步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式为
(2)海水晒盐:
①利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是
A.在蒸发池中水蒸发所需能量主要为太阳能和风能
B.在结晶池中主要通过降温结晶使氯化钠析出
C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液
②粗盐中常含有泥沙等难溶性杂质。在实验室中除去粗盐中的难溶性杂质,可依次通过
(3)海水制碱:步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向NaCl饱和溶液中先后加入的两种物质分别是
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】兴趣小组的同学在实验室进行粗盐(只含有难溶性杂质)提纯的实验。回答下列问题:_________ (填数字序号,下同),正确的实验步骤是___________ 。
(2)操作④中,玻璃棒的作用是___________ ,当观察到蒸发皿中___________ 时,停止加热。

(2)操作④中,玻璃棒的作用是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】MnO2是一种重要的无机功能材料。已知粗MnO2中含有少量MnCO3,某化学兴趣小组在实验室中模拟提纯粗MnO2的工业流程(如下图所示)。

(1)操作A和操作B的名称是_____________
(2)蒸发所需的仪器有铁架台(带铁圈)、蒸发皿、酒精灯和_____________
(3)写出加稀H2SO4时产生CO2的化学方程式_____________
(4)该流程中可以循环利用的物质是H2SO4和_____________
(5)最终所得的MnO2质量____________

(1)操作A和操作B的名称是
(2)蒸发所需的仪器有铁架台(带铁圈)、蒸发皿、酒精灯和
(3)写出加稀H2SO4时产生CO2的化学方程式
(4)该流程中可以循环利用的物质是H2SO4和
(5)最终所得的MnO2质量
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】结合《粗盐中难溶性杂质的去除》实验活动,回答问题。
(1)粗盐的溶解:粗盐的溶解操作中,用玻璃棒搅拌的主要原因是___________ ;
(2)过滤:过滤后,从外观上看更加澄清的是___________ (选填“过滤前的液体”或“滤液”);
(3)蒸发:将滤液倒入蒸发皿时不小心洒出少许,滤液蒸发操作中,当观察到___________ 现象时,就可以停止加热;
(4)计算产率:按上述操作,精盐的产率比理论值___________ (选填“偏大”、“偏小”或“不变”)。
(1)粗盐的溶解:粗盐的溶解操作中,用玻璃棒搅拌的主要原因是
(2)过滤:过滤后,从外观上看更加澄清的是
(3)蒸发:将滤液倒入蒸发皿时不小心洒出少许,滤液蒸发操作中,当观察到
(4)计算产率:按上述操作,精盐的产率比理论值
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】从硝酸钾和氯化钠(少量)的混合溶液中提纯硝酸钾的一系列操作包括“加热蒸发浓缩、再冷却到一定温度、过滤”等步骤。
(1)请利用上表给出的硝酸钾的溶解度数据,在答题卡的坐标图中绘制硝酸钾的溶解度曲线___________ 。

(2) “加热蒸发浓缩”操作时所用到的仪器除铁架台、石棉网、坩埚钳外,还需要___________ 。
(3) “冷却到一定温度”能获得较纯净的硝酸钾晶体的原因是___________ 。
(4)30℃时,硝酸钾饱和溶液的溶质质量分数的计算公式为___________ 。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 |
| 硝酸钾溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |

(2) “加热蒸发浓缩”操作时所用到的仪器除铁架台、石棉网、坩埚钳外,还需要
(3) “冷却到一定温度”能获得较纯净的硝酸钾晶体的原因是
(4)30℃时,硝酸钾饱和溶液的溶质质量分数的计算公式为
您最近一年使用:0次
【推荐2】下图是进行有关化学实验的装置或操作。______ 时停止加热。
(2)实验二中观察到高锰酸钾几乎不溶于汽油,碘却可以溶解在汽油中。由此现象可得出的实验结论是______ 。
(3)实验三是“测定空气里氧气的含量”实验。若实验中氧气含量测定结果偏小,其原因可能是______ (写一点即可)。

(2)实验二中观察到高锰酸钾几乎不溶于汽油,碘却可以溶解在汽油中。由此现象可得出的实验结论是
(3)实验三是“测定空气里氧气的含量”实验。若实验中氧气含量测定结果偏小,其原因可能是
您最近一年使用:0次



