阅读下面的科普短文。
中国有很长的饮茶历史,茶叶中含有茶多酚等物质。
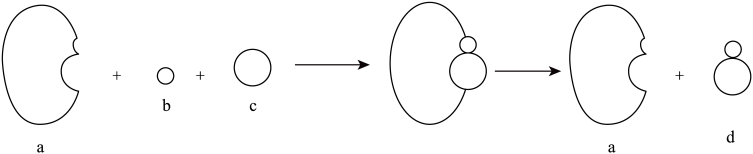
茶多酚是从天然茶叶中提取的混合物,由儿茶素、黄酮苷类、酚酸等组成,是一种白色粉末,略有吸水性。易溶于温水、乙醇等,在碱性环境中不稳定。茶多酚容易被氧化变色,下图是多酚氧化酶催化茶多酚氧化的示意图(图中a、b、c、d分别代表4种物质)。
研究发现,茶多酚是茶叶发挥健康保健功效最主要的物质,最典型的代表是儿茶素,具有抗氧化(消除氧自由基)、抗炎、降低心血管病发病几率、预防癌症、降血脂、减少体脂形成、抗菌、改变肠道菌群生态等多项功效。研究表明,喝下一杯茶半小时后,血中的抗氧化容量(对抗氧自由基的能力)增加41%﹣48%,并能在高水平状态持续一个半小时。
茶多酚还可用于食品保鲜防腐,根据我国《食品添加剂使用卫生标准》规定茶多酚的使用范围和使用量如下:
溶剂法是从茶叶中提取茶多酚的传统方法之一,利用茶多酚和茶叶中其他成分在乙醇中的溶解度不同进行分离。具体的方法是将茶叶用乙醇浸渍,然后把浸取液进行液﹣液分离,最后浓缩得到产品。
依据文章内容回答下列问题。
(1)根据以上描述请你归纳茶多酚的物理性质有_________________ 。
(2)多酚氧化酶催化茶多酚氧化的过程中,其中代表酶的是_________________
A a B b C c D d
(3)若一包方便面的质量是100g,则最多加入茶多酚保鲜剂_________________ mg。
(4)下列关于茶多酚的说法中,正确的是_________________
A 茶多酚在碱性环境中不稳定
B 适量喝茶有益身体健康
C 利用溶剂法提取茶多酚属于化学变化
D 某同学在中午12点喝了一杯茶,他血中的抗氧化容量的较高水平可持续到14点
(5)保存茶多酚晶体时应注意_________________ 。
中国有很长的饮茶历史,茶叶中含有茶多酚等物质。
茶多酚是从天然茶叶中提取的混合物,由儿茶素、黄酮苷类、酚酸等组成,是一种白色粉末,略有吸水性。易溶于温水、乙醇等,在碱性环境中不稳定。茶多酚容易被氧化变色,下图是多酚氧化酶催化茶多酚氧化的示意图(图中a、b、c、d分别代表4种物质)。

研究发现,茶多酚是茶叶发挥健康保健功效最主要的物质,最典型的代表是儿茶素,具有抗氧化(消除氧自由基)、抗炎、降低心血管病发病几率、预防癌症、降血脂、减少体脂形成、抗菌、改变肠道菌群生态等多项功效。研究表明,喝下一杯茶半小时后,血中的抗氧化容量(对抗氧自由基的能力)增加41%﹣48%,并能在高水平状态持续一个半小时。
茶多酚还可用于食品保鲜防腐,根据我国《食品添加剂使用卫生标准》规定茶多酚的使用范围和使用量如下:
食物 | 不含水的脂肪和油 | 熟坚果 | 油炸面制品 | 燕麦片 | 方便面 |
含量(g/kg) | 0.4 | 0.2 | 0.2 | 0.2 | 0.2 |
依据文章内容回答下列问题。
(1)根据以上描述请你归纳茶多酚的物理性质有
(2)多酚氧化酶催化茶多酚氧化的过程中,其中代表酶的是
A a B b C c D d
(3)若一包方便面的质量是100g,则最多加入茶多酚保鲜剂
(4)下列关于茶多酚的说法中,正确的是
A 茶多酚在碱性环境中不稳定
B 适量喝茶有益身体健康
C 利用溶剂法提取茶多酚属于化学变化
D 某同学在中午12点喝了一杯茶,他血中的抗氧化容量的较高水平可持续到14点
(5)保存茶多酚晶体时应注意
更新时间:2019-04-05 22:39:17
|
相似题推荐
填空与简答-填空题
|
较易
(0.85)
名校
解题方法
【推荐1】污水的处理不仅可以提高水资源的利用率,而且能恢复城市及河流良好的水域环境,以下是生活污水部分处理过程,分析流程,回答问题:
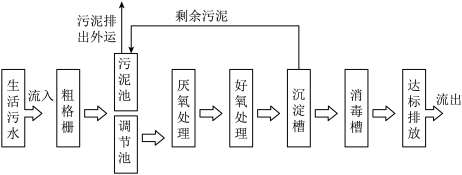
(1)粗格栅可除去不溶于水中的大颗粒杂质,相当于实验室中的______________ 装置。
(2)“好氧处理”需通入氧气,并利用氧气搅拌,这与_______ (填一种仪器)的作用相似。
(3)向“消毒槽”通臭氧(O3)来消毒杀菌,这是利用其_________ (填“物理”或“化学”)性质。O2在紫外线照射下可以转化 O3,其符号表达式为__________________ ,反应的微观实质为____________________ 。
(4)上述流程中需要加入絮凝剂的装置是_____________ 。
(5)生活污水处理达标后排放的意义有____________ (合理即可)。

(1)粗格栅可除去不溶于水中的大颗粒杂质,相当于实验室中的
(2)“好氧处理”需通入氧气,并利用氧气搅拌,这与
(3)向“消毒槽”通臭氧(O3)来消毒杀菌,这是利用其
(4)上述流程中需要加入絮凝剂的装置是
(5)生活污水处理达标后排放的意义有
您最近一年使用:0次
填空与简答-科普阅读题
|
较易
(0.85)
名校
解题方法
【推荐2】认真阅读下列材料,回答有关问题。
二氧化锰,是一种无机化合物,为黑色无定形粉末或黑色斜方晶体。其熔点:535℃密度:5.03g/cm3,难溶于水,在加热情况下溶于浓盐酸而产生氯气。二氧化锰在工业和实验室的应用很广泛,例如:用作干电池去极剂,合成工业的催化剂和氧化剂,玻璃工业和搪瓷工业的着色剂、消色剂、脱铁剂等。用于制造金属锰、特种合金、锰铁铸件、防毒面具和电子材料铁氧体等。另外,还可用于橡胶工业以增加橡胶的粘性。
(1)请写出二氧化锰的化学式_______ 。
(2)二氧化锰的物理性质为_______ (任写一条即可);
(3)实验室用作过氧化氢溶液分解制取氧气时,通常会放入少量二氧化锰。二氧化锰在这一反应中是_______ 剂。
二氧化锰,是一种无机化合物,为黑色无定形粉末或黑色斜方晶体。其熔点:535℃密度:5.03g/cm3,难溶于水,在加热情况下溶于浓盐酸而产生氯气。二氧化锰在工业和实验室的应用很广泛,例如:用作干电池去极剂,合成工业的催化剂和氧化剂,玻璃工业和搪瓷工业的着色剂、消色剂、脱铁剂等。用于制造金属锰、特种合金、锰铁铸件、防毒面具和电子材料铁氧体等。另外,还可用于橡胶工业以增加橡胶的粘性。
(1)请写出二氧化锰的化学式
(2)二氧化锰的物理性质为
(3)实验室用作过氧化氢溶液分解制取氧气时,通常会放入少量二氧化锰。二氧化锰在这一反应中是
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐3】自来水是我国目前主要的生活饮用水,下面是我国颁布的生活饮用水水质标准的部分内容。
项目 标准:①感官指标 :无异味、臭味等;②化学指标 pH 6.5~8.5,铜<1.0 m9•L-1,铁<0.3 mg•L-1,氟化物<1.0 mg•L-1,游离氯≥0.3 mg•L-1等
(1)感官指标表现的是自来水的______________________ 性质(填“物理”或“化学”),若水中有异味可以用_______________ (填物质名称)除去。
(2)自来水属于___________ (填“纯净物”或“混合物”);自来水中的游离氯有少量可转变成氯离子,氯离子的符号是___________ 。
(3)实验室用自来水制取纯净水的方法是________。
(4)长期饮用蒸馏水________ (填“利于”或“不利于”)人体健康。
项目 标准:①感官指标 :无异味、臭味等;②化学指标 pH 6.5~8.5,铜<1.0 m9•L-1,铁<0.3 mg•L-1,氟化物<1.0 mg•L-1,游离氯≥0.3 mg•L-1等
(1)感官指标表现的是自来水的
(2)自来水属于
(3)实验室用自来水制取纯净水的方法是________。
| A.吸附 | B.沉淀 | C.过滤 | D.蒸馏 |
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】工业上制取氧气是利用氮气和氧气的_____ 不同,先后从空气中分离出来,是一个______ 变化。
您最近一年使用:0次
填空与简答-流程题
|
较易
(0.85)
解题方法
【推荐2】小伟收集到一瓶浑浊的沂河水,他要模拟自来水厂的净水过程,最终制成自来水。其实验过程如下所示。请回答以下问题。
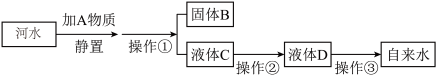
(1)操作①的名称是___________ 。
(2)操作②主要是除去一些异味和色素,选用的物质是活性炭,其作用是___________ ,该过程主要是___________ 变化(填“物理”或“化学”)。
(3)小刚发现经净化后的液体D是硬水,日常生活中常用___________ 的方法使其软化后使用。操作③是消毒杀菌,该过程主要是___________ 变化(填“物理”或“化学”)。

(1)操作①的名称是
(2)操作②主要是除去一些异味和色素,选用的物质是活性炭,其作用是
(3)小刚发现经净化后的液体D是硬水,日常生活中常用
您最近一年使用:0次
填空与简答-简答题
|
较易
(0.85)
【推荐3】如图A是液态水加热变成气态水蒸气的示意图,图B是水通电分解生成氢气和氧气的示意图。请据图回答。

(1)液态水变为气态水时_____ 发生了变化,但_____ 没有发生变化,故上述变化属于_____ (选填“物理”或“化学”)变化。
(2)水通电分解时水分子本身_____ (选填“发生”或“不发生”)变化。故水通电的变化属于_____ (选填“物理”或“化学”)变化;(b)中所得粒子_____ (选填“能”或“不能”)保持水的化学性质。
(3)图B中所得物质(b)属于_____ (选填“纯净物”或“混合物”),理由是_____ ;所得物质(d)属于_____ (选填“纯净物”或“混合物”),理由是_____ 。

(1)液态水变为气态水时
(2)水通电分解时水分子本身
(3)图B中所得物质(b)属于
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】钙是人体内含量最高的金属元素,是构成人体的重要组分。成人体内约含钙1.2kg,其中99%存在于骨骼和牙齿中,主要以羟基磷酸钙[Ca10(PO4)6(OH)2]晶体的形式存在,它使得骨骼和牙齿具有坚硬的结构支架。

(1)羟基磷酸钙[Ca10(PO4)6(OH)2]的组成元素有________ 种。
(2)羟基磷酸钙中钙元素与磷元素的质量比为___ 。
(3)如图是某品牌钙片的部分说明,按说明服用每天可为人体, XX钙片补钙多少g?

(1)羟基磷酸钙[Ca10(PO4)6(OH)2]的组成元素有
(2)羟基磷酸钙中钙元素与磷元素的质量比为
(3)如图是某品牌钙片的部分说明,按说明服用每天可为人体, XX钙片补钙多少g?
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】钙是人体必需元素。
(1)牛奶等食物含钙丰富,这里的“钙”指的是______ (填“单质”、“元素”或“原子”)。
(2)青少年缺钙会影响身高,可服用补钙剂。某钙片的标签如图所示。
①按标签用量服用钙片,每天能补充钙元素______ g。
②钙片中的碳酸钙与胃酸(含有 HCl)反应后钙才能被吸收。该反应的化学方程式为______ 。
(1)牛奶等食物含钙丰富,这里的“钙”指的是
(2)青少年缺钙会影响身高,可服用补钙剂。某钙片的标签如图所示。
| 主要成分:碳酸钙(CaCO3) 规格:2g/片 每片中含:碳酸钙75% 食用方法:嚼食,每日一片 |
②钙片中的碳酸钙与胃酸(含有 HCl)反应后钙才能被吸收。该反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较易
(0.85)
【推荐3】过氧化钙微溶于水,溶于酸,可用作分析试剂、医用防腐剂、消毒剂。以下是一种制备过氧化钙晶体(CaO2·8H2O)的实验方法。回答下列问题:
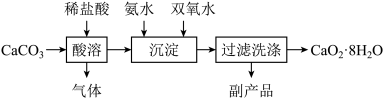
(1)标出碳酸钙中钙元素化合价______ ,酸溶过程中反应的符号表达式为______ 。
(2)沉淀池中的化学反应需要在冰水中进行,原因有______ (任答一点)。副产品为氯化铵,铵根离子的符号为______ 。
(3)过滤所需要的玻璃仪器有烧杯、玻璃棒、______ ,玻璃棒的作用是______ 。
(4)碳酸钙可以作为补钙剂,钙______ (填“是”或“不是”)人体所需的微量元素,儿童缺钙易患有______ 病。(填字母)
a.贫血症 b.侏儒症 c.佝偻病 d.甲状腺疾病
(5)CaO2加热至315°C时会分解生成一种氧化物和一种气体,其符号表达式为______ 。
(6)已知CaO2·8H2O的相对分子质量为216,现测得该所制得的过氧化钙晶体中,CaO2·8H2O的质量分数为86.4%(产品中其它成分不含钙元素),则该晶体中钙元素的质量分数为______ (写出解题过程)。

(1)标出碳酸钙中钙元素化合价
(2)沉淀池中的化学反应需要在冰水中进行,原因有
(3)过滤所需要的玻璃仪器有烧杯、玻璃棒、
(4)碳酸钙可以作为补钙剂,钙
a.贫血症 b.侏儒症 c.佝偻病 d.甲状腺疾病
(5)CaO2加热至315°C时会分解生成一种氧化物和一种气体,其符号表达式为
(6)已知CaO2·8H2O的相对分子质量为216,现测得该所制得的过氧化钙晶体中,CaO2·8H2O的质量分数为86.4%(产品中其它成分不含钙元素),则该晶体中钙元素的质量分数为
您最近一年使用:0次



