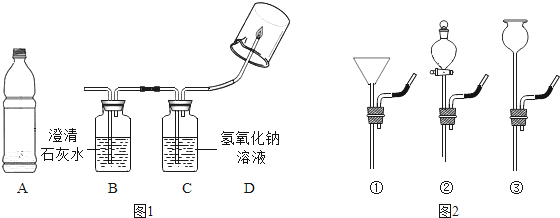
小华同学用排水法收集了一大瓶沼气池中气体(图1中的A),为了弄清它的成分,进行了有关实验.请你与他一起完成以下探究活动:
【对气体猜想】
猜想I:全部是CH4;
猜想Ⅱ:全部是CO;
猜想Ⅲ:是CO和CO2的混合气体;
猜想Ⅳ:是CH4和CO2的混合气体.
【实验和推断】将A中的气体依次通入B、C中,在D处点燃.
(1)要将A中的气体通入后面的装置中,应选图2中的_____ (填序号)“注水装置”.
(2)若B中石灰水变浑浊,则说明A中的气体中含有_____ 气体.
(3)装置C作用是_____ .
(4)若D处倒扣的是涂有澄清石灰水的烧杯,出现浑浊,且B中无明显现象,则“猜想_____ ”可能成立;若D处倒扣的是干冷的大烧杯,杯壁有水雾出现,有同学认为“猜想I、Ⅳ”可能成立,另有同学认为此现象不能证明收集到的气体中一定含有CH4,理由是_____ ;要排除这种干扰可采取的措施是_____ .
(5)采取(4)中的排除干扰措施后:若D处分别倒扣干冷的烧杯和涂石灰水的烧杯,分别出现水雾和浑浊,且B中也出现浑浊,则证明“猜想_____ ”成立.

【对气体猜想】
猜想I:全部是CH4;
猜想Ⅱ:全部是CO;
猜想Ⅲ:是CO和CO2的混合气体;
猜想Ⅳ:是CH4和CO2的混合气体.
【实验和推断】将A中的气体依次通入B、C中,在D处点燃.
(1)要将A中的气体通入后面的装置中,应选图2中的
(2)若B中石灰水变浑浊,则说明A中的气体中含有
(3)装置C作用是
(4)若D处倒扣的是涂有澄清石灰水的烧杯,出现浑浊,且B中无明显现象,则“猜想
(5)采取(4)中的排除干扰措施后:若D处分别倒扣干冷的烧杯和涂石灰水的烧杯,分别出现水雾和浑浊,且B中也出现浑浊,则证明“猜想
18-19九年级上·辽宁大连·阶段练习 查看更多[2]
更新时间:2019-04-17 16:32:27
|
相似题推荐
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐1】某化学兴趣小组的同学们在实验室用石灰石和稀盐酸制取二氧化碳,并对反应后所得溶液的溶质成分进行探究。
I.实验室制取二氧化碳的反应原理及装置
(1)写出石灰石与稀盐酸制二氧化碳的化学方程式_____ 。
(2)同学们从下图装置中选择合适的装置组合制取二氧化碳。
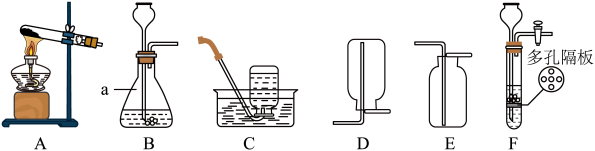
其中仪器a的名称为_____ ,从A-E中可选择的发生装置和收集装置的组合是______ (填序号),F装置的优点是________ 。
II.同学们对反应后所得溶液的溶质成分进行了以下探究。
【提出问题】实验室制取二氧化碳后,所得溶液的溶质成分是什么?
【猜想与假设】
猜想一:CaCl2
猜想二:CaCl2和CaCO3
猜想三:CaCl2和_____ (写化学式)
【理论分析】小华认为上述猜想中猜想______ 肯定不成立,理由是_____ 。
【查阅资料】CaCl2溶液呈中性。
【进行实验】同学们进行了如下实验。
【反思与评价】
反应后所得溶液的成分,主要考虑两个方面,一是生成物,二是_______________ 。
I.实验室制取二氧化碳的反应原理及装置
(1)写出石灰石与稀盐酸制二氧化碳的化学方程式
(2)同学们从下图装置中选择合适的装置组合制取二氧化碳。

其中仪器a的名称为
II.同学们对反应后所得溶液的溶质成分进行了以下探究。
【提出问题】实验室制取二氧化碳后,所得溶液的溶质成分是什么?
【猜想与假设】
猜想一:CaCl2
猜想二:CaCl2和CaCO3
猜想三:CaCl2和
【理论分析】小华认为上述猜想中猜想
【查阅资料】CaCl2溶液呈中性。
【进行实验】同学们进行了如下实验。
| 实验操作 | 实验现象与分析 | 实验结论 |
| 1.小明取反应后的上层清液,滴加 | 溶液由无色变成红色 | 猜想三正确 |
| 2.小红取反应后的上层清液,加入少量镁条 | 观察到 | |
| 3.小刚取反应后的上层清液,加入氧化铁粉末 | 固体逐渐减少,溶液变成 化学方程式为 |
反应后所得溶液的成分,主要考虑两个方面,一是生成物,二是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】某化学兴趣小组用石灰石和盐酸制取一瓶CO2,验满后,将澄清石灰水倒入集气瓶中,发现没有变浑浊,兴趣小组对这个异常现象进行了探究。
【提出问题】澄清石灰水为什么没有变浑浊?
【查阅资料】(1)CO2过量时,CaCO3沉淀会转化为可溶于水的Ca(HCO3)2
(2)AgCl不溶于稀硝酸。
【提出猜想】Ⅰ.石灰水已完全变质 Ⅱ.______________ Ⅲ.CO2中混有HCl
【实验方案】兴趣小组用原药品继续制备CO2,并进行探究。
【实验结论】制取的CO2气体中混入了HCl,所以澄清石灰水没有变浑浊。
【交流讨论】若要收集到纯净、干燥的CO2,需将混合气体依次通入________ 和__________
【拓展思考】回忆课本中收集呼出气体的操作后,同学们尝试用排水法收集一瓶CO2,倒入澄清石灰水后,石灰水变浑浊。你认为该实验成功的原因是___________ (写一点)。
【提出问题】澄清石灰水为什么没有变浑浊?
【查阅资料】(1)CO2过量时,CaCO3沉淀会转化为可溶于水的Ca(HCO3)2
(2)AgCl不溶于稀硝酸。
【提出猜想】Ⅰ.石灰水已完全变质 Ⅱ.
【实验方案】兴趣小组用原药品继续制备CO2,并进行探究。
| 步骤 | 实验操作 | 实验现象 | 结论 |
| (1) | 取少量澄清石灰水于试管中,加入 | 生成白色沉淀 | 猜想Ⅰ不成立 |
| (2) | 将少量气体通入盛有澄清石灰水的试管中 | 猜想Ⅱ不成立 | |
| (3) | 将气体通入盛有 | 猜想Ⅲ成立 |
【实验结论】制取的CO2气体中混入了HCl,所以澄清石灰水没有变浑浊。
【交流讨论】若要收集到纯净、干燥的CO2,需将混合气体依次通入
【拓展思考】回忆课本中收集呼出气体的操作后,同学们尝试用排水法收集一瓶CO2,倒入澄清石灰水后,石灰水变浑浊。你认为该实验成功的原因是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐3】某化学兴趣小组对某品牌牙膏中碳酸钙含量进行以下探究。该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成(假设其他成分与盐酸无反应)。现利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定B中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。请回答下列问题。
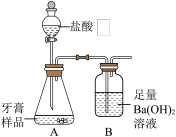
(1)若测定值比实际值小,可能的原因有______ 。(填数字序号)
①装置A中水蒸气、HCl等进入装置B中
②装置A中CO2未完全进入装置B
③CO2气流速度太快导致Ba(OH)2未完全吸收
④盐酸未滴加过量
(2)为防止HCl进入B装置,可在A、B之间增加装有______ (填药品名称或化学式)溶液的洗气瓶。
(3)实验中,有时在装置B中的长导管下方增加一个带孔球泡,这样做可以提高_____ 。
(4)为了减少实验误差,你还可以采取一项措施____________ 。
(5)准确称取三份质量均为8.00g的样品,进行了三次测定,测得BaCO3平均质量为3.94 g。则样品中碳酸钙的质量分数为________________ 。

(1)若测定值比实际值小,可能的原因有
①装置A中水蒸气、HCl等进入装置B中
②装置A中CO2未完全进入装置B
③CO2气流速度太快导致Ba(OH)2未完全吸收
④盐酸未滴加过量
(2)为防止HCl进入B装置,可在A、B之间增加装有
(3)实验中,有时在装置B中的长导管下方增加一个带孔球泡,这样做可以提高
(4)为了减少实验误差,你还可以采取一项措施
(5)准确称取三份质量均为8.00g的样品,进行了三次测定,测得BaCO3平均质量为3.94 g。则样品中碳酸钙的质量分数为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐1】某燃料气体成分可能含有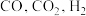 和
和 等,某化学兴趣小组的同学对该燃料气体样品的成分进行了如下探究:
等,某化学兴趣小组的同学对该燃料气体样品的成分进行了如下探究:
【猜想】①该混合气体只含 有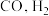 ②该混合气体含有
②该混合气体含有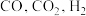 和
和
③该混合气体只含有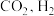 和
和 ④该混合气体只含有
④该混合气体只含有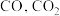 和
和
……
【实验】同学们在老师的指导下设计了如下图所示装置,并进行了实验。提示:每个装置中的药品都足量。白色无水硫酸铜固体遇到水会变蓝色

(1)装置A中无水硫酸铜变蓝,B中澄清石灰水变浑浊,B中发生的化学反应方程式为___________ 。结论:猜想中不符合的为_______________ (填猜想中的序号)。
(2)装置C和D的设计有错误地方,如何改进_______________
(3)实验结束后,同学们一致认为猜想③正确。
其中同学们在装置F中加入了无水硫酸铜,你认为在装置G中所加药品最好为_______________ ,他们所依据的实验现象分别为:E中_______________ ,F中_______________ ,G中___________
(4)实验后,有同学对装置A中所得蓝色固体感兴趣,并对其进行实验探究。
10g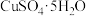 样品受热脱水过程的热重曲线(固体质量随温度变化的曲线)如下图所示。
样品受热脱水过程的热重曲线(固体质量随温度变化的曲线)如下图所示。
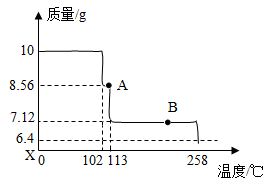
请回答下列问题:
①试确定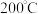 时固体物质的化学式
时固体物质的化学式__________ 。(写出解题过程)
②取 所得的样品,于
所得的样品,于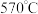 下灼烧得到的主要产物是黑色粉末和一种氧化物气体,该反应的化学方程式为
下灼烧得到的主要产物是黑色粉末和一种氧化物气体,该反应的化学方程式为____________ 。
③把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体(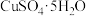 )析出,其晶体存在的最高温度是
)析出,其晶体存在的最高温度是__________________ 。
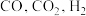 和
和 等,某化学兴趣小组的同学对该燃料气体样品的成分进行了如下探究:
等,某化学兴趣小组的同学对该燃料气体样品的成分进行了如下探究:【猜想】①该混合气体只含 有
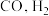 ②该混合气体含有
②该混合气体含有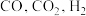 和
和
③该混合气体只含有
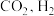 和
和 ④该混合气体只含有
④该混合气体只含有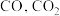 和
和
……
【实验】同学们在老师的指导下设计了如下图所示装置,并进行了实验。提示:每个装置中的药品都足量。白色无水硫酸铜固体遇到水会变蓝色

(1)装置A中无水硫酸铜变蓝,B中澄清石灰水变浑浊,B中发生的化学反应方程式为
(2)装置C和D的设计有错误地方,如何改进
(3)实验结束后,同学们一致认为猜想③正确。
其中同学们在装置F中加入了无水硫酸铜,你认为在装置G中所加药品最好为
(4)实验后,有同学对装置A中所得蓝色固体感兴趣,并对其进行实验探究。
10g
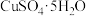 样品受热脱水过程的热重曲线(固体质量随温度变化的曲线)如下图所示。
样品受热脱水过程的热重曲线(固体质量随温度变化的曲线)如下图所示。
请回答下列问题:
①试确定
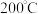 时固体物质的化学式
时固体物质的化学式②取
 所得的样品,于
所得的样品,于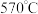 下灼烧得到的主要产物是黑色粉末和一种氧化物气体,该反应的化学方程式为
下灼烧得到的主要产物是黑色粉末和一种氧化物气体,该反应的化学方程式为③把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体(
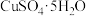 )析出,其晶体存在的最高温度是
)析出,其晶体存在的最高温度是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】某化学兴趣小组同学,在学习了化石燃料后,对天然气的主要成分甲烷,燃烧后得到的气体是什么产生了兴趣,他们收集了一些甲烷燃烧后的气体,请你参与探究并回答下列问题。
【查阅资料】
甲烷充分燃烧的化学方程式为_____ ;也可能不充分燃烧生成CO。
白色无水硫酸铜粉末遇水变蓝色;浓硫酸可以吸收水分,做干燥剂。
甲烷也具有还原性,在高温下可以与铁、铜等的金属氧化物反应生成对应金属单质和二氧化碳、水。
【提出问题】
甲烷燃烧后得到的气体中有哪些成分?
【猜想假设】
猜想I:CO;
猜想Ⅱ:CO2;
猜想Ⅲ:CO2、CO
【实验设计】
将甲烷燃烧的产物依次通过A-E装置进行实验:

观察到的实验现象如下:
(1)A中澄清石灰水变浑浊,相关反应方程式为_____ :
(2)C中_____ ;
(3)D中澄清石灰水变浑浊。
【实验结论】
根据以上实验现象可推断出猜想Ⅲ成立。
【反思交流】
有同学认为实验设计不合理,因为可能会有没烧完的甲烷对实验产生干扰。同学们经过讨论,在原有实验装置的基础上进行了改进:在B、C装置之间添加一个_____ (填字母序号,下同)装置,在C、D装置之间添加一个_____ 装置。

重新实验后,两个新加的装置都无明显现象,其他装置的现象与上次实验相同。充分证明猜想Ⅲ成立。
【拓展延伸】
在装置末端“?”处应连接(放置)一个_____ 进行尾气处理,处理尾气的原因是_____ 。
【查阅资料】
甲烷充分燃烧的化学方程式为
白色无水硫酸铜粉末遇水变蓝色;浓硫酸可以吸收水分,做干燥剂。
甲烷也具有还原性,在高温下可以与铁、铜等的金属氧化物反应生成对应金属单质和二氧化碳、水。
【提出问题】
甲烷燃烧后得到的气体中有哪些成分?
【猜想假设】
猜想I:CO;
猜想Ⅱ:CO2;
猜想Ⅲ:CO2、CO
【实验设计】
将甲烷燃烧的产物依次通过A-E装置进行实验:

观察到的实验现象如下:
(1)A中澄清石灰水变浑浊,相关反应方程式为
(2)C中
(3)D中澄清石灰水变浑浊。
【实验结论】
根据以上实验现象可推断出猜想Ⅲ成立。
【反思交流】
有同学认为实验设计不合理,因为可能会有没烧完的甲烷对实验产生干扰。同学们经过讨论,在原有实验装置的基础上进行了改进:在B、C装置之间添加一个

重新实验后,两个新加的装置都无明显现象,其他装置的现象与上次实验相同。充分证明猜想Ⅲ成立。
【拓展延伸】
在装置末端“?”处应连接(放置)一个
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】(一)草酸(H2C2O4)是一种酸,存在于自然界的植物中,易溶于水,酸性强于碳酸,其熔点为101.5℃,在157℃升华,加热后分解成CO、CO2和水三种物质。
【提示】1、CuSO4是白色粉末,遇水变蓝
2、浓硫酸有吸水性,但不会和CO、CO2反应
3。NaOH溶液会吸收CO2,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O
4、CO不与氢氧化钠溶液反应
利用下图所示各装置(加持装置未画出),完成草酸分解实验并验证其产物。实验过程中:CuSO4粉末变蓝,盛放澄清石灰水的装置中溶液均变浑浊,C中粉末由黑变红。
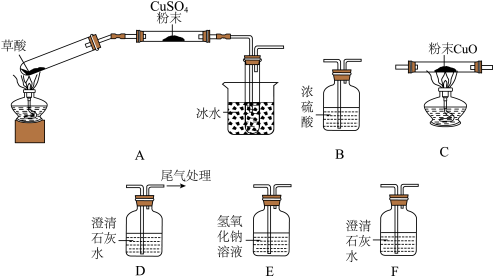
(1)该实验中各仪器的连接顺序为A→→D,排序正确的是_____ 。(填字母)
a、B-C-E-F b、 B-C-F-E c、F-E-B-C
其中E装置的作用是_____ 。
(2)CuSO4中硫元素的化合价为_____ 。
(3)草酸溶液中加入澄清石灰水,生成草酸钙(CaC2O4)固体和水。该反应的化学方程式为_____ 。
(二)草酸钙(CaC2O4)是一种白色晶体粉末,不溶于水,不溶于醋酸,高温灼烧会发生如下反应:CaC2O4 CaCO3 + CO ↑,兴趣小组取一定量的CaC2O4固体,在老师的指导下用下图装置进行实验。
CaCO3 + CO ↑,兴趣小组取一定量的CaC2O4固体,在老师的指导下用下图装置进行实验。

【实验一】
反应前先向试管内通入N2,再加热相应固体,一段时间后停止加热,缓缓通入N2至试管冷却。
(1)反应前先通N2的原因是_____ 。
(2)反应结束后装置B的质量增加了,说明加热过程中产生了_____ 气体。
【实验二】
取出装置A的试管中加热后的剩余固体,按图①-③进行实验。
(3)烧杯②中温度升高,则剩余固体中含有_____ 。
(4)将烧杯③中的溶液蒸干,得到CaCl2固体22.2g。
【结论】
I、取用的CaC2O4固体质量的为_____ g。(写出计算过程)
【提示:反应过程中钙元素的质量不变;加入稀盐酸反应后烧杯③中无固体剩余】
II、结合实验现象,请写出CaC2O4分解的总反应化学方程式为_____ 。
【提示】1、CuSO4是白色粉末,遇水变蓝
2、浓硫酸有吸水性,但不会和CO、CO2反应
3。NaOH溶液会吸收CO2,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O
4、CO不与氢氧化钠溶液反应
利用下图所示各装置(加持装置未画出),完成草酸分解实验并验证其产物。实验过程中:CuSO4粉末变蓝,盛放澄清石灰水的装置中溶液均变浑浊,C中粉末由黑变红。

(1)该实验中各仪器的连接顺序为A→→D,排序正确的是
a、B-C-E-F b、 B-C-F-E c、F-E-B-C
其中E装置的作用是
(2)CuSO4中硫元素的化合价为
(3)草酸溶液中加入澄清石灰水,生成草酸钙(CaC2O4)固体和水。该反应的化学方程式为
(二)草酸钙(CaC2O4)是一种白色晶体粉末,不溶于水,不溶于醋酸,高温灼烧会发生如下反应:CaC2O4
 CaCO3 + CO ↑,兴趣小组取一定量的CaC2O4固体,在老师的指导下用下图装置进行实验。
CaCO3 + CO ↑,兴趣小组取一定量的CaC2O4固体,在老师的指导下用下图装置进行实验。
【实验一】
反应前先向试管内通入N2,再加热相应固体,一段时间后停止加热,缓缓通入N2至试管冷却。
(1)反应前先通N2的原因是
(2)反应结束后装置B的质量增加了,说明加热过程中产生了
【实验二】
取出装置A的试管中加热后的剩余固体,按图①-③进行实验。
(3)烧杯②中温度升高,则剩余固体中含有
(4)将烧杯③中的溶液蒸干,得到CaCl2固体22.2g。
【结论】
I、取用的CaC2O4固体质量的为
【提示:反应过程中钙元素的质量不变;加入稀盐酸反应后烧杯③中无固体剩余】
II、结合实验现象,请写出CaC2O4分解的总反应化学方程式为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】小华所在的化学兴趣小组同学,在学习燃料的合理利用与开发后,对“天然气的主要成分甲烷燃烧后的气体产物是什么”产生了兴趣。他们在老师的指导下进行探究,请你参与探究并回答下列问题:
【提出问题】甲烷燃烧后生成哪些气体物质?
【查阅资料】①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;②白色无水硫酸铜粉末遇水变蓝色。
【猜想假设】猜想Ⅰ:CO2、H2O;猜想Ⅱ:CO、H2O;猜想Ⅲ:_____ 。
【实验设计】将甲烷在一定量纯净氧气中燃烧的产物依次通过A~E装置(部分夹持、固定装置省略)进行实验:

观察到的现象:①A中白色粉末变为蓝色;②B、E中澄清石灰水变浑浊;③D中红棕色粉末变成黑色。
【实验结论】根据以上实验现象可推断出猜想_____ 成立。
【反思交流】(1)装置B的作用是鉴别是否有_____ 生成,其中发生反应的化学方程式为_____ ;装置C的作用是_____ 。
(2)实验过程中用纯净的氧气而不用空气的原因是空气中含有_____ ,影响实验结果。
【实验改进】小明认为图示实验装置有缺陷,还应该在C、D装置之间增加一个装有澄清石灰水的洗气瓶。请你帮小明说明理由:_____ 。
【拓展延伸】日常生活中使用含碳燃料时,请你说出一条防止一氧化碳中毒的方法:_____ 。
【提出问题】甲烷燃烧后生成哪些气体物质?
【查阅资料】①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;②白色无水硫酸铜粉末遇水变蓝色。
【猜想假设】猜想Ⅰ:CO2、H2O;猜想Ⅱ:CO、H2O;猜想Ⅲ:
【实验设计】将甲烷在一定量纯净氧气中燃烧的产物依次通过A~E装置(部分夹持、固定装置省略)进行实验:

观察到的现象:①A中白色粉末变为蓝色;②B、E中澄清石灰水变浑浊;③D中红棕色粉末变成黑色。
【实验结论】根据以上实验现象可推断出猜想
【反思交流】(1)装置B的作用是鉴别是否有
(2)实验过程中用纯净的氧气而不用空气的原因是空气中含有
【实验改进】小明认为图示实验装置有缺陷,还应该在C、D装置之间增加一个装有澄清石灰水的洗气瓶。请你帮小明说明理由:
【拓展延伸】日常生活中使用含碳燃料时,请你说出一条防止一氧化碳中毒的方法:
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
【推荐2】通过对有机物的学习,知道甲烷是天然气的主要成分,密度小于空气,难溶于水,具有可燃性。同学们对甲烷继续进行探究学习:

探究Ⅰ:甲烷的制取
【查阅资料】实验室通过加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷。
(1)仪器a的名称是______ 。
(2)制取甲烷的发生装置应选______ (填序号,下同),选用装置C收集甲烷时气体应从______ 端进入,如果选择装置D收集,其中装满水,则气体应从______ 端进入。
探究Ⅱ:甲烷的组成元素
(3)点燃甲烷气体,在火焰上方罩一冷而干燥的烧杯(见图E),烧杯内壁有______ 生成,向烧杯中倒入少量澄清石灰水,振荡,现象为______ 。由此推断,甲烷中一定含C、H两种元素。
(4)点燃甲烷前,应先验纯,并且将甲烷气体通过盛有______ 的干燥装置D,目的是______ 。
(5)同学们通过隔绝空气对甲烷气体加强热,也得出了甲烷的组成元素,反应的化学方程式为:
______ 。
探究Ⅲ:甲烷的化学性质
【提出问题】通过以上探究,甲烷除了具有可燃性、能分解外,还具有什么化学性质?
(6)写出甲烷燃烧的化学方程式______ 。
【查阅资料】①无水硫酸铜粉末遇水由白色变蓝色,②甲烷具有还原性。
【验证实验】该同学按如图装置进行实验:
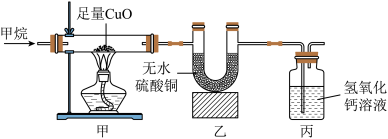
【实验现象与结论】
甲中黑色固体变为红色,乙中无水硫酸铜变为蓝色,丙中澄清石灰水变浑浊。
(7)根据实验现象,写出甲烷还原氧化铜的化学方程式:______ 。
【反思与评价】
实验时,要先向装置中通入一段时间的氮气,再通入甲烷加热的目的是______ 。

探究Ⅰ:甲烷的制取
【查阅资料】实验室通过加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷。
(1)仪器a的名称是
(2)制取甲烷的发生装置应选
探究Ⅱ:甲烷的组成元素
(3)点燃甲烷气体,在火焰上方罩一冷而干燥的烧杯(见图E),烧杯内壁有
(4)点燃甲烷前,应先验纯,并且将甲烷气体通过盛有
(5)同学们通过隔绝空气对甲烷气体加强热,也得出了甲烷的组成元素,反应的化学方程式为:

探究Ⅲ:甲烷的化学性质
【提出问题】通过以上探究,甲烷除了具有可燃性、能分解外,还具有什么化学性质?
(6)写出甲烷燃烧的化学方程式
【查阅资料】①无水硫酸铜粉末遇水由白色变蓝色,②甲烷具有还原性。
【验证实验】该同学按如图装置进行实验:

【实验现象与结论】
甲中黑色固体变为红色,乙中无水硫酸铜变为蓝色,丙中澄清石灰水变浑浊。
(7)根据实验现象,写出甲烷还原氧化铜的化学方程式:
【反思与评价】
实验时,要先向装置中通入一段时间的氮气,再通入甲烷加热的目的是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】几年前,我国在南海海域成功开采天然气水合物——可燃冰,可燃冰是甲烷与水在低温、高压的条件下形成的无色、冰状固体,是最具开发前景的能源之一。可燃冰的主要成分是CH4·nH2O,在开采过程中若甲烷泄漏,会导致严重温室效应。某校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与探究并回答有关问题:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;
②无水CuSO4遇水变蓝;
③氢氧化钠溶液与二氧化碳反应没有明显现象,常用于吸收二氧化碳气体。
【猜想与假设】甲:CO2、H2O 乙:CO、H2O 丙:NH3、H2O 丁:CO2、CO、H2O
你认为_______ 同学的猜想是错误的。
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的纯净氧气中燃烧的产物依次通过下列装置,进行验证:

【实验结论】
(1)A装置中无水CuSO4变蓝,则证明甲烷燃烧产物中有__________ ;
(2)B装置的作用是_____ ,装置中澄清石灰水变浑浊,其反应的化学方程式为_______ ;
(3)黑色氧化铜变红色,D装置中澄清石灰水也变浑浊,则证明甲烷燃烧产物中有_______ ;
(4)由此推断_______ 的猜想成立。
【交流反思】
(5)A、B装置的顺序不能颠倒,理由是_________________ ;
(6)实验中用纯净O2而不用空气的原因是___________________ ;
(7)为避免有毒的CO污染环境,所有含碳元素的物质燃烧必须满足的条件是______ 。
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;
②无水CuSO4遇水变蓝;
③氢氧化钠溶液与二氧化碳反应没有明显现象,常用于吸收二氧化碳气体。
【猜想与假设】甲:CO2、H2O 乙:CO、H2O 丙:NH3、H2O 丁:CO2、CO、H2O
你认为
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的纯净氧气中燃烧的产物依次通过下列装置,进行验证:

【实验结论】
(1)A装置中无水CuSO4变蓝,则证明甲烷燃烧产物中有
(2)B装置的作用是
(3)黑色氧化铜变红色,D装置中澄清石灰水也变浑浊,则证明甲烷燃烧产物中有
(4)由此推断
【交流反思】
(5)A、B装置的顺序不能颠倒,理由是
(6)实验中用纯净O2而不用空气的原因是
(7)为避免有毒的CO污染环境,所有含碳元素的物质燃烧必须满足的条件是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】向一定量的NaOH溶液中慢慢通入CO2气体,看不到明显现象。某实验小组的同学对所得溶液成分进行了如下探究,请你参与他们的探究活动,并完成以下问题:
【提出问题】所得溶液中溶质的成分是什么?
【查阅资料】资料一:将CO2气体慢慢地通入一定量的NaOH溶液中,可能发生以下两个化学反应:
先发生反应: 当NaOH反应完全后,继续发生反应:
当NaOH反应完全后,继续发生反应: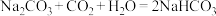
资料二:Ca(HCO3)2易溶于水:CaCl2溶液与NaCl溶液呈中性:NaHCO3溶液呈碱性,可使酚酞溶液变红色。
【猜想与假设】小组同学通过讨论,提出了以下四种猜想:
猜想一:溶质为NaOH和Na2CO3
猜想二:溶质全为Na2CO3
你认为猜想三;(1)溶质为_________
猜想四:溶质全为 NaHCO3
【实验探究】小组同学设计并完成了如下实验:
【实验反思】(6)根据所学的知识,请你推测将二氧化碳慢慢地通入一定量澄清石灰水中直至过量,将会出现的现象___________________ 。
【提出问题】所得溶液中溶质的成分是什么?
【查阅资料】资料一:将CO2气体慢慢地通入一定量的NaOH溶液中,可能发生以下两个化学反应:
先发生反应:
 当NaOH反应完全后,继续发生反应:
当NaOH反应完全后,继续发生反应: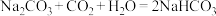
资料二:Ca(HCO3)2易溶于水:CaCl2溶液与NaCl溶液呈中性:NaHCO3溶液呈碱性,可使酚酞溶液变红色。
【猜想与假设】小组同学通过讨论,提出了以下四种猜想:
猜想一:溶质为NaOH和Na2CO3
猜想二:溶质全为Na2CO3
你认为猜想三;(1)溶质为
猜想四:溶质全为 NaHCO3
【实验探究】小组同学设计并完成了如下实验:
| 实验步骤 | 实验过程 | 实验现象 | 实验结论 |
| ① | 取适量反应后的溶液置于试管中,加入过量CaCl2溶液 | 有白色沉淀生成 | (2)猜想 |
| ② | 取适量步骤①反应后的上层清液,滴加几滴酚酞溶液 | (3)现象为 | 猜想二不成立 |
| ③ | 取适量步骤①反应后的上层清液,加入适量(4) | (5)现象为 | 猜想三成立 |
【实验反思】(6)根据所学的知识,请你推测将二氧化碳慢慢地通入一定量澄清石灰水中直至过量,将会出现的现象
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】(1)实验探究小组的同学欲利用下列仪器验证某混合气体可能含有H2、CO、H2O、HCl中的一种或几种组成。
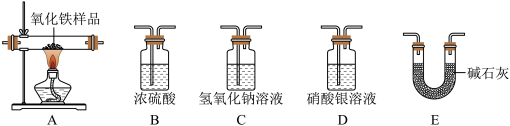
【实验设计】 所选仪器的连接顺序为:混合气体→D→B1→A→B2→C→E(B1、B2均为盛装浓硫酸的试剂瓶)。
【实验及数据】样品充分反应(假设每步均反应完全),并测定部分装置反应前后的质量变化,数据如下:
请回答下列问题:
①装置A中能观察到的明显现象是___________________________________ ;
②装置D的作用是_________________________________ ;
③根据表格中的现象和数据判断,混合气体中一定不存在的气体是 ___________ ;无法确定是否存在的气体是 ___________ ,要验证该气体是否存在,应如何改进实验设计 ______________________________________________ ;
④从环境保护的角度考虑,针对该套实验装置不足提出改进建议____________________ 。
(2)“84”消毒液在日常生活中使用广泛,化学兴趣小组对一瓶敞口久置的“84”消毒液成分产生兴趣,展开探究。
【查阅资料】“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO为有效成分,有腐蚀性并易与空气中CO2反应(2NaClO+CO2+H2O═2HClO+Na2CO3)。NaClO溶液、HClO都具有漂白、杀菌、消毒功效,HClO不稳定,受热或光照会发生分解。
【分析讨论】小组同学经过讨论,认为该消毒液中的溶质一定有_______ ,可能还有NaClO、Na2CO3、HClO中的一种或多种。
【实验过程】大家对可能存在的溶质继续进行以下探究:
【交流反思】“84”消毒液贮藏时应注意密封保存,其原因可能是____________________ 。
【拓展延伸】日常生活中“84”消毒液不能与洁厕灵(主要成分为盐酸)混合使用,因为二者混合生成氯化钠、水及有毒的氯气,写出该反应的化学方程式______________________ 。

【实验设计】 所选仪器的连接顺序为:混合气体→D→B1→A→B2→C→E(B1、B2均为盛装浓硫酸的试剂瓶)。
【实验及数据】样品充分反应(假设每步均反应完全),并测定部分装置反应前后的质量变化,数据如下:
| 装置编号 | D | B1 | B2 | C |
| 试剂 | 硝酸银溶液 | 浓硫酸 | 浓硫酸 | 氢氧化钠溶液 |
| 现象或质量变化 | 无明显现象 | 增重1.0g | 无增重 | 增重6.6g |
①装置A中能观察到的明显现象是
②装置D的作用是
③根据表格中的现象和数据判断,混合气体中一定
④从环境保护的角度考虑,针对该套实验装置不足提出改进建议
(2)“84”消毒液在日常生活中使用广泛,化学兴趣小组对一瓶敞口久置的“84”消毒液成分产生兴趣,展开探究。
【查阅资料】“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO为有效成分,有腐蚀性并易与空气中CO2反应(2NaClO+CO2+H2O═2HClO+Na2CO3)。NaClO溶液、HClO都具有漂白、杀菌、消毒功效,HClO不稳定,受热或光照会发生分解。
【分析讨论】小组同学经过讨论,认为该消毒液中的溶质一定有
【实验过程】大家对可能存在的溶质继续进行以下探究:
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取适量的该消毒液于试管中,放入有色布条 | 布条长时间不褪色 | |
| 2. | 生成白色沉淀 | 该消毒液中含有Na2CO3 |
【交流反思】“84”消毒液贮藏时应注意密封保存,其原因可能是
【拓展延伸】日常生活中“84”消毒液不能与洁厕灵(主要成分为盐酸)混合使用,因为二者混合生成氯化钠、水及有毒的氯气,写出该反应的化学方程式
您最近一年使用:0次
【推荐3】CaCl2可用于冷冻剂、干燥剂、融雪剂、医药及冶金工业等。化学兴趣小组在完成实验室制取二氧化碳的实验后,欲对剩余废液的组成进行探究,并制定回收CaCl2的方案。
【提出问题】实验室制取二氧化碳后的废液中含有哪些溶质?
【猜想与假设】猜想一:CaCl2猜想二:CaCl2和HCl
【查阅资料】CaCl2溶液呈中性
【探究活动一】取少量废液等分成2份,甲、乙两组同学分别利用其中一份进行如下探究:
甲组同学向废液中滴加紫色石蕊溶液,溶液变成___________ 色,证明猜想二成立。
乙组同学用图1装置进行实验,将80mL一定质量分数的碳酸钠溶液逐滴加入废液,测得数据如图2。
I.a点的实验现象为___________ 。
Ⅱ.b点发生反应的化学方程式为___________ 。
Ⅲ.c点对应溶液中全部溶质的化学式为___________ 。
【探究活动二】丙组同学提出直接蒸发溶剂可从剩余废液中回收纯净CaCl2,理由是___________ 。
【交流与反思】甲组同学认为丙组同学提出的方法会对空气造成污染。在不借助其它试剂和仪器的情况下,除去废液中对空气造成污染的物质,建议最好先在废液中加入下面______ (填选项序号)试剂。
A.CaO B.Ca(OH)2 C.CaCO3
【提出问题】实验室制取二氧化碳后的废液中含有哪些溶质?
【猜想与假设】猜想一:CaCl2猜想二:CaCl2和HCl
【查阅资料】CaCl2溶液呈中性
【探究活动一】取少量废液等分成2份,甲、乙两组同学分别利用其中一份进行如下探究:
甲组同学向废液中滴加紫色石蕊溶液,溶液变成
乙组同学用图1装置进行实验,将80mL一定质量分数的碳酸钠溶液逐滴加入废液,测得数据如图2。
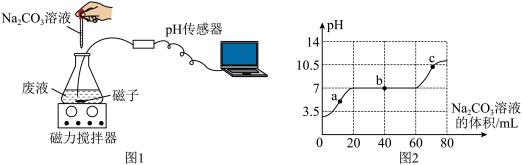
I.a点的实验现象为
Ⅱ.b点发生反应的化学方程式为
Ⅲ.c点对应溶液中全部溶质的化学式为
【探究活动二】丙组同学提出直接蒸发溶剂可从剩余废液中回收纯净CaCl2,理由是
【交流与反思】甲组同学认为丙组同学提出的方法会对空气造成污染。在不借助其它试剂和仪器的情况下,除去废液中对空气造成污染的物质,建议最好先在废液中加入下面
A.CaO B.Ca(OH)2 C.CaCO3
您最近一年使用:0次



