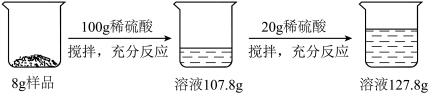
菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中MgCO3的含量,学习小组进行了实验研究.取10克菱镁矿样品,向其中逐滴加入未知质量分数的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:
(假设菱镁矿中的杂质不溶于水,不与酸发生反应.)
(1)10克菱镁矿与H2SO4溶液完全反应,生成CO2的质量为_____.
(2)该菱镁矿中MgCO3的质量分数是多少?
(3)该实验研究中所用H2SO4溶液的溶质质量分数是多少?
加入H2SO4溶液的质量/g | 50 | 100 | 150 | 200 |
NaOH溶液增加的质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
(假设菱镁矿中的杂质不溶于水,不与酸发生反应.)
(1)10克菱镁矿与H2SO4溶液完全反应,生成CO2的质量为_____.
(2)该菱镁矿中MgCO3的质量分数是多少?
(3)该实验研究中所用H2SO4溶液的溶质质量分数是多少?
更新时间:2019-04-19 13:26:07
|
【知识点】 化学方程式与实验的计算解读
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】某钙片(补钙剂)说明书的部分信息如图1所示,化学兴趣小组探究该钙片中碳酸钙的含量,取20片药剂制成粉末,进行了如下的定量实验:用图所示的装置进行实验,将稀盐酸全部加入锥形瓶中,天平示数的变化如图所示。请计算:
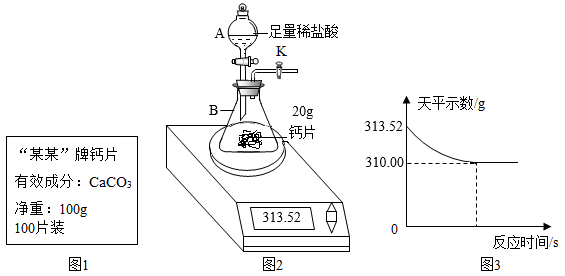
(1)实验中生成二氧化碳___________ g。
(2)这种钙片中碳酸钙的质量分数为______ ?(写出计算过程)
(3)若某同学需补充0.8克钙元素,则需服用这种钙片___________ 片。

(1)实验中生成二氧化碳
(2)这种钙片中碳酸钙的质量分数为
(3)若某同学需补充0.8克钙元素,则需服用这种钙片
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】向20g碳酸钙中不断加入稀盐酸,其质量变化如图所示,请回答下列问题:
(1)当20g碳酸钙恰好完全反应时,所加稀盐酸的质量为多少克?
(2)所加稀盐酸的溶质质量分数为多少?(结果精确到0.01%)
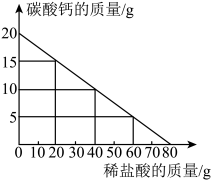
(1)当20g碳酸钙恰好完全反应时,所加稀盐酸的质量为多少克?
(2)所加稀盐酸的溶质质量分数为多少?(结果精确到0.01%)

您最近一年使用:0次