某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。请计算:
(1)若要清洗1000kg的这种石油产品,需要______ kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。每处理1000kg这种产品,可以节约多少经费?已知工业级的NaOH和Ca(OH)2的最新市场批发价如下表:
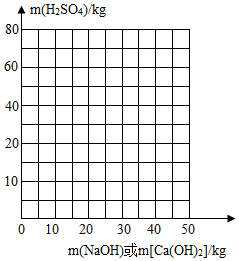
(3)请画出用氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线表示,氢氧化钙用实线表示。______
(4)将反应后生成的硫酸钙回收,在一定条件下加入高温硫酸盐还原菌,可以将SO42-离子转化生成H2S气体,然后用以硫酸的生产工业。不考虑整个过程中硫元素的损失,若将(2)中产生的硫酸钙全部转化,可生产H2S的质量为______ kg。
(1)若要清洗1000kg的这种石油产品,需要
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。每处理1000kg这种产品,可以节约多少经费?已知工业级的NaOH和Ca(OH)2的最新市场批发价如下表:
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 1.00 | 6.00 |
(3)请画出用氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线表示,氢氧化钙用实线表示。

(4)将反应后生成的硫酸钙回收,在一定条件下加入高温硫酸盐还原菌,可以将SO42-离子转化生成H2S气体,然后用以硫酸的生产工业。不考虑整个过程中硫元素的损失,若将(2)中产生的硫酸钙全部转化,可生产H2S的质量为
更新时间:2019-05-20 15:52:04
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】有一含有纯碱的食盐样品,为了测定其中碳酸钠的含量,某同学称取10g的样品放入烧杯中,向烧杯中加入100g足量的 稀盐酸,充分反应后气体全部逸出,烧杯中剩余物的总质量为109.56g(假设产生的气体全部逸出。以下计算结果保留一位小数)
(1)样品中碳酸钠的含量是___
(2)NaCl中氯元素质量分数是____
(3)反应后溶液中溶质质量分数是___ ?
(1)样品中碳酸钠的含量是
(2)NaCl中氯元素质量分数是
(3)反应后溶液中溶质质量分数是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某综合实践活动小组同学,对我市某化工厂排放的污水进行检测,发现主要的污染物为氢氧化钠。为测定污水中氢氧化钠的含量,取100 g污水于烧杯中,加入36.5 g质量分数为10%的稀盐酸恰好完全反应。(假设污水中其他成分不与稀盐酸反应,反应的化学方程式为:HCl+NaOH=NaCl+H2O)
求:(1)100 g污水中含氢氧化钠多少克?
(2)污水中所含氢氧化钠的质量分数。
求:(1)100 g污水中含氢氧化钠多少克?
(2)污水中所含氢氧化钠的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】化学兴趣小组的同学进行酸与锌反应制取氢气的实验研究,取6.5g等质量的金属锌,分别加入400g过量的H2SO4溶液,按下表进行实验,产生氢气的质量随时间变化曲线如图所示。
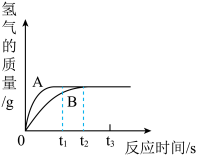
回答下列问题:
(1)表示实验Ⅱ的是图中的曲线______(填A或B)。
(2)请计算实验Ⅰ产生氢气的质量(写出计算过程)。
(3)对比实验Ⅰ和Ⅲ你能得出的结论是______。
(4)若用图甲进行实验Ⅲ的探究,请在图中乙画出该探究相应的曲线图。
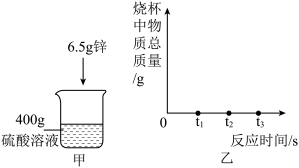
| 实验编号 | 药品 | 反应时间 | 曲线 |
| Ⅰ | 颗粒状锌粒、5%H2SO4溶液 | t1或t2 | 如图曲线A或B |
| Ⅱ | 粉末状锌、5%H2SO4溶液 | ||
| Ⅲ | 颗粒状锌粒、2.5% H2SO4溶液 | t3 | 未绘制 |

回答下列问题:
(1)表示实验Ⅱ的是图中的曲线______(填A或B)。
(2)请计算实验Ⅰ产生氢气的质量(写出计算过程)。
(3)对比实验Ⅰ和Ⅲ你能得出的结论是______。
(4)若用图甲进行实验Ⅲ的探究,请在图中乙画出该探究相应的曲线图。

您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】某锥形瓶盛有盐酸和氯化铜的混合溶液 100g,向其中逐滴加入氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量的变化关系如图所示。

请计算:
(1)m 的值是______ ;
(2)生成沉淀的物质的质量是______ g;
(3)反应至 B 点时锥形瓶内所得溶液的溶质质量分数为(结果保留至 0.1%)

请计算:
(1)m 的值是
(2)生成沉淀的物质的质量是
(3)反应至 B 点时锥形瓶内所得溶液的溶质质量分数为(结果保留至 0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某地岩石以石灰岩为主,石灰石储量达50亿吨,是制造水泥、石灰、轻质碳酸钙的主要原料来源.某校科学探究小组同学把一块从山上捡来的石灰石做纯度分析,进行了如下实验:
①用天平准确称取30克石灰石放入甲图A装置中,同时加入足量稀盐酸;
②测量C装置中吸收到的由反应过程中产生的二氧化碳的质量,并据此绘成乙图中的曲线;
③根据实验结果计算该石灰石的纯度;
请分析回答下列问题:

(1)根据实验数据计算该石灰石中CaCO3的质量分数为_____________;
(2)忽略空气中二氧化碳及盐酸挥发对实验结果的影响,由C装置测得的二氧化碳质量与实际反应产生的二氧化碳质量并不相等.试分析原因可能是_____________;请说说你的改进措施___________。
①用天平准确称取30克石灰石放入甲图A装置中,同时加入足量稀盐酸;
②测量C装置中吸收到的由反应过程中产生的二氧化碳的质量,并据此绘成乙图中的曲线;
③根据实验结果计算该石灰石的纯度;
请分析回答下列问题:

(1)根据实验数据计算该石灰石中CaCO3的质量分数为_____________;
(2)忽略空气中二氧化碳及盐酸挥发对实验结果的影响,由C装置测得的二氧化碳质量与实际反应产生的二氧化碳质量并不相等.试分析原因可能是_____________;请说说你的改进措施___________。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】有一种管道疏通剂,主要成分为铝粉和氢氧化钠混合粉末。小柯利用如图装置测定疏通剂中铝的质量分数。

Ⅰ.取样品20g,倒入容积为200ml的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。
Ⅲ.实验数据如下表:
回答下列问题:
(1)配平化学方程式:2Al+2NaOH+2H2O=_____NaAlO2+3H2↑
(2)根据化学方程式计算样品中铝的质量分数。_____

Ⅰ.取样品20g,倒入容积为200ml的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。
Ⅲ.实验数据如下表:
| 反应前总质量m1 | 反应后总质量m2 |
| 371.84g | 371.24g |
回答下列问题:
(1)配平化学方程式:2Al+2NaOH+2H2O=_____NaAlO2+3H2↑
(2)根据化学方程式计算样品中铝的质量分数。_____
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】为测定一瓶氢氧化钠溶液的质量分数,小芳同学进行了以下实验,如图所示,当溶液颜色恰好变为无色时,消耗稀盐酸7.3g。
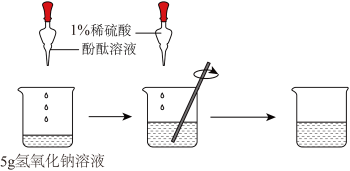
(1)理论计算:计算该氢氧化钠溶液的质量分数(写出计算过程)。
(2)实验分析:已知酚酞溶液的变色范围是pH在8.2~10.0之间,当pH<8.2时显无色。用该方法测定的氢氧化钠溶液的质量分数可能比实际值 (选填“偏大”或“偏小”),原因是 。

(1)理论计算:计算该氢氧化钠溶液的质量分数(写出计算过程)。
(2)实验分析:已知酚酞溶液的变色范围是pH在8.2~10.0之间,当pH<8.2时显无色。用该方法测定的氢氧化钠溶液的质量分数可能比实际值 (选填“偏大”或“偏小”),原因是 。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】现用质量分数为29.2%的盐酸溶液配制500g质量分数为7.3%的稀盐酸,用所配稀盐酸测得某NaOH溶液的溶质质量分数为20%。
(1)需要加入_____g水来配得上述稀盐酸。
(2)测得溶液pH=7时,消耗稀盐酸200g。求恰好完全反应时,所得溶液中溶质质量分数。_____(写出计算过程,计算结果保留一位小数)
(3)若所测NaOH溶液在空气中放置时间较长,已经变质,那么测定的NaOH质量_____(填“偏大”、“偏小”、“不变”或“无法确定”)。
(1)需要加入_____g水来配得上述稀盐酸。
(2)测得溶液pH=7时,消耗稀盐酸200g。求恰好完全反应时,所得溶液中溶质质量分数。_____(写出计算过程,计算结果保留一位小数)
(3)若所测NaOH溶液在空气中放置时间较长,已经变质,那么测定的NaOH质量_____(填“偏大”、“偏小”、“不变”或“无法确定”)。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
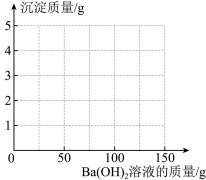
【推荐3】某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸50 g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如图所示。(结果保留两位小数)

(1)参加反应的Ba(OH)2质量共有______ g;当滴加Ba(OH)2溶液50 g时,烧杯内溶液的pH______ 7(填“>”“<”或“=”)。
(2)求该硫酸溶液的溶质质量分数(写出答题过程,结果保留0.01%)。
(3)在如图中画出产生沉淀质量与滴加Ba(OH)2溶液的质量关系图(请你标注具体坐标)。
(4)滴加Ba(OH)2溶液至150 g时,所得溶液的溶质质量分数为______ (结果保留0.01%)。

(1)参加反应的Ba(OH)2质量共有
(2)求该硫酸溶液的溶质质量分数(写出答题过程,结果保留0.01%)。
(3)在如图中画出产生沉淀质量与滴加Ba(OH)2溶液的质量关系图(请你标注具体坐标)。

(4)滴加Ba(OH)2溶液至150 g时,所得溶液的溶质质量分数为
您最近一年使用:0次



