现有一瓶无色溶液,溶质可能是KOH、K2CO3中的一种或两种,某兴趣小组对其成分进行如下实验探究:
【查阅资料】①KOH与NaOH的化学性质相似,K2CO3与Na2CO3的化学性质相似。②K2CO3溶液呈碱性,BaCl2溶液、CaCl2溶液、KCl溶液呈中性。
【实验探究】设计并进行实验
【评价反思】①甲同学提出操作(1)加入的CaCl2溶液必须过量,其目的是证明K2CO3存在的同时还要______ 。
②乙同学提出操作(1)在溶液较浓时,没有K2CO3也能产生相同现象,其原因是_____ ;建议改加过量的BaCl2溶液,BaCl2参加反应的化学方程式为_____ 。
【拓展应用】KOH和K2CO3的混合溶液敞口久置后可能变成K2CO3溶液,反应的化学方程式为______ 。
【查阅资料】①KOH与NaOH的化学性质相似,K2CO3与Na2CO3的化学性质相似。②K2CO3溶液呈碱性,BaCl2溶液、CaCl2溶液、KCl溶液呈中性。
【实验探究】设计并进行实验
| 实验操作步骤 | 实验现象 | 实验结论 |
| (1)向盛有少量样品溶液的试管中加入过量CaCl2溶液 | 肯定含有K2CO3 | |
| (2)将操作(1)后的试管静置,再向上层清液中加入几滴酚酞溶液 | 酚酞溶液变红色 | 肯定含有 |
【评价反思】①甲同学提出操作(1)加入的CaCl2溶液必须过量,其目的是证明K2CO3存在的同时还要
②乙同学提出操作(1)在溶液较浓时,没有K2CO3也能产生相同现象,其原因是
【拓展应用】KOH和K2CO3的混合溶液敞口久置后可能变成K2CO3溶液,反应的化学方程式为
更新时间:2019-06-28 20:10:18
|
相似题推荐
科学探究题
|
较难
(0.4)
真题
【推荐1】某校九年级“我们爱化学”活动小组的同学,在探究碱的化学性质时,完成了如图所示的A、B两个实验。请你回答下列问题:

(1)A实验中酚酞的作用是_______ ,所发生的化学反应方程式为___________ 。
(2)B实验中可观察到的现象是__________ 。
(3)实验后,将两支试管中的废液都倒入废液杯C中,发现混合废液浑浊并显红色。
【分析思考】同学们经过思考一致认为,混合废液显红色是B实验后试管中的溶质与A实验后试管中的酚酞反应的结果。
【提出问题】B实验后试管中的溶质是什么?
【作出猜想】猜想一:试管中的溶质是NaOH;猜想二:试管中的溶质是____________ ;
猜想三:试管中的溶质是Ca(OH)2和NaOH。
【实验验证】华雪同学利用废液杯C中的混合废液来确定B实验后试管中的溶质:将一定质量的废液过滤,取10g滤液并向其中逐滴加入质量分数为7.3% 的稀盐酸,当加入稀盐酸的质量为20g时反应完全,继续加入稀盐酸,气体的质量不再增加,根据反应现象得到如图所示的图像。
【查阅资料】碳酸钠溶液与稀盐酸的反应是分步进行的。首先是碳酸钠与稀盐酸反应生成碳酸氢钠和氯化钠:Na2CO3 + HCl===NaHCO3 +NaCl;然后是生成的碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳气体和水:NaHCO3+HCl===NaCl+CO2↑+H2O。
【实验结论】定性结论:分析图像得出:猜想二是正确的,产生的气体是________ (填化学式);猜想一和猜想三是错误的,原因是_______ 。
定量结论:10g废液中含有______ g NaOH,_______ g Na2CO3,_______ g Ca(OH)2。
【拓展提升】请另外设计一个实验,定性证明上述猜想二是正确的:_________ 。

(1)A实验中酚酞的作用是
(2)B实验中可观察到的现象是
(3)实验后,将两支试管中的废液都倒入废液杯C中,发现混合废液浑浊并显红色。
【分析思考】同学们经过思考一致认为,混合废液显红色是B实验后试管中的溶质与A实验后试管中的酚酞反应的结果。
【提出问题】B实验后试管中的溶质是什么?
【作出猜想】猜想一:试管中的溶质是NaOH;猜想二:试管中的溶质是
猜想三:试管中的溶质是Ca(OH)2和NaOH。
【实验验证】华雪同学利用废液杯C中的混合废液来确定B实验后试管中的溶质:将一定质量的废液过滤,取10g滤液并向其中逐滴加入质量分数为7.3% 的稀盐酸,当加入稀盐酸的质量为20g时反应完全,继续加入稀盐酸,气体的质量不再增加,根据反应现象得到如图所示的图像。
【查阅资料】碳酸钠溶液与稀盐酸的反应是分步进行的。首先是碳酸钠与稀盐酸反应生成碳酸氢钠和氯化钠:Na2CO3 + HCl===NaHCO3 +NaCl;然后是生成的碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳气体和水:NaHCO3+HCl===NaCl+CO2↑+H2O。
【实验结论】定性结论:分析图像得出:猜想二是正确的,产生的气体是
定量结论:10g废液中含有
【拓展提升】请另外设计一个实验,定性证明上述猜想二是正确的:
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】某校化学课堂围绕课本《实验活动6酸、碱的化学性质》开展自主探究活动,以下是探究片段,请你参与学习。
(1)向装有生锈铁钉的试管中加入稀盐酸,观察到铁锈逐渐消失,因此盐酸常用于金属表面除锈,该反应的化学方程式为:______ 。
(2)在进行盐酸中和氢氧化钠溶液实验时,某一小组忘记向氢氧化钠溶液中滴加酚酞试液,因此未观察到明显现象,该小组同学对此时反应后所得溶液的成分产生疑问。
[假设猜想]针对疑问,第一组同学的猜想如下:
猜想一:只有NaCl
猜想二:有NaCl和HCl
猜想三:有NaCl和NaOH
猜想四:有NaCl、HCl 和NaOH
第二组同学对以上猜想提出质疑,认为有一种猜想是不合理的,你认为不合理的猜想是_____ 。
[实验探究]
①第三组同学取少量该溶液于试管中,滴加_____ 溶液,无明显变化,则溶液中一定没有氢氧化钠。
②为验证其余猜想,第四组同学分别取该溶液样品按下列方案探究:
(3)[得出结论]通过比较分析,同学们一致确定猜想二是正确的。
[评价反思]①老师对同学们能用多种方法进行探究给予肯定,同时指出方案二是错误的,原因是______ 。
②小明发现,排除不合理猜想后,选用一种试剂只做一次实验就能同时验证其余猜想,此试剂是:______ 。(填名称)
(4)[交流讨论]中和反应在日常生活和工农业生产中有广泛应用,请你举一个实例说明:___ 。
(1)向装有生锈铁钉的试管中加入稀盐酸,观察到铁锈逐渐消失,因此盐酸常用于金属表面除锈,该反应的化学方程式为:
(2)在进行盐酸中和氢氧化钠溶液实验时,某一小组忘记向氢氧化钠溶液中滴加酚酞试液,因此未观察到明显现象,该小组同学对此时反应后所得溶液的成分产生疑问。
[假设猜想]针对疑问,第一组同学的猜想如下:
猜想一:只有NaCl
猜想二:有NaCl和HCl
猜想三:有NaCl和NaOH
猜想四:有NaCl、HCl 和NaOH
第二组同学对以上猜想提出质疑,认为有一种猜想是不合理的,你认为不合理的猜想是
[实验探究]
①第三组同学取少量该溶液于试管中,滴加
②为验证其余猜想,第四组同学分别取该溶液样品按下列方案探究:
| 方案 | 实验操作 | 实验现象 | 实验结论 |
| 方案一 | 往溶液中滴加 | 有气泡产生 | 溶液中有HCl |
| 方案二 | 往溶液中滴加AgNO3溶液 | 产生白色沉淀 | 溶液中有HCl |
(3)[得出结论]通过比较分析,同学们一致确定猜想二是正确的。
[评价反思]①老师对同学们能用多种方法进行探究给予肯定,同时指出方案二是错误的,原因是
②小明发现,排除不合理猜想后,选用一种试剂只做一次实验就能同时验证其余猜想,此试剂是:
(4)[交流讨论]中和反应在日常生活和工农业生产中有广泛应用,请你举一个实例说明:
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】请回忆你和老师共同学习的酸和碱反应的实验探究,并按要求进行实验设计与分析:
【实验探究】
(1)据图设计酸和碱反应:
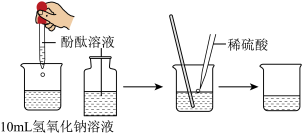
写出硫酸与氢氧化钠反应的化学方程式__________________ 。
(2)为探究上述酸、碱反应后硫酸是否过量,甲、乙两位同学设计了以下方案:
【实验评价】
①甲、乙两位同学设计的二个方案中,有一个正确的方案,是________ (填“甲”“乙” )。
②请分析另一个同学方案错误的原因是__________ 。
【实验反思】
探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂是( )
AFe BCa(OH)2 CCuO DNa2CO3
【实验探究】
(1)据图设计酸和碱反应:

| 实验步骤 | 实验现象 | 结论 |
| ①向烧杯中加入 10mL 氢氧化钠溶液,并滴入几滴酚酞试液 | ①溶液颜色 | 酸和碱发生了中和反应。 |
| ②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液 | ②不断搅拌溶液至溶液颜色变成 |
写出硫酸与氢氧化钠反应的化学方程式
(2)为探究上述酸、碱反应后硫酸是否过量,甲、乙两位同学设计了以下方案:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 甲同学的方案 | 取样,滴入几滴无色酚酞溶液 | 酚酞溶液不变色 | 酸、碱恰好完全反应 |
| 乙同学的方案 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 硫酸过量 |
【实验评价】
①甲、乙两位同学设计的二个方案中,有一个正确的方案,是
②请分析另一个同学方案错误的原因是
【实验反思】
探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂是
AFe BCa(OH)2 CCuO DNa2CO3
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
【提出问题1】该样品中含有哪些物质?
【做出猜想】通过分析,做出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3。
【查阅资料】
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
②CO2在饱和的碳酸氢钠溶液中几乎不溶解。
【实验探究1】
为确定该样品的成分,小明设计了如下实验方案请你一起完成下列实验报告。
【提出问题2】如何测量该部分变质样品中碳酸钠的质量分数?
【实验探究2】
小红同学设计了如图所示的装置(铁架台略去),实验在27℃,101kPa下进行,步骤如下:
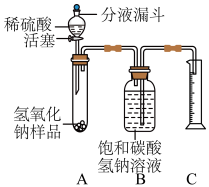
①按图连接好装置;
②用托盘天平准确称取该样品2g,放入A中试管内,向B集气瓶中倒入饱和的碳酸氢钠溶液至瓶颈处;
③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞。反应结束后,量筒中收集到饱和的碳酸氢钠溶液220mL。
请回答下列问题:
(1)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是__________ 。
(2)B中集气瓶盛装的饱和的碳酸氢钠溶液不能用水代替,其理由是__________ 。
(3)试管中原有的空气对实验结果是否有明显影响?__________ (选填“有”或“没有”)。
【提出问题3】怎样提纯该样品得到纯净的氢氧化钠固体?
【实验探究3】
为得到纯净的氢氧化钠固体,小亮设计了如下图所示的实验流程。

(4)该实验最终所得氢氧化钠固体质量__________ (选填“大于”“等于”或“小于”)变质后样品中氢氧化钠的质量。
注意:若答对第(5)(6)小题奖励3分,化学试卷总分不超过40分。
【实验反思】
(5)通过本题,你学会了定性检验氢氧化钠的变质、定量测定变质后某成分的含量,以及除杂提纯物质。为了得到可靠的实验结果,探究过程中你需要思考问题有__________ (填数字序号)。
①选择试剂种类②确定试剂用量③试剂产地④实验装置与步骤的设计⑤实验安全环保⑥测量中减少误差
(6)实验探究1中的检验和实验探究3中的除杂都将碳酸钠进行了转化,但二者目的不同,分别是__________ 、__________ 。
【提出问题1】该样品中含有哪些物质?
【做出猜想】通过分析,做出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3。
【查阅资料】
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
②CO2在饱和的碳酸氢钠溶液中几乎不溶解。
【实验探究1】
为确定该样品的成分,小明设计了如下实验方案请你一起完成下列实验报告。
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品溶于水,加入 | 有白色沉淀产生 | 该反应的化学方程式为 |
| ②将上述反应后的混合液过滤,取滤液加 入 | 猜想Ⅱ成立 |
【实验探究2】
小红同学设计了如图所示的装置(铁架台略去),实验在27℃,101kPa下进行,步骤如下:

①按图连接好装置;
②用托盘天平准确称取该样品2g,放入A中试管内,向B集气瓶中倒入饱和的碳酸氢钠溶液至瓶颈处;
③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞。反应结束后,量筒中收集到饱和的碳酸氢钠溶液220mL。
请回答下列问题:
(1)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是
(2)B中集气瓶盛装的饱和的碳酸氢钠溶液不能用水代替,其理由是
(3)试管中原有的空气对实验结果是否有明显影响?
【提出问题3】怎样提纯该样品得到纯净的氢氧化钠固体?
【实验探究3】
为得到纯净的氢氧化钠固体,小亮设计了如下图所示的实验流程。

(4)该实验最终所得氢氧化钠固体质量
注意:若答对第(5)(6)小题奖励3分,化学试卷总分不超过40分。
【实验反思】
(5)通过本题,你学会了定性检验氢氧化钠的变质、定量测定变质后某成分的含量,以及除杂提纯物质。为了得到可靠的实验结果,探究过程中你需要思考问题有
①选择试剂种类②确定试剂用量③试剂产地④实验装置与步骤的设计⑤实验安全环保⑥测量中减少误差
(6)实验探究1中的检验和实验探究3中的除杂都将碳酸钠进行了转化,但二者目的不同,分别是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】某实验小组为探究酸的化学性质,由甲、乙、丙同学设计并完成了如图所示的实验。

(1)甲同学实验中所发生反应的化学方程式为__________ 。
丙同学实验试管中的反应现象是_____________ 。
【查阅资料】CaCl2、NaCl的溶液呈中性,Na2CO3溶液显碱性。
【实验探究一】确定甲、乙同学上述实验后所得溶液中的溶质。
(2)取甲所得溶液少许,加入石蕊溶液,溶液显红色,甲所得溶液中一定含有的溶质是__________ (填化学式)。
(3)取乙所得溶液少许,加入酚酞溶液,溶液显红色,乙所得溶液中一定含有的溶质是__________ (填化学式)。
【实验探究二】确定甲、乙同学上述实验所得溶液混合后的成分。
(4)甲、乙同学把上述实验所得溶液倒入同一废液缸中,观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
【提出猜想】
(5)甲同学猜想:NaCl 乙同学猜想:NaCl、CaCl2 丙同学猜想:NaCl、CaCl2、HCl你的猜想:_________________ 。
【交流讨论】
(6)你认为丙同学的猜想一定不正确,理由是有盐酸就不会有白色沉淀产生。
【设计实验】
请设计实验证明你的猜想正确。

(1)甲同学实验中所发生反应的化学方程式为
丙同学实验试管中的反应现象是
【查阅资料】CaCl2、NaCl的溶液呈中性,Na2CO3溶液显碱性。
【实验探究一】确定甲、乙同学上述实验后所得溶液中的溶质。
(2)取甲所得溶液少许,加入石蕊溶液,溶液显红色,甲所得溶液中一定含有的溶质是
(3)取乙所得溶液少许,加入酚酞溶液,溶液显红色,乙所得溶液中一定含有的溶质是
【实验探究二】确定甲、乙同学上述实验所得溶液混合后的成分。
(4)甲、乙同学把上述实验所得溶液倒入同一废液缸中,观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
【提出猜想】
(5)甲同学猜想:NaCl 乙同学猜想:NaCl、CaCl2 丙同学猜想:NaCl、CaCl2、HCl你的猜想:
【交流讨论】
(6)你认为丙同学的猜想一定不正确,理由是有盐酸就不会有白色沉淀产生。
【设计实验】
请设计实验证明你的猜想正确。
| 实验步骤 | 实验现象 | 实验结论 |
| ① | ② | 猜想成立 |
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐3】为了研究二氧化碳与碱的反应,化学小组的同学进行了如下实验:
用两个塑料瓶收集满二氧化碳,分别加入等量的饱和石灰水(1号)、饱和氢氧化钠溶液(2号),拧紧瓶盖,振荡,塑料瓶变瘪的情况如图所示。实验过程中同学们还发现石灰水变浑浊后,很快又变澄清了。

【提出问题】1 为什么两个塑料瓶变瘪程度不同?
2 为什么石灰水变浑浊后又变澄清?
3 两个塑料瓶中溶液的成分是什么?
【查阅资科】碳酸钙与水、二氧化碳反应生成能溶于水的碳酸氢钙。
【对比分析】
(1)氢氧化钠易溶于水,氢氧化钙___________ 溶于水,饱和氢氧化钠溶液比等量饱和石灰水吸收了更多的二氧化碳。
(2)石灰水与二氧化碳反应变浑浊后,碳酸钙继续与水、二氧化碳反应,根据化学方程式可以推出生成物碳酸氢钙的化学式:
___________ 。
【猜想假设】2号塑料瓶中溶液成分可能是(1)Na2CO3
(2)Na2CO3和___________ 。
【实验验证】
乙同学步骤(1)中的化学方程式为___________ 。
【反思评价】对甲同学的实验操作进行改进,也可以得出与乙同学相同的结论,操作方案和现象是___________ 。
用两个塑料瓶收集满二氧化碳,分别加入等量的饱和石灰水(1号)、饱和氢氧化钠溶液(2号),拧紧瓶盖,振荡,塑料瓶变瘪的情况如图所示。实验过程中同学们还发现石灰水变浑浊后,很快又变澄清了。

【提出问题】1 为什么两个塑料瓶变瘪程度不同?
2 为什么石灰水变浑浊后又变澄清?
3 两个塑料瓶中溶液的成分是什么?
【查阅资科】碳酸钙与水、二氧化碳反应生成能溶于水的碳酸氢钙。
【对比分析】
(1)氢氧化钠易溶于水,氢氧化钙
(2)石灰水与二氧化碳反应变浑浊后,碳酸钙继续与水、二氧化碳反应,根据化学方程式可以推出生成物碳酸氢钙的化学式:

【猜想假设】2号塑料瓶中溶液成分可能是(1)Na2CO3
(2)Na2CO3和
【实验验证】
| 实验操作 | 现象 | 结论 | |
| 甲同学 | 取少量液体于试管中,滴加稀盐酸 | 无明显现象 | 猜想1和2均不正确 |
| 乙同学 | (1)取少量液体于试管中,滴加足量 (2)过滤,向滤液中滴加酚酞试液。 | 产生白色沉淀 | 猜想2正确 |
【反思评价】对甲同学的实验操作进行改进,也可以得出与乙同学相同的结论,操作方案和现象是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐1】实验桌上现有一包白色粉末,可能是氢氧化钠、硫酸钠、碳酸钠和氯化铜中的两种或两种以上组成。现将其放入一干净的烧杯M中,加入足量的水后,固体全部溶解得到无色溶液,再滴加几滴无色酚酞,溶液变为红色。
为进一步确定白色粉末的成分,同学们进行了如下探究。
【查阅资料】氯化钡溶液和硫酸钠溶液呈中性。
【讨论猜想】经过分析,针对白色粉末的组成,大家提出如下猜想:
小红:氢氧化钠、硫酸钠; 小华:__________________ ;
小明:碳酸钠、硫酸钠; 小亮:氢氧化钠、碳酸钠和硫酸钠。
【实验分析】四位同学共同设计并进行了如下实验:
实验完毕后,同学们将试管A、B中的物质倒在同一个烧杯中,然后过滤,滤液中除酚酞外一定还含有的溶质有______ 。
为进一步确定白色粉末的成分,同学们进行了如下探究。
【查阅资料】氯化钡溶液和硫酸钠溶液呈中性。
【讨论猜想】经过分析,针对白色粉末的组成,大家提出如下猜想:
小红:氢氧化钠、硫酸钠; 小华:
小明:碳酸钠、硫酸钠; 小亮:氢氧化钠、碳酸钠和硫酸钠。
【实验分析】四位同学共同设计并进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取烧杯M中的少量溶液于试管A中,向其中加入一定量的稀盐酸 | 溶液由红色变为无色且有气泡产生 | |
| 2.另取烧杯M中的少量溶液于另一试管B中,向其中加入过量氯化钡溶液 | 小亮的猜想正确 | |
| 3.继续向试管B中加入过量的稀盐酸 |
实验完毕后,同学们将试管A、B中的物质倒在同一个烧杯中,然后过滤,滤液中除酚酞外一定还含有的溶质有
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】某实验小组的同学在加热铜与浓硫酸的混合物实验时,发现生成了一种无色有刺激性气味的气体和蓝色溶液,小明同学进行如下探究活动。
【查阅资料】
①二氧化硫能使澄清石灰水变浑浊,二氧化硫能使品红溶液褪色而二氧化碳不能。
②硫酸铜溶于水后,溶液呈酸性。
③某些不活泼的金属(如铜)能与一些强氧化性的酸(如浓硫酸)发生反应,生成水而不生成氢气,同时生成氧化物和含铜离子的盐。
探究一:该无色有刺激性气味的气体的成分:
小明说:该气体可能是氢气、氧气、二氧化碳、二氧化硫中的一种;
小华说:不可能是二氧化碳,原因是______ ;不可能是氢气或氧气,因为______ ;
【实验探究】小明将气体通入品红溶液,观察到______ ,该气体为二氧化硫;
探究二:上述蓝色溶液中有无硫酸剩余;
【实验论证】小坤认为可向蓝色溶液中滴加氯化钡溶液,观察有无沉淀产生,经大家讨论后,该方案被否定,你觉得否定该方案的理由是____________ ,写出铜与浓硫酸共热的化学方程式_______________________________________________________ 。
(注意:答对以下小题将奖励4分,但化学试卷总分不超过60分)
【反思评价】
①有同学提出:能否用石蕊试液来检验蓝色溶液中是否含有硫酸呢?你的回答是______ (填“可以”或“不可以”),理由_____________________________________ 。
②同学们发现,将足量的铜和足量的浓硫酸置于容器中加热,一段时间后,反应会逐渐变慢,最后反应停止,你能说出反应停止的原因吗?
_________________________________________________________
③小东根据化学方程式说,该方法适用与以铜为原料大量制取硫酸铜,小田认为不适用,你能说出小田的一个理由吗?______________________________________________ 。
【查阅资料】
①二氧化硫能使澄清石灰水变浑浊,二氧化硫能使品红溶液褪色而二氧化碳不能。
②硫酸铜溶于水后,溶液呈酸性。
③某些不活泼的金属(如铜)能与一些强氧化性的酸(如浓硫酸)发生反应,生成水而不生成氢气,同时生成氧化物和含铜离子的盐。
探究一:该无色有刺激性气味的气体的成分:
小明说:该气体可能是氢气、氧气、二氧化碳、二氧化硫中的一种;
小华说:不可能是二氧化碳,原因是
【实验探究】小明将气体通入品红溶液,观察到
探究二:上述蓝色溶液中有无硫酸剩余;
【实验论证】小坤认为可向蓝色溶液中滴加氯化钡溶液,观察有无沉淀产生,经大家讨论后,该方案被否定,你觉得否定该方案的理由是
(注意:答对以下小题将奖励4分,但化学试卷总分不超过60分)
【反思评价】
①有同学提出:能否用石蕊试液来检验蓝色溶液中是否含有硫酸呢?你的回答是
②同学们发现,将足量的铜和足量的浓硫酸置于容器中加热,一段时间后,反应会逐渐变慢,最后反应停止,你能说出反应停止的原因吗?
③小东根据化学方程式说,该方法适用与以铜为原料大量制取硫酸铜,小田认为不适用,你能说出小田的一个理由吗?
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐3】某化学兴趣小组的同学为了探究“复分解反应发生的条件”,将CuSO4溶液,NaOH溶液,BaCl2三种溶液两两混合,实验结束后将三根试管中所有废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色。

(1)上述三个反应中不能发生复分解反应的是______ (填字母)。
(2)写出废液混合后使滤液变无色时一定发生的是氢氧化钠和______ (化学式)的反应。
(3)取少量滤液于试管中,滴入酚酞试液,酚酞试液呈红色,该小组的同学认为滤液成分一定有______ (化学式)。除上述成分外,对滤液中其余溶质的成分继续进行了如下探究实验:
【作出猜想】猜想I:BaCl2;猜想Ⅱ:______ 。
【实验探究】
(4)【交流拓展】要使蓝色溶液变成无色,还可以用不同于上述原理的化学方法,即在蓝色溶液中加入______ 。

(1)上述三个反应中不能发生复分解反应的是
(2)写出废液混合后使滤液变无色时一定发生的是氢氧化钠和
(3)取少量滤液于试管中,滴入酚酞试液,酚酞试液呈红色,该小组的同学认为滤液成分一定有
【作出猜想】猜想I:BaCl2;猜想Ⅱ:
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 实验①:取少量滤液于试管中,加入适量的纯碱溶液,振荡 | 产生白色沉淀 | 猜想I成立 |
| 实验②: | 无明显现象 | 猜想Ⅱ不成立 |
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】足球比赛中让意外昏迷的球员快速恢复意识会用到“嗅盐”。同学们对“嗅盐”产生了好奇,并对其成分进行如下探究。
【查阅资料】
①嗅盐是一种由盐类和香料配制而成的药品,给人闻后有刺激作用。
②氯化钙稀溶液与碳酸氢铵稀溶液不发生反应
【提出问题】嗅盐中盐类物质是什么?
一、“嗅盐”的组成探究:
(1)甲同学:取适量“嗅盐”于试管中,加入______ (填一种物质)混合研磨,扇闻,可闻到氨味,说明“嗅盐”中含NH4+。
(2)乙同学:取适量“嗅盐”于试管中,加入______ ,并将生成的气体通入澄清石灰水 ,观察到的现象是_______ ,出现该现象的原因是(用化学方程式表示):______ ,说明“嗅盐”中含CO32-。
(3)丙同学认为乙同学的实验结论不严谨。丙同学通过补做一个实验(见图1),观察到的现象是__ ,由此排除嗅盐中含HCO3-的可能性,进而确认了乙同学的结论。
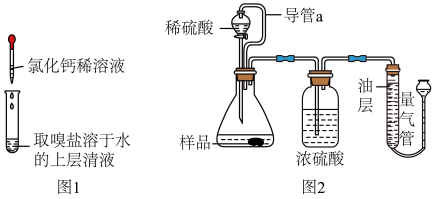
二、“嗅盐”中碳酸铵含量的探究:
称取6.0克样品,用图2装置进行实验(每步反应均充分),利用量气管获得的气体体积来进行计算。
(4)量气管内水面上的油层起的作用是_____ 。
(5)该方案实验结束后,会有气体残留,不能完全进入量气管中,__________ (填“需要”或“不需要”)通入N2将其中残留的气体排入量气管中。
(6)实验测得量气管中产生气体的体积为558mL,该方案所测嗅盐中碳酸铵的质量分数为____ (CO2的密度约为1.97g/L)
【实验反思】
(7)如果图2装置中无导管a,则测得的碳酸铵的质量分数会____ (填“偏大”、“不变”或“偏小”)。
【查阅资料】
①嗅盐是一种由盐类和香料配制而成的药品,给人闻后有刺激作用。
②氯化钙稀溶液与碳酸氢铵稀溶液不发生反应
【提出问题】嗅盐中盐类物质是什么?
一、“嗅盐”的组成探究:
(1)甲同学:取适量“嗅盐”于试管中,加入
(2)乙同学:取适量“嗅盐”于试管中,加入
(3)丙同学认为乙同学的实验结论不严谨。丙同学通过补做一个实验(见图1),观察到的现象是

二、“嗅盐”中碳酸铵含量的探究:
称取6.0克样品,用图2装置进行实验(每步反应均充分),利用量气管获得的气体体积来进行计算。
(4)量气管内水面上的油层起的作用是
(5)该方案实验结束后,会有气体残留,不能完全进入量气管中,
(6)实验测得量气管中产生气体的体积为558mL,该方案所测嗅盐中碳酸铵的质量分数为
【实验反思】
(7)如果图2装置中无导管a,则测得的碳酸铵的质量分数会
您最近一年使用:0次
【推荐2】带着对钠电池开发的期待,某同学对钠及其化合物开展了系列探究。
【探究一】钠和水的反应
取一小块钠,放入50mL水中,观察到钠浮在水面做不规则游动,变成闪亮的小球,发出“嘶嘶”声响,偶尔气体爆鸣并火光闪现,小球变小最后消失。用pH传感器和温度传感器分别获得相关变化曲线如图所示。

(1)根据上图,该反应属于___________ (填“放热”或“吸热”)反应,反应后溶液呈___________ (填“酸”“中”或“碱”)性。
(2)根据上述现象写出钠的一条物理性质:___________ (合理即可)。
(3)反应的化学方程式为___________ 。
【探究二】久置氢氧化钠的变质情况。
【提出问题】①氢氧化钠是否变质?②氢氧化钠是部分变质还是完全变质?
【查阅资料】①氯化钙溶液呈中性:
②向氢氧化钠和碳酸钠混合物中加入盐酸时,盐酸先与氢氧化钠反应,再与碳酸钠反应。
【设计实验】探究氢氧化钠固体的变质情况
(1)小红同学取少量该固体样品置于试管中,向其中加入少量稀盐酸,无明显变化,她认为该样品没有发生变质。你认为她说的是否正确,理由是___________ 。
(2)为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如下表所示的实验,请将下表填写完整。
【探究一】钠和水的反应
取一小块钠,放入50mL水中,观察到钠浮在水面做不规则游动,变成闪亮的小球,发出“嘶嘶”声响,偶尔气体爆鸣并火光闪现,小球变小最后消失。用pH传感器和温度传感器分别获得相关变化曲线如图所示。

(1)根据上图,该反应属于
(2)根据上述现象写出钠的一条物理性质:
(3)反应的化学方程式为
【探究二】久置氢氧化钠的变质情况。
【提出问题】①氢氧化钠是否变质?②氢氧化钠是部分变质还是完全变质?
【查阅资料】①氯化钙溶液呈中性:
②向氢氧化钠和碳酸钠混合物中加入盐酸时,盐酸先与氢氧化钠反应,再与碳酸钠反应。
【设计实验】探究氢氧化钠固体的变质情况
(1)小红同学取少量该固体样品置于试管中,向其中加入少量稀盐酸,无明显变化,她认为该样品没有发生变质。你认为她说的是否正确,理由是
(2)为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如下表所示的实验,请将下表填写完整。
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
| 取少量该固体样品溶于水配成溶液,滴加足量的氯化钙溶液,充分反应后过滤 | 有关反应的化学方程式为 | ||
| 检验样品中是否还含有氢氧化钠 | 向过滤后的滤液中滴入 | 该样品中还含有氢氧化钠 |
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐3】某化学兴趣小组同学往NaOH溶液中滴加无色酚酞溶液时,发现溶液变成红色,可是过了一会儿红色消失,重新恢复为无色。于是该小组在老师指导下对这一现象进行了探究。
【提出问题】溶液的红色为什么会变成无色呢?
【猜想与假设】
猜想一:可能是所用的酚酞溶液变质了
猜想二:可能是NaOH与空气中的CO2反应了。
猜想三:可能是酚酞与空气中的O2反应了。
猜想四:可能是与NaOH溶液浓度大小有关。
【讨论交流】
小组同学集体讨论后认为猜想一_____ (填“合理”或“不合理”),原因是_____ 。
【查阅资料】
NaOH与空气中的CO2反应,生成Na2CO3。Na2CO3俗称纯碱,溶液呈碱性,pH约为10~11.9,能使酚酞溶液变红,且红色不会消失。所以猜想二_____ (填“正确”或“错误”)
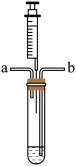
【设计并实验】
(1)为了验证猜想三,小组同学先往如图装有NaOH溶液的试管中,从b处通入密度比空气大的稀有气体一段时间,目的是_____ 。然后通过注射器滴入无色酚酞溶液,观察到溶液变成红色,过一会儿红色仍然消失。则猜想三_____ 。(填“正确”或“错误”)
(2)为了验证猜想四,小组同学继续进行实验探究,并得出了实验结论,请你帮助该小组完成下表。
【拓展延伸】
小组同学百度“酚酞”得知,酚酞(以H2In表示)其实是一种极弱的酸,遇碱溶液变红的变化可表示为:H2In(无色)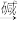 In2-(红色),据此信息写出H2In与NaOH溶液反应的化学反应方程式
In2-(红色),据此信息写出H2In与NaOH溶液反应的化学反应方程式_____ 。
【提出问题】溶液的红色为什么会变成无色呢?
【猜想与假设】
猜想一:可能是所用的酚酞溶液变质了
猜想二:可能是NaOH与空气中的CO2反应了。
猜想三:可能是酚酞与空气中的O2反应了。
猜想四:可能是与NaOH溶液浓度大小有关。
【讨论交流】
小组同学集体讨论后认为猜想一
【查阅资料】
NaOH与空气中的CO2反应,生成Na2CO3。Na2CO3俗称纯碱,溶液呈碱性,pH约为10~11.9,能使酚酞溶液变红,且红色不会消失。所以猜想二

【设计并实验】
(1)为了验证猜想三,小组同学先往如图装有NaOH溶液的试管中,从b处通入密度比空气大的稀有气体一段时间,目的是
(2)为了验证猜想四,小组同学继续进行实验探究,并得出了实验结论,请你帮助该小组完成下表。
| 实验操作 | 实验现象 | 实验结论 |
| 在两支相同试管中,分别放入等体积的质量分数为5%和l0%的氢氧化钠溶液,然后分别滴加1-2滴酚酞试液 | 猜想四是正确的。红色褪去变成无色是因为NaOH溶液浓度过大造成的。 |
小组同学百度“酚酞”得知,酚酞(以H2In表示)其实是一种极弱的酸,遇碱溶液变红的变化可表示为:H2In(无色)
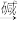 In2-(红色),据此信息写出H2In与NaOH溶液反应的化学反应方程式
In2-(红色),据此信息写出H2In与NaOH溶液反应的化学反应方程式
您最近一年使用:0次



