二氧化锰可作过氧化氢溶液分解的催化剂,兴趣小组想探究过氧化氢分解有没有其他催化剂,以及影响过氧化氢分解速率的因素除催化剂外还有哪些。
Ⅰ.【提出问题】氧化铁能否作过氧化氢分解的催化剂?如果能,其催化效果如何?
【实验探究】
【实验结论】
(1)步骤②证明氧化铁的___ 在反应前后没有发生变化;③中如果a=___ ,证明氧化铁的___ 在反应前后没有发生变化。由①②③可知,氧化铁可以作过氧化氢分解的催化剂。
(2)写出试管A中发生反应的文字表达式___ 。
【实验评价】
设计实验步骤④的目的是___ ,若观察到D试管中产生气泡的速率比C试管中快,由此可以得到的结论是___ 。
Ⅱ.探究过氧化氢溶液浓度对过氧化氢分解速率的影响。
【交流讨论】可以通过测定相同条件下不同浓度过氧化氢溶液___ 来探究。
A 产生相同体积氧气的时间 B 产生氧气的总体积 C 单位时间内产生氧气的体积
【实验探究】
按图1装置进行实验:水浴温度控制在21℃,二氧化锰均为0.5g,过氧化氢溶液均为5mL,三颈瓶容积为250mL,恒压漏斗(漏斗的支管与三颈瓶相连)的作用是使过氧化氢溶液自行下滴。数字传感器数据绘制图像如图2、图3。
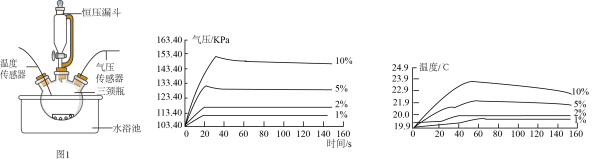
【实验结论】
图2说明过氧化氢溶液浓度与反应速率之间的关系是____ ,结合图3,以10%H2O2溶液为例分析,三颈瓶内气压后来慢慢降低的原因是_____ 。
Ⅰ.【提出问题】氧化铁能否作过氧化氢分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| ①分别取5mL5%过氧化氢溶液放入A、B两支试管中,向A中加入1g氧化铁粉末,并分别在A、B试管中插入带火星的木条,观察现象。 | A试管中产生气泡,带火星的木条复燃,B试管中无明显现象。 |
| ②待A中没有现象发生时,重新加入过氧化氢溶液,把带火星的木条伸入试管,如此反复3次。 | 试管中均产生气泡,带火星的木条均复燃。 |
| ③将步骤②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量为ag。 | |
| ④分别取5mL5%过氧化氢溶液放入C、D两支试管中,向C中加入1g氧化铁粉末,向D中加入1g二氧化锰粉末,观察现象。 |
【实验结论】
(1)步骤②证明氧化铁的
(2)写出试管A中发生反应的文字表达式
【实验评价】
设计实验步骤④的目的是
Ⅱ.探究过氧化氢溶液浓度对过氧化氢分解速率的影响。
【交流讨论】可以通过测定相同条件下不同浓度过氧化氢溶液
A 产生相同体积氧气的时间 B 产生氧气的总体积 C 单位时间内产生氧气的体积
【实验探究】
按图1装置进行实验:水浴温度控制在21℃,二氧化锰均为0.5g,过氧化氢溶液均为5mL,三颈瓶容积为250mL,恒压漏斗(漏斗的支管与三颈瓶相连)的作用是使过氧化氢溶液自行下滴。数字传感器数据绘制图像如图2、图3。

【实验结论】
图2说明过氧化氢溶液浓度与反应速率之间的关系是
更新时间:2019-10-12 07:20:36
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】关于低化剂的研究是一项重要的课题,某小组以“探究催化剂的奥密”为题展开了项目化学习。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法不正确的是_______ (填字母)。
【任务二】探究催化剂
(2)查阅资料发现氧化铜也可以作为过氧化氢分解的催化剂,于是进行相应的探究。称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如图所示实验。
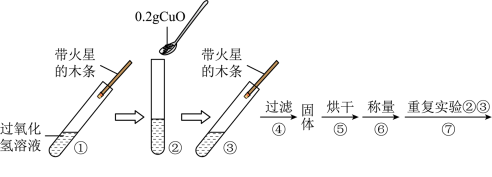
写出上述反应的化学方程式_________ ,步骤⑦的作用________ 。
【任务三】探究催化剂的催化效果
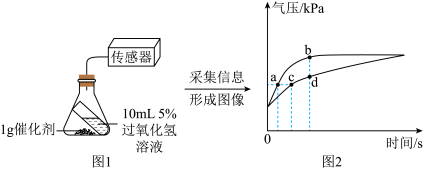
分别取10mL5%过氧化氢溶液、1g二氧化锰、1g氧化铜,按图1所示装置进行实验,实验时倾斜锥形瓶使过氧化氢溶液与催化剂完全接触,测得相同条件下瓶内气压的变化如图2所示。
(3)对比分析图2中的_______ (填字母)点,可知化学反应速率与催化剂的种类有关。
(4)请从催化剂的角度解释在实验过程中,上述两个反应虽化学反应速率不同,但完全反应后两个装置内压强相同的原因是________ 。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法不正确的是
| A.用作催化剂的物质还可能是其他反应的反应物成生成物 |
| B.在化学反应前后催化剂的质量和化学性质都不发生改变 |
| C.不加入催化剂化学反应就一定不能发生 |
| D.一个化学反应可能有多种催化剂 |
【任务二】探究催化剂
(2)查阅资料发现氧化铜也可以作为过氧化氢分解的催化剂,于是进行相应的探究。称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如图所示实验。

| 步骤①现象 | 步骤⑥结果 | 步骤⑦现象 | 实验结论 |
| 试管中有极少量的气泡产生,带火星的木条没有复燃 | 称得氧化铜的质量为 | 氧化铜是过氧化氢分解反应的催化剂 |
【任务三】探究催化剂的催化效果

分别取10mL5%过氧化氢溶液、1g二氧化锰、1g氧化铜,按图1所示装置进行实验,实验时倾斜锥形瓶使过氧化氢溶液与催化剂完全接触,测得相同条件下瓶内气压的变化如图2所示。
(3)对比分析图2中的
(4)请从催化剂的角度解释在实验过程中,上述两个反应虽化学反应速率不同,但完全反应后两个装置内压强相同的原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】实验室常用加热氯酸钾和少量二氧化锰的混合物的方法制取氧气,写出该反应的符号表达式______________ 。
小明发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是他进行了如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表完成实验并记录数据:分解温度(分解温度越低,催化效果越好)。
【分析数据、得出结论】
(1)通过实验__________ 与实验④对比,证明小明的猜想是合理的。
(2)实验所用的三种物质,催化效果由好到差的顺序是____________________ 。
【反思】
(1)如果要证明氧化铁是该反应的催化剂,还要验证氧化铁的______ 和____________ 在反应前后不变。
(2)当使用同种催化剂时,可能影响催化效果的因素有____________________________ 。
小明发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是他进行了如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表完成实验并记录数据:分解温度(分解温度越低,催化效果越好)。
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | 氯酸钾 | 580 |
| ② | 氯酸钾、二氧化锰(质量比1:1) | 350 |
| ③ | 氯酸钾、氧化铜(质量比l:1) | 370 |
| ④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
(1)通过实验
(2)实验所用的三种物质,催化效果由好到差的顺序是
【反思】
(1)如果要证明氧化铁是该反应的催化剂,还要验证氧化铁的
(2)当使用同种催化剂时,可能影响催化效果的因素有
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某研究小组对过氧化氢溶液制取氧气进行如下探究:
【实验一】氧气制取和性质实验。现有如图1装置:
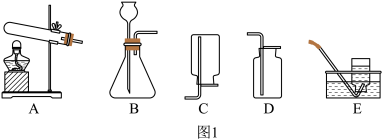
(1)实验室用过氧化氢溶液制氧气的化学方程式为__________ ,应选择的发生装置是_________ 。(填标号,下同),收集装置是_________ 。
(2)用收集的氧气进行“铁丝在氧气中燃烧”的实验,观察到的现象是_________ 。
【实验二】探究H2O2质量分数、温度对反应速率的影响:
设计如下表实验方案:
(3)实验①和③的实验目的是_____________ 。
【实验三】探究制取氧气的适宜催化剂。
实验方案如下:
I.用等质量的MnO2、CuO、Fe2O3、Cr2O3四种催化剂粉末分别与海藻酸钠溶液混合,滴入氯化钙溶液制成颗粒表面积相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海藻酸钠微球,采用图2装置进行实验。改用其他三种微球,分别重复上述实验,得到图3的锥形瓶内压强随时间变化的曲线图。
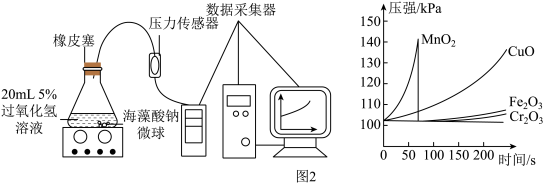
(4)每次实验时,海藻酸钠微球数应相同的原因__________ 。
(5)用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是_________ 。
(6)从实验曲线看,催化效果较好、反应温和的催化剂是_________ 。
【实验一】氧气制取和性质实验。现有如图1装置:

(1)实验室用过氧化氢溶液制氧气的化学方程式为
(2)用收集的氧气进行“铁丝在氧气中燃烧”的实验,观察到的现象是
【实验二】探究H2O2质量分数、温度对反应速率的影响:
设计如下表实验方案:
| 实验序号 | H2O2质量分数/% | 温度/℃ | 每分钟气泡数 |
| ① | 30 | 30 | |
| ② | 30 | 20 | |
| ③ | 15 | 30 |
【实验三】探究制取氧气的适宜催化剂。
实验方案如下:
I.用等质量的MnO2、CuO、Fe2O3、Cr2O3四种催化剂粉末分别与海藻酸钠溶液混合,滴入氯化钙溶液制成颗粒表面积相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海藻酸钠微球,采用图2装置进行实验。改用其他三种微球,分别重复上述实验,得到图3的锥形瓶内压强随时间变化的曲线图。

(4)每次实验时,海藻酸钠微球数应相同的原因
(5)用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是
(6)从实验曲线看,催化效果较好、反应温和的催化剂是
您最近一年使用:0次
【推荐1】某化学研究性学习小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白。
[提出问题]Al2O3能不能作过氧化氢分解的催化剂呢?
[作出猜想]Al2O3能作过氧化氢分解的催化剂。
[实验验证]填写表中实验一的步骤和实验二的结论
[得出结论]Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂:写出该反应的文字表达式_____ ;该反应属于____ 反应 (填基本反应类型)。
[反思提高]经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验三:
实验三:
[实验目的]探究_____ 。
[实验步骤]
①正确称取Al2O3的质量(少量);
②按实验二的步骤完成实验;
③待反应结束,将试管中的物质进行过滤,洗涤,烘干,称量;
④对比反应前后Al2O3的质量。
[交流讨论]如果Al2O3在反应前后质量不变,则说明Al2O3是过氧化氢分解的催化剂。
[提出新问题]小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验四:
[实验四目的]探究___
[提出问题]Al2O3能不能作过氧化氢分解的催化剂呢?
[作出猜想]Al2O3能作过氧化氢分解的催化剂。
[实验验证]填写表中实验一的步骤和实验二的结论
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 有少量气泡放出,木条不复燃。 | 常温下过氧化氢溶液分解速率很慢。 | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中。 | 加入Al2O3后过氧化氢溶液分解速率很快。 |
[得出结论]Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂:写出该反应的文字表达式
[反思提高]经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验三:
实验三:
[实验目的]探究
[实验步骤]
①正确称取Al2O3的质量(少量);
②按实验二的步骤完成实验;
③待反应结束,将试管中的物质进行过滤,洗涤,烘干,称量;
④对比反应前后Al2O3的质量。
[交流讨论]如果Al2O3在反应前后质量不变,则说明Al2O3是过氧化氢分解的催化剂。
[提出新问题]小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验四:
[实验四目的]探究
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组在做“寻找新的催化剂”课题时,发现将生锈的铁钉(氧化铁与铁的混合物)放到过氧化氢溶液中,也可以加快过氧化氢的分解速率。于是,他们对此展开探究:
【提出问题】什么物质是该反应的催化剂?
【散出猜想】猜想一:氧化铁 猜想二:铁
【实验与结论】
(1)请回答下列问题。
【讨论交流】
(2)同学们认为实验1还不能准确地说明氧化铁是过氧化氢分解制氧气的催化剂,理由是________ 。
(3)实验改进后,证明氧化铁就是该反应的催化剂,写出该反应的文字表达式:_______ 。
【拓展探究】利用数字化实验探究不同催化剂的催化效果。分别取20mL浓度为5%的过氧化氢溶液、0.5g二氧化锰、0.5g氧化铁,按图1所示装置进行实验,实验时倾斜锥形瓶使过氧化氢溶液与催化剂接触,瓶内气压的变化如图2所示。

(4)对比分析图2中的_______ 点,可知化学反应速率与催化剂的种类有关。
(5)请从催化剂的角度解释上述两个反应里化学反应速率不同,但完全反应后两个装置内压强相同的原因:________ 。
【提出问题】什么物质是该反应的催化剂?
【散出猜想】猜想一:氧化铁 猜想二:铁
【实验与结论】
(1)请回答下列问题。
| 实验操作 | 实验现象 | 实验结论 |
| 实验Ⅰ:将ag氧化铁粉末加入到装有10mL5%过氧化氢溶液的试管中,并用一根带火星的木条置于试管内,观察现象。 | 猜想一成立 | |
| 实验Ⅱ:将ag铁粉加入到装有10mL5%过氧化氢溶液的试管中,并用一根带火星的木条置于试管内,观察现象。 | 无明显现象 | 猜想二 |
【讨论交流】
(2)同学们认为实验1还不能准确地说明氧化铁是过氧化氢分解制氧气的催化剂,理由是
(3)实验改进后,证明氧化铁就是该反应的催化剂,写出该反应的文字表达式:
【拓展探究】利用数字化实验探究不同催化剂的催化效果。分别取20mL浓度为5%的过氧化氢溶液、0.5g二氧化锰、0.5g氧化铁,按图1所示装置进行实验,实验时倾斜锥形瓶使过氧化氢溶液与催化剂接触,瓶内气压的变化如图2所示。

(4)对比分析图2中的
(5)请从催化剂的角度解释上述两个反应里化学反应速率不同,但完全反应后两个装置内压强相同的原因:
您最近一年使用:0次
【推荐3】学习了MnO2对过氧化氢的分解有催化作用的知识后。某同学想:Fe2O3对过氧化氢的分解能否起到类似MnO2的催化作用呢?于是进行了如下探究。
【查阅资料】Fe2O3难溶于水
【猜想】I. Fe2O3不能改变过氧化氢的分解速率、也不参与反应,反应前后质量和化学性质不变;
II. Fe2O3参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ. Fe2O3是反应的催化剂。
【实验】用天平称量m1g Fe2O3,取5mL5%的过氧化氢溶液于试管中,进行下图所示实验:

(1)回答下表中问题:
(2)步骤__________ (填2个步骤序号)对比的目的是证明Fe2O3能加快过氧化氢溶液分解的速率。
(3)步骤⑦的目的是___________________________________________ 。
(4)过氧化氢能被Fe2O3催化分解放出氧气的符号表达式为________________________ ,该反应的基本反应类型是__________ 。
【查阅资料】Fe2O3难溶于水
【猜想】I. Fe2O3不能改变过氧化氢的分解速率、也不参与反应,反应前后质量和化学性质不变;
II. Fe2O3参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ. Fe2O3是反应的催化剂。
【实验】用天平称量m1g Fe2O3,取5mL5%的过氧化氢溶液于试管中,进行下图所示实验:

(1)回答下表中问题:
| 步骤③的现象 | 步骤⑥的结果 | 步骤⑦的现象 | 结论 |
| A.有大量气泡产生; B.带火星的木条复燃 | m2 (填“大于”、“小于”或“等于”) | A.有大量气泡产生; B. | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立。 |
(3)步骤⑦的目的是
(4)过氧化氢能被Fe2O3催化分解放出氧气的符号表达式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】茶垢清洁剂能快速清除茶具上附着的茶垢。某小组同学对茶垢清洁剂进行探究。
主要成分:过碳酸钠(化学式为: )
)
去渍原理:过碳酸钠溶于水有气体产生,受热易分解,具有Na2CO3和H2O2的双重性质,Na2CO3溶液有较好的去污效果,H2O2分解生成活性氧,可深层带走污垢。
【提出问题1】茶垢清洁剂溶于水生成的气体成分是什么?
【猜想与假设】小华说:该气体可能是CO2、O2、N2。
(1)小明说:不可能含有N2,因为_______________ 。
【实验验证】将产生的气体通入澄清石灰水,石灰水不变浑浊,气体带火星的木条复燃,说明该气体是O2。
【提出问题2】茶垢清洁剂的使用效果是否与温度有关?
研究小组向两个装有10g茶垢清洁剂的抽滤瓶中,分别注入5mL的冷水、热水,实验装置如图1所示,氧气浓度传感器采集的数据如图2所示。________________ 。
(3)茶垢清洁剂清洗茶垢时,用______ (填“冷水”或“热水”)的效果更好。
【提出问题3】茶垢清洁剂如何保存?
(4)下列物质能与茶垢清洁剂溶液反应使其变质的是______(填序号)。
(5)茶垢清洁剂在保存时需要注意______ 。
【提出问题4】茶垢清洁剂溶于水时生成碳酸钠,是否还生成了氢氧化钠?取茶垢清洁剂的水溶液,按如图流程进行实验。______________ 。
主要成分:过碳酸钠(化学式为:
 )
)去渍原理:过碳酸钠溶于水有气体产生,受热易分解,具有Na2CO3和H2O2的双重性质,Na2CO3溶液有较好的去污效果,H2O2分解生成活性氧,可深层带走污垢。
【提出问题1】茶垢清洁剂溶于水生成的气体成分是什么?
【猜想与假设】小华说:该气体可能是CO2、O2、N2。
(1)小明说:不可能含有N2,因为
【实验验证】将产生的气体通入澄清石灰水,石灰水不变浑浊,气体带火星的木条复燃,说明该气体是O2。
【提出问题2】茶垢清洁剂的使用效果是否与温度有关?
研究小组向两个装有10g茶垢清洁剂的抽滤瓶中,分别注入5mL的冷水、热水,实验装置如图1所示,氧气浓度传感器采集的数据如图2所示。

(3)茶垢清洁剂清洗茶垢时,用
【提出问题3】茶垢清洁剂如何保存?
(4)下列物质能与茶垢清洁剂溶液反应使其变质的是______(填序号)。
| A.硫酸钠 | B.稀盐酸 | C.石灰水 | D.二氧化锰 |
(5)茶垢清洁剂在保存时需要注意
【提出问题4】茶垢清洁剂溶于水时生成碳酸钠,是否还生成了氢氧化钠?取茶垢清洁剂的水溶液,按如图流程进行实验。

您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】无明显现象反应的可视化是一项重要的课题,某小组以“探究二氧化碳与氢氧化钠是否反应”为主题展开化学反应可视化的项目式学习。
【任务一】证明反应物的减少或消失
(1)实验一:一体化实验
该小组同学利用图4所示装置按照下列步骤展开探究。

步骤1:关闭K1,打开K2、K3,将2mL稀硫酸迅速全部注入注射器C中。
步骤2:拉动注射器B的活塞至18mL,关闭K3。
步骤3:打开K1,将2mL氢氧化钠溶液注入注射器B中,关闭K1,充分振荡,观察现象。
通过上述实验,能证明氢氧化钠溶液与二氧化碳反应的现象是______ ;二氧化碳与氢氧化钠反应的化学方程式为______ 。
(2)实验二:数字化实验

按照图5所示进行实验,将针筒内的水和氢氧化钠溶液同时注入装满二氧化碳的烧瓶中,振荡测得两烧瓶内气压随时间变化的趋势如图6所示,则曲线______ (填“Ⅰ”或“Ⅱ”)表示氢氧化钠溶液与二氧化碳的反应;向二氧化碳中加入20mL蒸馏水的目的是______ 。
【任务二】证明有新物质生成
(3)实验三:产物转化法实验
完成下列表格:
实验反思:第二组实验向溶液中滴加稀盐酸时,起初并无明显现象。滴加稀盐酸一段时间后有气泡产生,可能的原因是______ 。
(4)实验四:绿色化实验
查阅资料:①乙醇不与NaOH、Na2CO3、CO2反应
②25°C时,NaOH和Na2CO3在乙醇中的解度如表:
进行实验:如图7所示,取2mL4%的氢氧化钠的乙醇溶流于试管中,向试管中吹气约30秒。观察现象。

实验现象:______ 。
实验结论:氢氧化钠与二氧化碳发生了反应。
【实验总结】对无明显现象的反应,证明反应发生的方法,常见思路:
①证明反应物减少或消失;②证明______ 。
【任务一】证明反应物的减少或消失
(1)实验一:一体化实验
该小组同学利用图4所示装置按照下列步骤展开探究。

步骤1:关闭K1,打开K2、K3,将2mL稀硫酸迅速全部注入注射器C中。
步骤2:拉动注射器B的活塞至18mL,关闭K3。
步骤3:打开K1,将2mL氢氧化钠溶液注入注射器B中,关闭K1,充分振荡,观察现象。
通过上述实验,能证明氢氧化钠溶液与二氧化碳反应的现象是
(2)实验二:数字化实验

按照图5所示进行实验,将针筒内的水和氢氧化钠溶液同时注入装满二氧化碳的烧瓶中,振荡测得两烧瓶内气压随时间变化的趋势如图6所示,则曲线
【任务二】证明有新物质生成
(3)实验三:产物转化法实验
完成下列表格:
实验步骤 | 实验现象 | 实验结论 | |
第一组 | 向氢氧化钠溶液中通入二氧 化碳,振荡,再往溶液中滴 加足量 | 有白色沉淀生成 | 氢氧化钠溶液与二 氧化碳发生了反应 |
第二组 | 向氢氧化钠溶液中通入二氧 化碳,振荡,再往溶液中滴 加足量的稀盐酸 |
(4)实验四:绿色化实验
查阅资料:①乙醇不与NaOH、Na2CO3、CO2反应
②25°C时,NaOH和Na2CO3在乙醇中的解度如表:
物质 | NaOH | Na2CO3 |
溶解度/g | 17.3 | <0.1 |

实验现象:
实验结论:氢氧化钠与二氧化碳发生了反应。
【实验总结】对无明显现象的反应,证明反应发生的方法,常见思路:
①证明反应物减少或消失;②证明
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】化学兴趣小组利用图1装置探究磷在空气中燃烧后氧气浓度的变化。
【提出问题】
足量红磷在密闭的图1容器内燃烧,火焰熄灭后,容器内是否有氧气剩余?
【猜想假设】
猜想1:有氧气剩佘;
猜想2:无氧气剩余。
【实验验证】
按图1组装好实验装置,利用高能激光笔照射燃烧匙上的足量红磷,红磷燃烧直至熄灭;待装置完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。____ 。
(2)激光笔的作用是___ 。
(3)红磷燃烧产物与瓶底热水反应生成磷酸(H3PO4)的化学方程式是____ 。
(4)实验过程中,燃烧匙内的白磷先未燃着的原因是_____ 。
【得出结论】
(5)结论1:猜想___ 正确。
(6)结论2:图2上用“燃烧红磷测定空气中氧气的含量”的方法是____ (填“严谨”或“不严谨”)的,其理由是____ 。
【拓展延伸】
图3是该小组同学在整个实验过程中,用氧气传感器测定容器内氧气浓度变化的曲线图。
(7)在图3中,___ (填“A”“B”“C”“D”或“E”)点为红磷熄灭。
(8)请你解释曲线CD段、DE段氧气浓度变化的主要原因:①CD段:___ ;②DE段:____ 。
【提出问题】
足量红磷在密闭的图1容器内燃烧,火焰熄灭后,容器内是否有氧气剩余?
【猜想假设】
猜想1:有氧气剩佘;
猜想2:无氧气剩余。
【实验验证】
按图1组装好实验装置,利用高能激光笔照射燃烧匙上的足量红磷,红磷燃烧直至熄灭;待装置完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。

(2)激光笔的作用是
(3)红磷燃烧产物与瓶底热水反应生成磷酸(H3PO4)的化学方程式是
(4)实验过程中,燃烧匙内的白磷先未燃着的原因是
【得出结论】
(5)结论1:猜想
(6)结论2:图2上用“燃烧红磷测定空气中氧气的含量”的方法是
【拓展延伸】
图3是该小组同学在整个实验过程中,用氧气传感器测定容器内氧气浓度变化的曲线图。
(7)在图3中,
(8)请你解释曲线CD段、DE段氧气浓度变化的主要原因:①CD段:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】只有氧气才能支持燃烧吗?某学习小组对这个问题进行如下探究。
【查阅资料】钠是一种银白色的金属,能与空气中的氧气或水蒸气反应。
【提出问题1】除氧气外,是否还有其他物质也能支持燃烧?
【进行实验一】如图,向盛有金属钠(Na)的硬质玻璃管中通入纯净、干燥的CO2,当观察到澄清石灰水中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,钠剧烈燃烧,产生白烟,燃烧结束后硬质玻璃管中有黑色颗粒和白色固体生成。
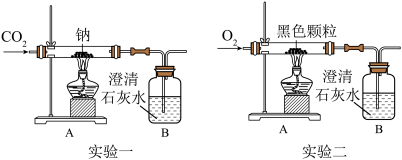
【得出结论】
(1)二氧化碳___________ (选填“能”或“不能”)支持某些物质燃烧。
【反思评价】
(2)点燃酒精灯前,要先向玻璃管中通入一段时间的CO2,其目的是____________ 。
【提出问题2】黑色颗粒和白色固体是什么? .
【猜想与假设】
(3)黑色颗粒可能是________ (用化学式填写)。
【进行实验二】
(4)现象:黑色颗粒逐渐减少,澄清石灰水____________ 。
【得出结论】实验二证明:黑色颗粒的猜想是正确的。
【猜想与假设】
(5)某同学对白色固体的成分做出猜想:①碳酸钠( Na2CO3);②氢氧化钠( NaOH)。你认为猜想_____ (填序号)一定是错误的,理由是__________ 。
【拓展延伸】
(6)通过以上研究,你对CO2有何新认识?
【查阅资料】钠是一种银白色的金属,能与空气中的氧气或水蒸气反应。
【提出问题1】除氧气外,是否还有其他物质也能支持燃烧?
【进行实验一】如图,向盛有金属钠(Na)的硬质玻璃管中通入纯净、干燥的CO2,当观察到澄清石灰水中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,钠剧烈燃烧,产生白烟,燃烧结束后硬质玻璃管中有黑色颗粒和白色固体生成。

【得出结论】
(1)二氧化碳
【反思评价】
(2)点燃酒精灯前,要先向玻璃管中通入一段时间的CO2,其目的是
【提出问题2】黑色颗粒和白色固体是什么? .
【猜想与假设】
(3)黑色颗粒可能是
【进行实验二】
(4)现象:黑色颗粒逐渐减少,澄清石灰水
【得出结论】实验二证明:黑色颗粒的猜想是正确的。
【猜想与假设】
(5)某同学对白色固体的成分做出猜想:①碳酸钠( Na2CO3);②氢氧化钠( NaOH)。你认为猜想
【拓展延伸】
(6)通过以上研究,你对CO2有何新认识?
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
[查阅资料]
[实验探究]
(1)探究两者水溶液酸碱性的差异:
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变_____ 色,但食用纯碱溶液中颜色更深,由此推测可能____ 溶液碱性更强.
(2)验证两种粉末的稳定性:在老师的指导下,该小组按如图所示装置进行实验操作,观察到___ (填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为___ ,装置中棉花的作用是____ .

[查阅资料]
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
(1)探究两者水溶液酸碱性的差异:
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变
(2)验证两种粉末的稳定性:在老师的指导下,该小组按如图所示装置进行实验操作,观察到

您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。
【作出猜想】
猜想 1.Cr>Fe>Cu;
猜想 2. Fe>Cu >Cr;
猜想 3.你的猜想是_______________ 。
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
【结论与解释】
(1)小聪得到的结论是猜想_______________ 正确。
(2)实验前用砂纸打磨金属片的目的是__________________ 。
【知识运用】
将铬片投入 FeSO4溶液中,反应_________________________ (填“能”或“不能”)进行。
【作出猜想】
猜想 1.Cr>Fe>Cu;
猜想 2. Fe>Cu >Cr;
猜想 3.你的猜想是
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
| 实验 | 试管 1 | 试管 2 | 试管 3 |
实验操作 |  |  |  |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 |
(1)小聪得到的结论是猜想
(2)实验前用砂纸打磨金属片的目的是
【知识运用】
将铬片投入 FeSO4溶液中,反应
您最近一年使用:0次



