在生活生产中,铁的应用非常广泛。
(一)认识铁元素及含铁物质
(1)人体缺铁会导致_____ (选填序号)。
A 佝偻病 B 贫血症 C 甲状腺疾病
(2)铁与铬(Cr)、镍(Ni)等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料。以上叙述中不涉及到_____ (选填序号)。
A 合金 B 无机非金属材料 C 合成材料 D 复合材料
(3)冬季取暖人们常用到暖宝宝,其热量来源于铁的缓慢氧化。已知暖宝宝的主要成分为铁粉、炭粉和少量氯化钠,暖宝宝反应的主要原理是铁粉与氧气、水共同作用生成氢氧化铁,写出反应的化学方程式:_____ ;氯化钠的作用是_____ 。
(二)制备硫酸亚铁铵晶体的探究
硫酸亚铁铵晶体【(NH4)aFeb(SO4)c·xH2O】(俗称摩尔盐晶体)是一种重要的化工原料,用途十分广泛。某化学实验小组制备硫酸亚铁铵晶体并设计实验测定其组成的流程如下:
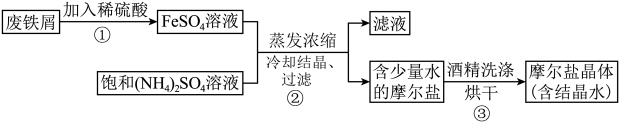
资料:硫酸亚铁铵晶体易溶于水,不溶于乙醇;
(4)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍,碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH_____ 7(填“>”、“=”、“<”)
(5)操作③中使用乙醇汽油洗涤可以快速晾干。这样做的优点是_____ ;
A 避免用水洗涤所造成的晶体损耗
B 酒精易挥发,可低温晾干晶体
C 防止硫酸亚铁被氧化
(三)硫酸亚铁铵晶体分解的定性探究
硫酸亚铁铵晶体受热分解可得到氧化铁。兴趣小组在科研人员指导下设计实验探究硫酸亚铁铵晶体受热分解的产物。
(6)甲组同学设计了如图1所示实验装置:
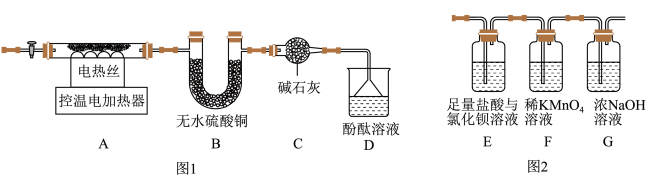
①实验中,装置B中观察到的现象是_____ ;
②装置D中观察到酚酞溶液变红色,由此可知分解的产物中有_____ (写化学式)。
(7)乙组同学认为硫酸亚铁铵晶体受热分解的产物中还有SO2、SO3。为进行验证,用甲组实验中的装置A和上图2所示装置连接进行实验。观察到装置E中有白色沉淀生成,证明了有SO3生成,写出该反应的化学方程式_____ ;而F装置中_____ 、表明生成了SO2。
(四)硫酸亚铁铵晶体成分的定量探究
【实验步骤】:取3份质量均为7.84g的(NH4)aFeb(SO4)c·xH2O晶体,分别进行实验。①向一份中加入过量的NaOH溶液,充分反应后得到0.68gNH3②向另一份中加入过量的BaCl2溶液,充分反应后过滤、洗涤、干燥得到9.32g沉淀③加热第三份晶体使其分解,剩余固体质量与温度的关系如图所示

回答下列问题:
资料:硫酸亚铁铵晶体受热时,在200℃以下只失去结晶水。
(8)实验中加入过量BaCl2溶液的目的_____ ;
(9)根据实验数据,计算硫酸亚铁铵晶体的化学式_____ ;写出A点到B点发生反应的化学方程式_____ 。
(一)认识铁元素及含铁物质
(1)人体缺铁会导致
A 佝偻病 B 贫血症 C 甲状腺疾病
(2)铁与铬(Cr)、镍(Ni)等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料。以上叙述中不涉及到
A 合金 B 无机非金属材料 C 合成材料 D 复合材料
(3)冬季取暖人们常用到暖宝宝,其热量来源于铁的缓慢氧化。已知暖宝宝的主要成分为铁粉、炭粉和少量氯化钠,暖宝宝反应的主要原理是铁粉与氧气、水共同作用生成氢氧化铁,写出反应的化学方程式:
(二)制备硫酸亚铁铵晶体的探究
硫酸亚铁铵晶体【(NH4)aFeb(SO4)c·xH2O】(俗称摩尔盐晶体)是一种重要的化工原料,用途十分广泛。某化学实验小组制备硫酸亚铁铵晶体并设计实验测定其组成的流程如下:

资料:硫酸亚铁铵晶体易溶于水,不溶于乙醇;
(4)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍,碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH
(5)操作③中使用乙醇汽油洗涤可以快速晾干。这样做的优点是
A 避免用水洗涤所造成的晶体损耗
B 酒精易挥发,可低温晾干晶体
C 防止硫酸亚铁被氧化
(三)硫酸亚铁铵晶体分解的定性探究
硫酸亚铁铵晶体受热分解可得到氧化铁。兴趣小组在科研人员指导下设计实验探究硫酸亚铁铵晶体受热分解的产物。
(6)甲组同学设计了如图1所示实验装置:

①实验中,装置B中观察到的现象是
②装置D中观察到酚酞溶液变红色,由此可知分解的产物中有
(7)乙组同学认为硫酸亚铁铵晶体受热分解的产物中还有SO2、SO3。为进行验证,用甲组实验中的装置A和上图2所示装置连接进行实验。观察到装置E中有白色沉淀生成,证明了有SO3生成,写出该反应的化学方程式
(四)硫酸亚铁铵晶体成分的定量探究
【实验步骤】:取3份质量均为7.84g的(NH4)aFeb(SO4)c·xH2O晶体,分别进行实验。①向一份中加入过量的NaOH溶液,充分反应后得到0.68gNH3②向另一份中加入过量的BaCl2溶液,充分反应后过滤、洗涤、干燥得到9.32g沉淀③加热第三份晶体使其分解,剩余固体质量与温度的关系如图所示

回答下列问题:
资料:硫酸亚铁铵晶体受热时,在200℃以下只失去结晶水。
(8)实验中加入过量BaCl2溶液的目的
(9)根据实验数据,计算硫酸亚铁铵晶体的化学式
更新时间:2019-11-16 16:40:09
|
相似题推荐
综合应用题
|
困难
(0.15)
【推荐1】镁及其化合物在生产、生活中有着广泛的应用前景。
(一)镁及其化合物的广泛应用
(1)金属镁可以用于制造信号弹和焰火,因其燃烧时发出____
(2)工业上通过反应: ,得到金属镁,反应中电能转化为
,得到金属镁,反应中电能转化为___ 能
(3)用不锈钢、合成橡胶、氧化镁等材料制造的飞机轮胎属于___ 材料。
(4)用含有Mg(OH)2的药物治疗胃酸过多,该反应的化学方程式为_________ .
(5)碳酸镁可作阻燃剂,其可能的原因是____ (选填序号)。
a 分解时吸热,降低可燃物的着火点
b 生成的固体覆盖燃烧物,隔绝氧气
(二)碳酸镁水合物的制备
MgCO3· 3H2O是制备镁产品的中间体。工业上从碱性卤水(主要成分为MgCl2中获取MgCO3·3H2O的方法如图1所示。


(1)“沉淀”过程的pH随时间的变化如图2所示,其操作为;向卤水中通入CO2至饱和然后滴加NaOH溶液,同时继续通入CO2,由此判断卤水的碱性比NaOH溶液_____ (“强”或“弱”)。
(2)“沉淀”时生成MgCO3 ·3H2O的总反应化学方程式为_____
(3)证明沉淀已经洗涤干净的方法是:取最后一次洗涤所得滤液,先加足量稀HNO3滴加____ 溶液,无现象。
(三)样品成分的分析
在烘干时,会有部分MgCO3·3H2O转化为碱式碳酸镁晶体Mga(OH)b(CO3)c · dH2O.为测定Mga(OH)b(CO3)c · dH2O的组成,称取18.46g固体混合物,在科研人员的指下用下图装置进行热分解实验,并记录实验数据于下表中。

【资料】
①MgCO3·3H2O在190℃完全失去结晶水;MgCO3;在400℃完全分解生成两种氧化物。
②Mga(OH)b(CO3)c · dH2O在210℃以下不分解:450℃完全分解生成三种氧化物。
(1)装配好实验装置后,先要______
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是__
(3)计算a:c=___ ,Mga(OH)b(CO3)c · dH2O中结晶水的质量为___ g
(4)若实验中缺少D装置,则α:c的值____ 选填“偏大”、“偏小”或“不变”
(5)MgCO3·3H2O受热转化为碱式碳酸镁晶体Mga(OH)b(CO3)c · dH2O的化学方程式为______ 。
(一)镁及其化合物的广泛应用
(1)金属镁可以用于制造信号弹和焰火,因其燃烧时发出
(2)工业上通过反应:
 ,得到金属镁,反应中电能转化为
,得到金属镁,反应中电能转化为(3)用不锈钢、合成橡胶、氧化镁等材料制造的飞机轮胎属于
(4)用含有Mg(OH)2的药物治疗胃酸过多,该反应的化学方程式为
(5)碳酸镁可作阻燃剂,其可能的原因是
a 分解时吸热,降低可燃物的着火点
b 生成的固体覆盖燃烧物,隔绝氧气
(二)碳酸镁水合物的制备
MgCO3· 3H2O是制备镁产品的中间体。工业上从碱性卤水(主要成分为MgCl2中获取MgCO3·3H2O的方法如图1所示。


(1)“沉淀”过程的pH随时间的变化如图2所示,其操作为;向卤水中通入CO2至饱和然后滴加NaOH溶液,同时继续通入CO2,由此判断卤水的碱性比NaOH溶液
(2)“沉淀”时生成MgCO3 ·3H2O的总反应化学方程式为
(3)证明沉淀已经洗涤干净的方法是:取最后一次洗涤所得滤液,先加足量稀HNO3滴加
(三)样品成分的分析
在烘干时,会有部分MgCO3·3H2O转化为碱式碳酸镁晶体Mga(OH)b(CO3)c · dH2O.为测定Mga(OH)b(CO3)c · dH2O的组成,称取18.46g固体混合物,在科研人员的指下用下图装置进行热分解实验,并记录实验数据于下表中。

| 温度/℃ | 室温 | 190 | 450 |
| 浓硫酸 | 150.00 | 155.40 | 156.30 |
| 碱石灰 | 100.00 | 100.00 | 106.16 |
①MgCO3·3H2O在190℃完全失去结晶水;MgCO3;在400℃完全分解生成两种氧化物。
②Mga(OH)b(CO3)c · dH2O在210℃以下不分解:450℃完全分解生成三种氧化物。
(1)装配好实验装置后,先要
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是
(3)计算a:c=
(4)若实验中缺少D装置,则α:c的值
(5)MgCO3·3H2O受热转化为碱式碳酸镁晶体Mga(OH)b(CO3)c · dH2O的化学方程式为
您最近一年使用:0次
综合应用题
|
困难
(0.15)
解题方法
【推荐2】钙元素是一种重要的金属元素,它形成的物质种类很多。
(1)生石灰溶于水,该反应过程中能量的变化是___________ (填“吸热”或“放热”)。所以,在实验室中,生石灰应___________ 保存。
(2)实验小组同学将Na2CO3溶液滴加到CaCl2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:NaCl;猜想二:NaCl和CaCl2;猜想三:NaCl和________
【实验过程】
【拓展延伸】实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小明用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液)。四组实验数据记录如下表。请分析计算:
①反应后,稀盐酸还有剩余的是第_________ 组。
②求表中m的值_________ (结果精确到0.1g)。
(1)生石灰溶于水,该反应过程中能量的变化是
(2)实验小组同学将Na2CO3溶液滴加到CaCl2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:NaCl;猜想二:NaCl和CaCl2;猜想三:NaCl和
【实验过程】
| 实验步骤 | 现象 | 结论 |
| 实验Ⅰ:取滤液,向其中滴入适量Na2CO3溶液 | 猜想二不成立 | |
| 实验Ⅱ:另取滤液,向其中加入足量 | 产生气泡 | 猜想三成立 |
【拓展延伸】实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小明用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液)。四组实验数据记录如下表。请分析计算:
| 实验组别 | 一 | 二 | 三 | 四 |
| 稀盐酸质量/g | 100.0 | 100.0 | 100.0 | 100.0 |
| 混合物质量/g | 6.0 | 12.0 | 18.0 | 24.0 |
| 所得溶液质量/g | 103.8 | 107.6 | 110.0 | 111.0 |
| 剩余固体质量 | 0 | 0 | m | n |
①反应后,稀盐酸还有剩余的是第
②求表中m的值
您最近一年使用:0次
综合应用题
|
困难
(0.15)
【推荐3】海洋是一个远未完全开发的巨大化学资源宝库,海洋资源的综合利用具有非常广阔的前景。工业上从海水中可提取许多广泛应用于生活、生产、科技等方面的物质和原料。
Ι.从海水中获得淡水
下列方法常用于海水淡化的是____________ (填字母)。
A.蒸馏法 B.吸附法 C.沉淀法 D.过滤法
Ⅱ.从海水中提取溴(Br2)
工业上通常是将氯气通入海水晒盐后的母液中,将溶液中的溴化钠(NaBr)转化为溴单质(Br2),然后鼓入热空气,使溴单质(Br2)从溶液中挥发出来,冷凝后得到粗溴。该过程中主要反应的化学方程式为_______________________ ,其反应类型是 ______________ 。
Ⅲ.从海水中提取金属镁
镁及其合金是一种用途很广的金属材料,工业上从海水晒盐后的母液中提取镁的主要流程如下:
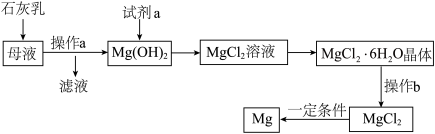
试回答下列问题:
(1)石灰乳主要成分的化学式为_____________ 。
(2)Mg(OH)2中加入试剂a发生反应的化学方程式为____________________________ 。
(3)操作b是在HCl气体氛围中高温灼烧进行的。若直接灼烧MgCl2·6H2O晶体,则生成MgO和另外两种化合物,写出有关反应的化学方程式___________________________ 。
Ⅳ.以海水中提取的食盐为原料制备纯碱
制备过程中主要涉及以下三步反应:
① CO2+NH3+H2O =NH4HCO3
② NH4HCO3 + NaCl=NaHCO3 ↓ + NH4Cl
③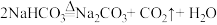
试回答下列问题:
(1)制备过程中可以直接循环回收利用的物质是H2O和__________________ 。
(2)在实验室里证明反应③中的NaHCO3已完全分解的具体操作是________ 。
(3)某化学兴趣小组认为,在碳酸氢钠完全分解的情况下,所得的纯碱中也会混有来自反应②中的杂质,为此他们进行了如下探究:
a.取2.2g纯碱样品,加水完全溶解得100g溶液;
b.配制100g 3.65%的稀盐酸;
c.取上述一种溶液25g于锥形瓶中,再将另一种溶液逐滴加入锥形瓶内,反应后溶液的pH变化情况如下图所示。

步骤c中当滴入另一种溶液为10g时,锥形瓶内物质恰好完全反应。则纯碱样品中碳酸钠的质量分数为___________ (写出计算过程,计算结果保留1位小数)
Ι.从海水中获得淡水
下列方法常用于海水淡化的是
A.蒸馏法 B.吸附法 C.沉淀法 D.过滤法
Ⅱ.从海水中提取溴(Br2)
工业上通常是将氯气通入海水晒盐后的母液中,将溶液中的溴化钠(NaBr)转化为溴单质(Br2),然后鼓入热空气,使溴单质(Br2)从溶液中挥发出来,冷凝后得到粗溴。该过程中主要反应的化学方程式为
Ⅲ.从海水中提取金属镁
镁及其合金是一种用途很广的金属材料,工业上从海水晒盐后的母液中提取镁的主要流程如下:

试回答下列问题:
(1)石灰乳主要成分的化学式为
(2)Mg(OH)2中加入试剂a发生反应的化学方程式为
(3)操作b是在HCl气体氛围中高温灼烧进行的。若直接灼烧MgCl2·6H2O晶体,则生成MgO和另外两种化合物,写出有关反应的化学方程式
Ⅳ.以海水中提取的食盐为原料制备纯碱
制备过程中主要涉及以下三步反应:
① CO2+NH3+H2O =NH4HCO3
② NH4HCO3 + NaCl=NaHCO3 ↓ + NH4Cl
③
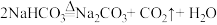
试回答下列问题:
(1)制备过程中可以直接循环回收利用的物质是H2O和
(2)在实验室里证明反应③中的NaHCO3已完全分解的具体操作是
(3)某化学兴趣小组认为,在碳酸氢钠完全分解的情况下,所得的纯碱中也会混有来自反应②中的杂质,为此他们进行了如下探究:
a.取2.2g纯碱样品,加水完全溶解得100g溶液;
b.配制100g 3.65%的稀盐酸;
c.取上述一种溶液25g于锥形瓶中,再将另一种溶液逐滴加入锥形瓶内,反应后溶液的pH变化情况如下图所示。

步骤c中当滴入另一种溶液为10g时,锥形瓶内物质恰好完全反应。则纯碱样品中碳酸钠的质量分数为
您最近一年使用:0次
综合应用题
|
困难
(0.15)
【推荐1】在生活生产中,含锰物质的应用较为广泛。
(一)含锰物质的有关知识
(1)植物生长需微量的锰,这里的锰是指_____ (选填序号)。
a 原子
b 单质
c 元素
(2)实验室用双氧水制氧气,须在其中加MnO2,其作用是_____ 。
(3)普通锌﹣锰干电池是由锌筒、电解质层、炭包、炭棒、铜帽、封口剂、电池盖和商标、热塑套(或铁皮)等组成。以上叙述中不涉及到_____ (选填序号)。
A 金属材料
B 无机非金属材料
C 合成材料
D 复合材料
(4)四氧化三锰是制金属锰的原料,在空气中灼烧主要成分为MnCO3的菱锰矿(其它成分不含锰)可生产四氧化三锰,该反应的化学方程式为_____ 。
(二)制取硫酸锰铵晶体
软锰矿主要成分为MnO2(含少量Fe2O3、SiO2等),可用于制备硫酸锰铵晶体。
(1)取经粉碎软锰矿先后加硫酸、草酸溶液,得MnSO4、Fe2(SO4)3混合溶液,加适量MnCO3消耗多余硫酸并将Fe2(SO4)3转化为沉淀,再趁热过滤得MnSO4溶液。
①将软锰矿粉碎的目的是_____ 。
②MnCO3和硫酸发生复分解反应的化学方程式为_____ 。
(2)用以上热MnSO4溶液和过量(NH4)2SO4并采用冰水浴制硫酸锰铵晶体,反应装置如图1.

①下列说法正确的是_____ (选填序号)。
a用过量(NH4)2SO4能提高晶体产率
b采用冰水浴可加速晶体形成
②从制备装置中分离出的晶体须经洗涤、滤纸吸干。
选用酒精洗涤晶体,其优点是_____ 。
(三)硫酸锰铵晶体的热分解实验
取12.27g硫酸锰铵晶体[(NH4)2SO4•MnSO4•7H2O],用图2装置进行热分解实验。

【查阅资料】371℃时,(NH4)2SO4•MnSO4•7H2O(相对分子质量409)完全失去结晶水。剩余物质在850℃完全分解为锰的某氧化物、NH3、H2O、SO2、SO3。
(1)装配好实验装置后,先要_____ 。
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是防止倒吸和_____ 。控制不同的温度对A中固体加热,测得装置B和C中的质量变化如下表、剩余固体质量随温度的变化如图3所示。

①图中m1的值为_____ ,m2的值为_____ 。
②F点对应固体的化学式为_____ 。
③将图中H点固体在空气中充分加热,发现固体增加0.32g后质量不再改变,写出此过程中发生反应的化学方程式_____ 。
(一)含锰物质的有关知识
(1)植物生长需微量的锰,这里的锰是指
a 原子
b 单质
c 元素
(2)实验室用双氧水制氧气,须在其中加MnO2,其作用是
(3)普通锌﹣锰干电池是由锌筒、电解质层、炭包、炭棒、铜帽、封口剂、电池盖和商标、热塑套(或铁皮)等组成。以上叙述中不涉及到
A 金属材料
B 无机非金属材料
C 合成材料
D 复合材料
(4)四氧化三锰是制金属锰的原料,在空气中灼烧主要成分为MnCO3的菱锰矿(其它成分不含锰)可生产四氧化三锰,该反应的化学方程式为
(二)制取硫酸锰铵晶体
软锰矿主要成分为MnO2(含少量Fe2O3、SiO2等),可用于制备硫酸锰铵晶体。
(1)取经粉碎软锰矿先后加硫酸、草酸溶液,得MnSO4、Fe2(SO4)3混合溶液,加适量MnCO3消耗多余硫酸并将Fe2(SO4)3转化为沉淀,再趁热过滤得MnSO4溶液。
①将软锰矿粉碎的目的是
②MnCO3和硫酸发生复分解反应的化学方程式为
(2)用以上热MnSO4溶液和过量(NH4)2SO4并采用冰水浴制硫酸锰铵晶体,反应装置如图1.

①下列说法正确的是
a用过量(NH4)2SO4能提高晶体产率
b采用冰水浴可加速晶体形成
②从制备装置中分离出的晶体须经洗涤、滤纸吸干。
选用酒精洗涤晶体,其优点是
(三)硫酸锰铵晶体的热分解实验
取12.27g硫酸锰铵晶体[(NH4)2SO4•MnSO4•7H2O],用图2装置进行热分解实验。

【查阅资料】371℃时,(NH4)2SO4•MnSO4•7H2O(相对分子质量409)完全失去结晶水。剩余物质在850℃完全分解为锰的某氧化物、NH3、H2O、SO2、SO3。
(1)装配好实验装置后,先要
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是防止倒吸和
| 温度/℃ | 室温 | 371 | 850 |
| B装置/g | 200.00 | 203.78 | 208.96 |
| C装置/g | 200.00 | 200.00 | 201.02 |

①图中m1的值为
②F点对应固体的化学式为
③将图中H点固体在空气中充分加热,发现固体增加0.32g后质量不再改变,写出此过程中发生反应的化学方程式
您最近一年使用:0次
综合应用题
|
困难
(0.15)
解题方法
【推荐2】金属材料是人类社会发展的见证者,人类文明的发展和社会的进步同金属材料关系十分密切。
(一)金属初探
(1)铜在空气中加热会逐渐变黑,写出该反应的化学方程式____________ 。
(2)硬铝、不锈钢是常见的金属材料。它们属于__________ (选填“合金”或“纯金属”)。
(3)为了减少和避免雷电对高层建筑的危害,需安装由金属材料制成的避雷装置,这主要是利用了金属材料的_______________ 。(填序号)
a.密度大 b.导电性 c.导热性 d.熔点高
(二)一氧化碳还原氧化铁
【查阅资料】氢氧化钠溶液能吸收二氧化碳;
兴趣小组设计了如图实验装置进行实验。

(1)实验前应先____________ 。
(2)加热前应先通CO一会,其作用是_______ ,实验结束后,应先 _____ 。(选填“停止加热”或“停止通CO”)
(3)将一定质量的氧化铁粉末放入玻璃管中,反应一段时间后,得到黑色固体粉末,并能全被磁铁吸引。兴趣小组猜想黑色粉末可能是
①铁粉;②四氧化三铁;③你的猜想是___________ 。
实验证明黑色粉末全是四氧化三铁,请写出该变化的化学方程式_____________ 。
(4)为收集尾气并除去气体样品中的二氧化碳,下列装置最为合理的是________ 。(填序号)

(三)铜锈成分的确定
【查阅资料】
①铜锈的主要成分可以看成是aCu(OH)2•bCuCO3。
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物。
③Cu(OH)2的分解温度为66℃~68℃,CuCO3的分解温度为200℃~220℃。
小组同学用热分析仪对aCu(OH)2•bCuCO3固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如右图,请根据图示回答下列问题:

(1)写出A B、C D段发生反应的化学方程式:AB段:________ ;CD段: _________ ;
(2)BC段固体为___________________ ;
(3)通过计算可得: a:b=___________ 。
(4)若将16.0g剩余固体继续加热到更高的温度,发现 固体质量减少了1.6g后质量不再改变,写出此过程中可能发生反应的化学方程式:_____________ 。
(一)金属初探
(1)铜在空气中加热会逐渐变黑,写出该反应的化学方程式
(2)硬铝、不锈钢是常见的金属材料。它们属于
(3)为了减少和避免雷电对高层建筑的危害,需安装由金属材料制成的避雷装置,这主要是利用了金属材料的
a.密度大 b.导电性 c.导热性 d.熔点高
(二)一氧化碳还原氧化铁
【查阅资料】氢氧化钠溶液能吸收二氧化碳;
| 铁及铁的氧化物 | Fe | FeO | Fe2O3 | Fe3O4 |
| 颜色 | 黑色 | 黑色 | 红棕色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |

(1)实验前应先
(2)加热前应先通CO一会,其作用是
(3)将一定质量的氧化铁粉末放入玻璃管中,反应一段时间后,得到黑色固体粉末,并能全被磁铁吸引。兴趣小组猜想黑色粉末可能是
①铁粉;②四氧化三铁;③你的猜想是
实验证明黑色粉末全是四氧化三铁,请写出该变化的化学方程式
(4)为收集尾气并除去气体样品中的二氧化碳,下列装置最为合理的是

(三)铜锈成分的确定
【查阅资料】
①铜锈的主要成分可以看成是aCu(OH)2•bCuCO3。
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物。
③Cu(OH)2的分解温度为66℃~68℃,CuCO3的分解温度为200℃~220℃。
小组同学用热分析仪对aCu(OH)2•bCuCO3固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如右图,请根据图示回答下列问题:

(1)写出A B、C D段发生反应的化学方程式:AB段:
(2)BC段固体为
(3)通过计算可得: a:b=
(4)若将16.0g剩余固体继续加热到更高的温度,发现 固体质量减少了1.6g后质量不再改变,写出此过程中可能发生反应的化学方程式:
您最近一年使用:0次
综合应用题
|
困难
(0.15)
【推荐1】根据所学知识解答:
(1)青少年缺“钙”易患的疾病是______ 。
(2)即热型快餐加热原理:利用生石灰和水反应放热,用化学方程式表示其反应______ 。
(二)过氧化钙(CaO2)的性质
(3)CaO2能与稀盐酸发生复分解反应,反应的化学方程式为______ 。
(4)鱼类运输的增氧剂主要含有CaO2,它与水缓慢反应生成O2,还生成一种碱,其化学式为:______ 。
(三)过氧化钙晶体的制备
【资料】过氧化钙晶体(CaO2•yH2O),常温为白色,能溶于酸,难溶于酒精。
制备原理:CaCl2+H2O2+NH3+H2O→CaO2•yH2O↓+NH4Cl,装置如图1。

(5)装置A中试管内发生反应的化学方程式为______ 。
(6)装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ、该反应是放热反应,温度低有利于提高CaO2•yH2O产率;
Ⅱ、______ 。
(7)反应结束后,经过滤、洗涤、低温烘干可获得CaO2•yH2O。
①洗涤时采用95%的酒精溶液洗涤的优点是减少晶体损失,易于干燥。
②检验晶体已洗涤干净的方法为______ 。
(四)过氧化钙晶体组成的测定
称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(图2)(过氧化钙晶体受热时会先失去结晶水)。
(8)根据图2可知y=______ 。
(9)350℃时发生反应的化学方程式为______ 。
(1)青少年缺“钙”易患的疾病是
(2)即热型快餐加热原理:利用生石灰和水反应放热,用化学方程式表示其反应
(二)过氧化钙(CaO2)的性质
(3)CaO2能与稀盐酸发生复分解反应,反应的化学方程式为
(4)鱼类运输的增氧剂主要含有CaO2,它与水缓慢反应生成O2,还生成一种碱,其化学式为:
(三)过氧化钙晶体的制备
【资料】过氧化钙晶体(CaO2•yH2O),常温为白色,能溶于酸,难溶于酒精。
制备原理:CaCl2+H2O2+NH3+H2O→CaO2•yH2O↓+NH4Cl,装置如图1。

(5)装置A中试管内发生反应的化学方程式为
(6)装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ、该反应是放热反应,温度低有利于提高CaO2•yH2O产率;
Ⅱ、
(7)反应结束后,经过滤、洗涤、低温烘干可获得CaO2•yH2O。
①洗涤时采用95%的酒精溶液洗涤的优点是减少晶体损失,易于干燥。
②检验晶体已洗涤干净的方法为
(四)过氧化钙晶体组成的测定
称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(图2)(过氧化钙晶体受热时会先失去结晶水)。
(8)根据图2可知y=
(9)350℃时发生反应的化学方程式为
您最近一年使用:0次



