通过海水提取的粗盐中含有 MgCl2、CaCl2、MgSO4.以及泥沙等杂质.以下是一种 制备精盐的实验方案(用于沉淀的试剂均过量).
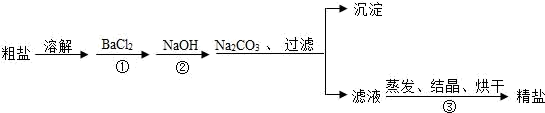
请回答下列问题:
(1)写出②中反应的化学方程式___________________________ .
(2)加入 BaCl2、NaOH、Na2CO3 的顺序还可以改变吗?若能改变则写出改变的顺序,若不能改变,请说明理由_______________________________________ .
(3)该实验方案还需完善,请写出具体的操作步骤___________________________________________ .

请回答下列问题:
(1)写出②中反应的化学方程式
(2)加入 BaCl2、NaOH、Na2CO3 的顺序还可以改变吗?若能改变则写出改变的顺序,若不能改变,请说明理由
(3)该实验方案还需完善,请写出具体的操作步骤
更新时间:2019-11-05 16:14:34
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如下图所示,向加有不同试剂的点滴板孔穴中分别滴加稀盐酸,研究物质的性质。
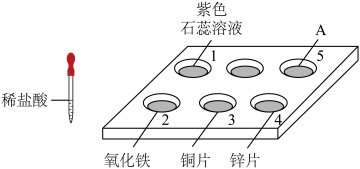
(1)孔穴1中观察到的现象是___________ 。
(2)孔穴2中的溶液变黄,反应的化学方程式为___________ 。
(3)从金属活动性的角度解释孔穴3、4现象不同的原因是___________ 。
(4)孔穴5中的现象为溶液由红色变为无色,则A可能是NaOH溶液和___________ 的混合液。

(1)孔穴1中观察到的现象是
(2)孔穴2中的溶液变黄,反应的化学方程式为
(3)从金属活动性的角度解释孔穴3、4现象不同的原因是
(4)孔穴5中的现象为溶液由红色变为无色,则A可能是NaOH溶液和
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】写出一种鉴别Fe粉和CuO粉末的化学方法。
| 实验方法 | 现象 | 结论 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】胆矾易溶于水,是一种重要的化工原料。某研究小组以生锈的铜屑为原料制备胆矾(CuSO4·5H2O),其流程如下:

(1)实验室进行操作①中的过滤时,玻璃棒的作用是___________ 。
(2)操作②所得的混合液中一定含有的阳离子有___________ (均填离子符号)。
(3)操作③能得到胆矾,说明胆矾的溶解度随温度的升高而___________ 。
(4)经操作④得到的胆矾不能用水洗涤的主要原因是___________ 。

(1)实验室进行操作①中的过滤时,玻璃棒的作用是
(2)操作②所得的混合液中一定含有的阳离子有
(3)操作③能得到胆矾,说明胆矾的溶解度随温度的升高而
(4)经操作④得到的胆矾不能用水洗涤的主要原因是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】中国首款完全自主知识产权民用客机C919飞机的钛合金用量达9.3%,工业上利用钛铁矿(主要成分为FeTiO3)制取钛并获得副产品A的主要工艺流程如图1所示:
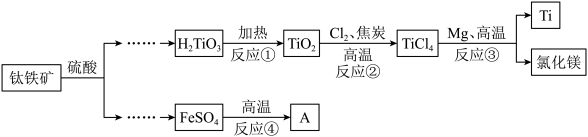
请回答下列问题:
(1)构成金属钛的微粒是_________ (填“分子”或“原子”或“离子”)。
(2)在加入硫酸前,需将铁钛矿粉碎,其目的是____________ 。
(3)该反应需持续通入氩气,氩气的作用是____________ 。
(4)反应④中FeSO4高温分解产物除红色固体A外。还有SO3和另外一种与SO3相对分子质量相差16的氧化物,制该反应的化学方程式为________ 。
(5)反应①②③④中属于分解反应的是___________ (填“①”、“②”、“③”、“④”)。
(6)让你对该工艺流程提出处理尾气的建议_________ (只写一条)。

请回答下列问题:
(1)构成金属钛的微粒是
(2)在加入硫酸前,需将铁钛矿粉碎,其目的是
(3)该反应需持续通入氩气,氩气的作用是
(4)反应④中FeSO4高温分解产物除红色固体A外。还有SO3和另外一种与SO3相对分子质量相差16的氧化物,制该反应的化学方程式为
(5)反应①②③④中属于分解反应的是
(6)让你对该工艺流程提出处理尾气的建议
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】CO2的捕捉是减少碳排放的措施之一、一种利用NaOH溶液捕捉回收CO2的工艺流程如下。

(1)Na2CO3中碳元素的化合价为___________ 。
(2)“捕捉室”中NaOH溶液常喷成雾状,主要目的是___________ 。
(3)“捕捉室”中发生反应的化学方程式为___________ 。
(4)“高温反应炉”中发生反应的基本反应类型是___________ 。
(5)流程中可循环使用的物质是___________ (写出1种即可)。

(1)Na2CO3中碳元素的化合价为
(2)“捕捉室”中NaOH溶液常喷成雾状,主要目的是
(3)“捕捉室”中发生反应的化学方程式为
(4)“高温反应炉”中发生反应的基本反应类型是
(5)流程中可循环使用的物质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】在上海世博园江苏馆的“春华秋实”展区,用我市东海水晶雕出的作品《寄畅园之冬》吸引了众多参观者的眼球。东海县石国家火炬计划硅胶材料产业化基地,产品由晶莹剔透的成分为SiO2)是制取高纯硅的主要原料,高纯硅又是制造计算机芯片的主要原料。
①SiO2+2C Si(粗)+2CO↑
Si(粗)+2CO↑
②Si(粗)+2Cl2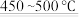 SiCl4
SiCl4
③SiCl4+2H2 Si(纯)+4HCl
Si(纯)+4HCl
其生产过程示意图如下:

请你自学上述资料后,回答下列问题
(1)由石英砂制得高纯硅的反应原理中,属于化合反应的是________ 填数字代号,下同),属于置换反应的是 _______
(2)粗硅提纯必须在无氧的氛围中进行,除了考虑到硅易被氧化成二氧化硅外,还有一个原因是_______
(3)生产过程示意图中的“物质A”用水吸收,可得副产品(一种常见的酸)的名称是____
(4)作为电器、电子、光纤等行业原料的石英砂纯度要求高,需要对普通石英砂(含有少量的CaCO3、Fe2O3)进行提纯,其中酸洗(用盐酸)和高纯水洗是两个最重要的步骤。请写出酸洗步骤中的一个反应的化学方程式_____ (任写一个);判断高纯水洗是否洗净的方法是:取少量最后的洗涤液于试管中,向其中滴加AgNO3溶液,若无 _____ 现象,则表明残留物已洗净;否则,表明残留物未洗净。
①SiO2+2C
 Si(粗)+2CO↑
Si(粗)+2CO↑②Si(粗)+2Cl2
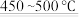 SiCl4
SiCl4③SiCl4+2H2
 Si(纯)+4HCl
Si(纯)+4HCl其生产过程示意图如下:

请你自学上述资料后,回答下列问题
(1)由石英砂制得高纯硅的反应原理中,属于化合反应的是
(2)粗硅提纯必须在无氧的氛围中进行,除了考虑到硅易被氧化成二氧化硅外,还有一个原因是
(3)生产过程示意图中的“物质A”用水吸收,可得副产品(一种常见的酸)的名称是
(4)作为电器、电子、光纤等行业原料的石英砂纯度要求高,需要对普通石英砂(含有少量的CaCO3、Fe2O3)进行提纯,其中酸洗(用盐酸)和高纯水洗是两个最重要的步骤。请写出酸洗步骤中的一个反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】下列流程中的物质均为初中化学常见的物质,其中A、B、D均属于氧化物,如图是它们之间的相互转化关系,部分生成物已经略去。请回答:
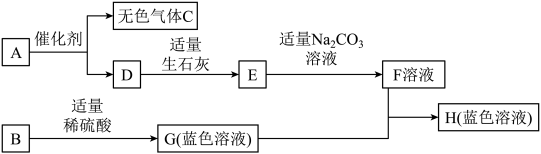
(1)写出B的化学式:____________ ;
(2)试写出图中G与F反应生成H的化学方程式:____________ ;
(3)图中化学反应D→E的基本反应类型是:____________ ;
(4)写出E的一种用途_________ 。

(1)写出B的化学式:
(2)试写出图中G与F反应生成H的化学方程式:
(3)图中化学反应D→E的基本反应类型是:
(4)写出E的一种用途
您最近一年使用:0次
【推荐3】海水是一种取之不尽、用之不竭的资源宝库。请围绕科学利用海水资源,填写空格:
(1)用海水“晒盐”的方法得到的粗盐中,除氯化钠外,还含有氯化镁、氯化钙、硫酸钠等杂质。将此粗盐提纯的部分实验方案如下:

①加入碳酸钠溶液的目的是_______ 。
②过滤后得到的沉淀成分有:氢氧化镁、碳酸钙、_______ 。
③在滤液中加入稀盐酸时发生中和反应的化学方程式_______ 。
④请设计实验,能通过清晰可见的现象,准确控制在少量滤液样品中加入稀盐酸,至恰好完全反应:__________ 。
(2)利用制得精盐水,进行如下流程,制取纯碱
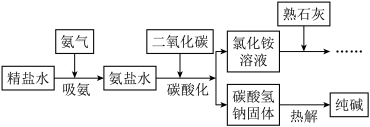
①向饱和食盐水中通入过量氨气制成饱和氨盐水的目的是________ 。
②碳酸氢钠比氯化铵更容易析出的原因________ 。
(1)用海水“晒盐”的方法得到的粗盐中,除氯化钠外,还含有氯化镁、氯化钙、硫酸钠等杂质。将此粗盐提纯的部分实验方案如下:

①加入碳酸钠溶液的目的是
②过滤后得到的沉淀成分有:氢氧化镁、碳酸钙、
③在滤液中加入稀盐酸时发生中和反应的化学方程式
④请设计实验,能通过清晰可见的现象,准确控制在少量滤液样品中加入稀盐酸,至恰好完全反应:
(2)利用制得精盐水,进行如下流程,制取纯碱

①向饱和食盐水中通入过量氨气制成饱和氨盐水的目的是
②碳酸氢钠比氯化铵更容易析出的原因
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】为除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加入过量BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。
【提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性】
(1)以上操作中所发生的复分解反应共有______ 个。
(2)加入过量Na2CO3溶液的目的是______ ?写出CaCl2与Na2CO3反应的化学方程式______ 。
(3)小明加入适量稀盐酸是忘记观察现象。现想通过实验判断溶液中除了氯化钠外溶液中的成分。
①向溶液中滴加稀盐酸,有气体生成,由此认为溶液中含有碳酸钠,不含盐酸。结论否合理?______ ,理由是______ 。
②向溶液中滴加酚酞试液。溶液变成红色,由此认为溶液中含有氢氧化钠。结论否合理?______ ,理由是______ 。
【提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性】
(1)以上操作中所发生的复分解反应共有
(2)加入过量Na2CO3溶液的目的是
(3)小明加入适量稀盐酸是忘记观察现象。现想通过实验判断溶液中除了氯化钠外溶液中的成分。
①向溶液中滴加稀盐酸,有气体生成,由此认为溶液中含有碳酸钠,不含盐酸。结论否合理?
②向溶液中滴加酚酞试液。溶液变成红色,由此认为溶液中含有氢氧化钠。结论否合理?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】中国传统文化中蕴含着丰富的化学知识。
(1)《本草纲目》记载,杨桃具有去风热、生津止渴等功效。杨桃的主要成分是水,还有蔗糖、蛋白质和维生素等,经测定酸杨桃的pH为1.35,甜杨桃的pH为1.81,其中酸性较强的是___________ (填“酸杨桃”或“甜杨桃”)。
(2)《四川盐法志》记载,“敞锅熬盐”主要步骤为:①将黄卤水(主要成分是NaCl、MgSO4)和黑卤水(主要成分是NaCl、BaCl2)按照一定比例混合;②过滤,将滤液放入敞口锅中加热浓缩,析出粗盐;③用“花水”冲洗粗盐获得精盐。步骤①中产生白色沉淀的化学方程式为___________ ;步骤②中“敞锅熬盐”与___________ 的原理相同;步骤③用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl,则“花水”应当是___________ (填标号)。
A.蒸馏水B.饱和NaCl溶液C.饱和NaOH溶液D.饱和BaCl2溶液
(3)中华医学博大精深,我国古代典籍中记载有“银针验毒”的原理,其反应方程式为: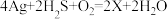 ,X的化学式是
,X的化学式是___________ 。
(1)《本草纲目》记载,杨桃具有去风热、生津止渴等功效。杨桃的主要成分是水,还有蔗糖、蛋白质和维生素等,经测定酸杨桃的pH为1.35,甜杨桃的pH为1.81,其中酸性较强的是
(2)《四川盐法志》记载,“敞锅熬盐”主要步骤为:①将黄卤水(主要成分是NaCl、MgSO4)和黑卤水(主要成分是NaCl、BaCl2)按照一定比例混合;②过滤,将滤液放入敞口锅中加热浓缩,析出粗盐;③用“花水”冲洗粗盐获得精盐。步骤①中产生白色沉淀的化学方程式为
A.蒸馏水B.饱和NaCl溶液C.饱和NaOH溶液D.饱和BaCl2溶液
(3)中华医学博大精深,我国古代典籍中记载有“银针验毒”的原理,其反应方程式为:
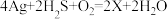 ,X的化学式是
,X的化学式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】从海水得到的粗盐,往往含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须分离和提纯后才能用于工业生产和人们的日常生活。粗盐提纯的部分流程如图:
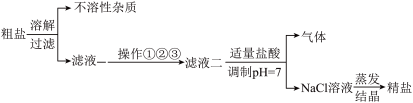
其中,滤液一至滤液二之间需进行三步操作:
操作①:加入过量的碳酸钠,除去滤液中的Ca2+;
操作②:加入过量的X,除去滤液中的Mg2+;
操作③:加入过量的氯化钡,除去滤液中的 。
。
请回答:
(1)操作中的物质X为_________ ,正确的操作顺序为_________ (填序号),
(2)为最终获得精盐,操作①、②和③后还需增加的操作是_________ 。

其中,滤液一至滤液二之间需进行三步操作:
操作①:加入过量的碳酸钠,除去滤液中的Ca2+;
操作②:加入过量的X,除去滤液中的Mg2+;
操作③:加入过量的氯化钡,除去滤液中的
 。
。请回答:
(1)操作中的物质X为
(2)为最终获得精盐,操作①、②和③后还需增加的操作是
您最近一年使用:0次



