小华测定Cu-Zn合金及Cu-Ag合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀盐酸和必要的仪器。
(1)你认为能测出其铜的质量分数的是_____合金。
(2)小明取该合金的粉末65g与足量该盐酸充分反应,经测定,产生了0.4g气体,请求出该合金中铜的质量分数?
(1)你认为能测出其铜的质量分数的是_____合金。
(2)小明取该合金的粉末65g与足量该盐酸充分反应,经测定,产生了0.4g气体,请求出该合金中铜的质量分数?
2012·安徽马鞍山·中考模拟 查看更多[14]
2023-2024九化课后作业与单元测试 沪教版 第5章 单元测试B卷2024年湖北省初中学业水平考试模拟演练化学训练设计(02卷)河北省邯郸市第十三中学2023-2024学年九年级上学期11月月考化学试题(实验班)(已下线)第5章 金属的冶炼和利用(章末检测卷)-2023-2024学年九年级化学上册同步精品课堂(沪教版)河北省邯郸市鸡泽县2022-2023学年九年级上学期期末化学试题吉林省白城市洮北区白城市第三中学2021-2022学年九年级上学期第三次学科测查化学试题黑龙江省绥化市绥棱县绥中乡学校2021-2022学年九年级上学期期中化学试题河北省衡水市武邑县武邑中学2019-2020学年九年级下学期3月月考(网考)化学试题贵州省遵义市道真县2018-2019学年九年级下学期第一次联考化学试题广东省九年级人教版第八单元金属和金属材料单元测试题2017-2018年人教版九年级化学第八单元测试题2017-2018学年沪教版九年级化学第5章 金属与矿物 单元测试(已下线)2015届云南省腾冲县五校初三上学期联考化学试卷(已下线)2012届安徽省当涂县第三次四校联考中考模拟化学试卷
更新时间:2019-12-09 01:13:37
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】碳酸钙在高温条件下生成氧化钙和二氧化碳(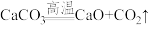 )。现有10g碳酸钙,高温煅烧一段时间后停止加热,剩余固体的质量是7.8g。
)。现有10g碳酸钙,高温煅烧一段时间后停止加热,剩余固体的质量是7.8g。
(1)反应中生成二氧化碳的质量是_________ 。
(2)利用化学方程式计算生成的氧化钙的质量。
(3)计算剩余固体中各元素的质量。
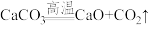 )。现有10g碳酸钙,高温煅烧一段时间后停止加热,剩余固体的质量是7.8g。
)。现有10g碳酸钙,高温煅烧一段时间后停止加热,剩余固体的质量是7.8g。(1)反应中生成二氧化碳的质量是
(2)利用化学方程式计算生成的氧化钙的质量。
(3)计算剩余固体中各元素的质量。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某化学兴趣小组在实验室用碳酸钠溶液和熟石灰固体制取少量氢氧化钠溶液.他们的实验过程和相关数据如图所示.请计算:

(1)实验中生成沉淀的质量为_______ g;
(2)求碳酸钠溶液中的溶质的质量。(写出解题过程)
(3)若反应后滤液中的溶质质量为M,则所得滤液的溶质质量分数的计算式可表示为_____ (列出含M的计算式即可)。

(1)实验中生成沉淀的质量为
(2)求碳酸钠溶液中的溶质的质量。(写出解题过程)
(3)若反应后滤液中的溶质质量为M,则所得滤液的溶质质量分数的计算式可表示为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】小苏打是发酵粉的主要成分,可用于制作发面食品。化学兴趣小组为测定某品牌小苏打样品(含杂质氯化钠)中碳酸氢钠的含量做了如下实验:将该样品8.55g放入锥形瓶中,加水全部溶解后,得到129.4g样品溶液,向该样品溶液中不断加入稀盐酸(如图),反应过程中锥形瓶中溶液质量的变化如下表所示(忽略二氧化碳在水中的溶解)。

试计算:
(1)当加入75g稀盐酸时,充分反应后所得溶液中的微粒有______ (填化学符号)。
(2)8.55g小苏打样品中碳酸氢钠的质量(写出计算过程,下同)。
(3)当锥形瓶内样品溶液中的碳酸氢钠与加入的稀盐酸恰好完全反应时,锥形瓶中溶液的溶质质量分数(计算结果精确至0.1%)。

| 加入稀盐酸的总质量/g | 25 | 50 | 75 |
| 锥形瓶中溶液的质量/g | 152.2 | 175 | 200 |
(1)当加入75g稀盐酸时,充分反应后所得溶液中的微粒有
(2)8.55g小苏打样品中碳酸氢钠的质量(写出计算过程,下同)。
(3)当锥形瓶内样品溶液中的碳酸氢钠与加入的稀盐酸恰好完全反应时,锥形瓶中溶液的溶质质量分数(计算结果精确至0.1%)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】“黄铜”是铜和锌的合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下。(烧杯质量均为56.5克)
请回答下列问题:
(1)_____同学用的稀盐酸和黄铜样品恰好完全反应,他制取的氢气的质量是_____。
(2)计算黄铜样品中锌的质量分数(要求写出计算过程)。
(3)计算盐酸的质量分数为_____。
| 1 | 甲 | 乙 | 丙 |
| 烧杯+稀盐酸质量 | 98.0g | 93.0g | 93.0g |
| 加入黄铜样品质量 | 10.0g | 12.0g | 10.0g |
| 充分反应后,烧杯+剩余物质质量 | 107.9g | 104.9g | 102.9g |
请回答下列问题:
(1)_____同学用的稀盐酸和黄铜样品恰好完全反应,他制取的氢气的质量是_____。
(2)计算黄铜样品中锌的质量分数(要求写出计算过程)。
(3)计算盐酸的质量分数为_____。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】黄铜(铜锌合金)因性能优良,被广泛用于制作钱币、饰品和生产中,铜的质量分数在59%~65%之间的黄铜性能优良。兴趣小组为了解某黄铜螺母的材料性能进行如下实验:取多个黄铜螺母放入烧杯中,另取 80g 稀硫酸,分四次等质量加入,每次均充分反应,得到实验数据如下表所示:
(1)m= 。所取黄铜螺母中铜的质量为 g。
(2)请通过计算说明该黄铜螺母的材料性能是否优良?
(3)计算稀硫酸中溶质的质量分数(写出计算过程)。
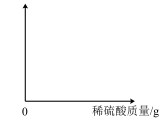
(4)分析实验数据,在下图坐标中画出加入 80g 稀硫酸过程中相应的曲线图(纵坐标为自行设定物质的质量;并标出曲线中必要的数据)。
| 实验次数 | 1 | 2 | 3 | 4 |
| 稀硫酸的用量/g | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 20.0 | 17.4 | m | 13.5 |
(1)m= 。所取黄铜螺母中铜的质量为 g。
(2)请通过计算说明该黄铜螺母的材料性能是否优良?
(3)计算稀硫酸中溶质的质量分数(写出计算过程)。
(4)分析实验数据,在下图坐标中画出加入 80g 稀硫酸过程中相应的曲线图(纵坐标为自行设定物质的质量;并标出曲线中必要的数据)。

您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】现有一块锌铜合金,某同学对其成分进行分析。取10g此样品,向其中分五次加入相同溶质质量分数的稀盐酸,使之充分反应,每次所用稀盐酸的质量及剩余固体的质量记录于下表:
试计算:
(1)表格中m的值为___________ 。
(2)所加入稀盐酸中溶质的质量分数。
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
充分反应后剩余固体的质量/g | 8.7 | 7.4 | 6.1 | 5.6 | m |
试计算:
(1)表格中m的值为
(2)所加入稀盐酸中溶质的质量分数。
您最近一年使用:0次



